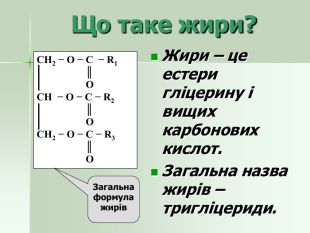
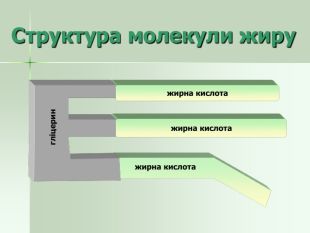
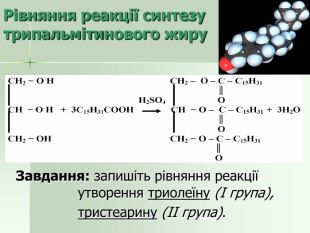
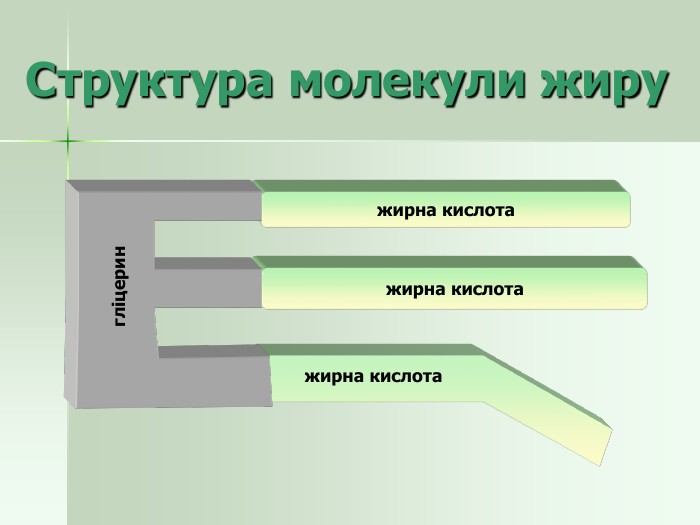
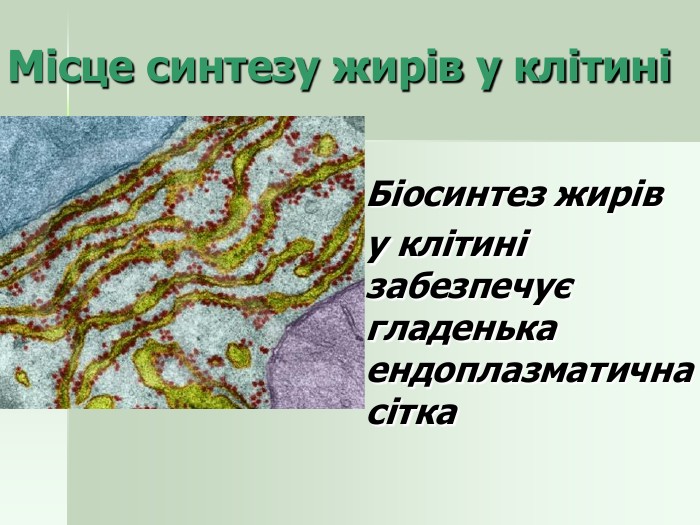
Презентація "Жири як представники естерів. Класифікація жирів, їхні хімічні властивості"





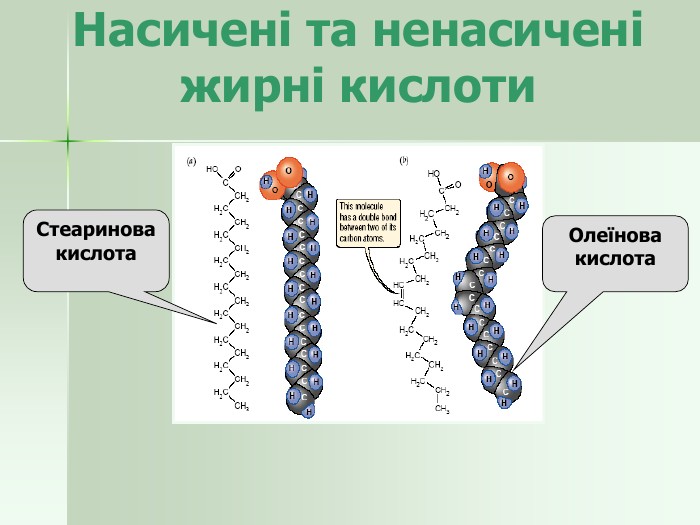





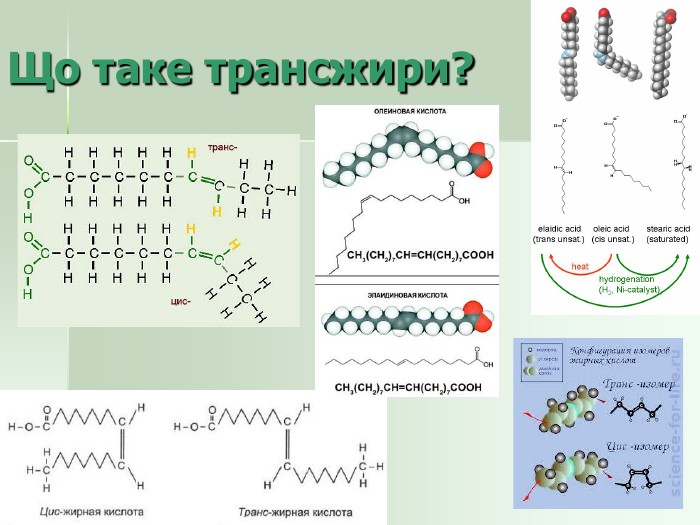








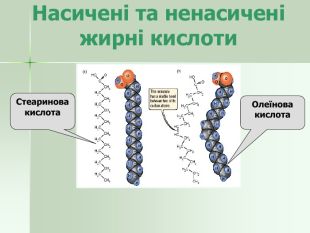
Кислоти – складові жирів Формула кислоти Назва кислоти Тип кислоти Природне джерело Пальмітинова Насичена Жири всіх тваринних тканин Стеаринова Насичена Жири всіх тваринних тканин Олеїнова Ненасичена Жири тканин та природні олії Лінолева Ненасичена Фосфоліпіди тканин та природних олій Ліноленова Ненасичена Фосфоліпіди тканин C15Н31СООН C17Н35СООН C17Н33СООН C17Н31СООН C17Н29СООН
З історії дослідження жирів 1741 р. – французький хімік Клод Жозеф Жоффруа (1685-1752) дією сильної неорганічної кислоти на мило добув масну на дотик суміш. Він припустив, що добута маса є жиром. Досліджуючи її властивості, науковець виявив, що це не так. Гідроліз жирів – хімічна реакція, за допомогою якої у 1779 р. шведський хімік Карл Вільгельм Шеєле виявив один з продуктів гідролізу (розкладання під дією води) жирів – гліцерин. 1817 р. – його співвітчизник Шеврьоль добув з жирів уже відому «солодку олію Шеєле». Сорок років потому Марселен Бертло встановив структуру гліцерину і з нього та вищих карбонових кислот синтезував жир. Отже, склад і структуру природних жирів було доведено експериментально.
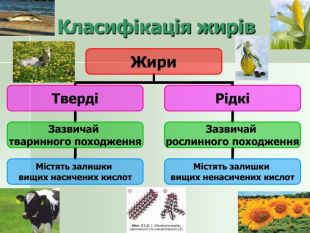
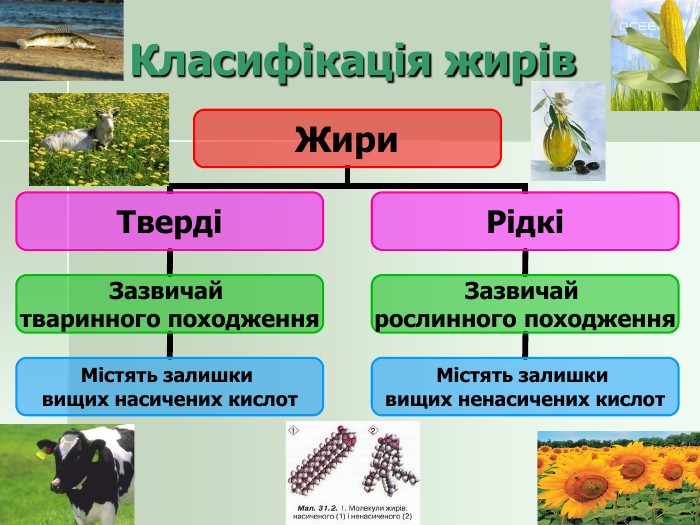
Фізичні властивості жирів 1. Агрегатний стан: Твердий – тваринні жири (крім риб’ячого); Рідкий – рослинні жири (крім кокосового і пальмового). 2. Температура плавлення залежить від складу жиру (жири, які містять залишки насичених кислот мають вищі температури плавлення). 3. Жири легші за воду. 4. Нерозчинні у воді, але розчинні в органічних розчинниках. Розчинник Чи розчинний жир Етиловий спирт малорозчинний Бензин розчинний Тетрахлорметан розчинний Вода нерозчинний
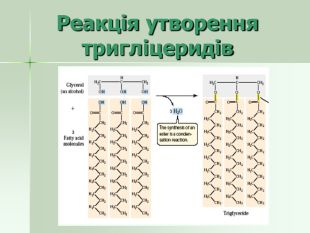
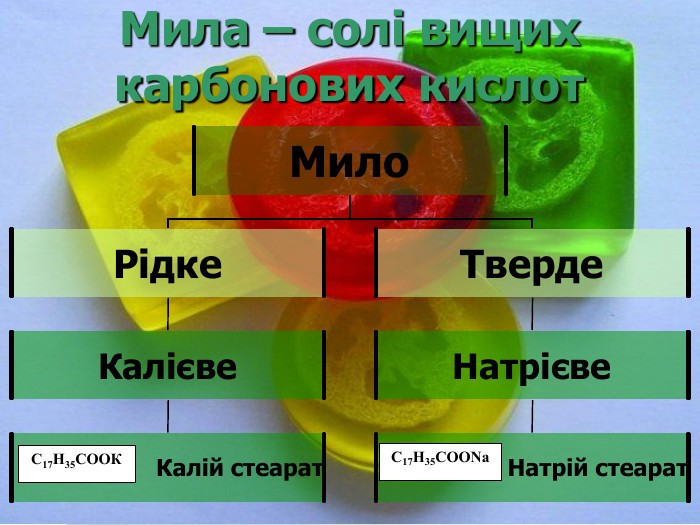
Гідроліз жирів Взаємодія з водою при t=200 – 250˚С та певному тиску або в присутності каталізатора: Реакція омилення – гідроліз у лужному середовищі: Завдання: напишіть рівняння гідролізу тристеарину у водному (І група) та лужному (ІІ група) середовищах СН2 − О − С − R СН2 – ОН ║ О СН − О − С − R + 3Н2О СН − ОН + 3R− СООН ║ О СН2 − О − С − R СН2 − ОН ║ О СН2 − О − С − R СН2 – ОН ║ О СН − О − С − R + 3КОН СН − ОН + 3R− СООК ║ О СН2 − О − С − R СН2 − ОН ║ О
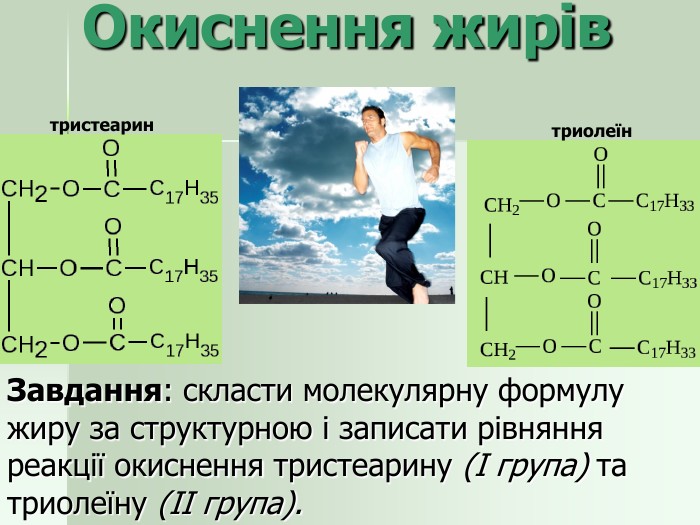
Гідрування жирів Приєднання до залишків ненасичених карбонових кислот атомів Гідрогену при t=160 – 240 ̊ С і наявності каталізатора: Перетворення рідких жирів на тверді. СН2 − О − С − С17Н33 СН2 – О – С − С17Н35 ║ ║ О О СН − О − С − С17Н33 + 3Н2 СН − О − С − С17Н35 ║ ║ О О СН2 − О − С − С17Н33 СН2 − О − С − С17Н35 ║ ║ О О
Історія походження маргарину 1860-і роки – французький хімік Іпполіт Меже Мур'є винайшов продукт, який в основному складався зі знежиреного молока та жиру яловичини, і назвав свій продукт «олеомаргарин»; У 1870 році у Франції в місті Пуассі почав працювати перший завод по виробництву маргарину; 1906 рік – С. Фокін здійснив першу гідрогенізацію жирів.
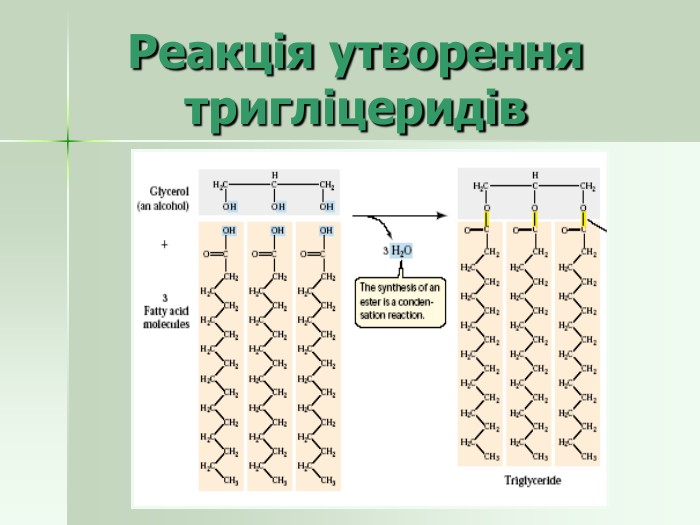
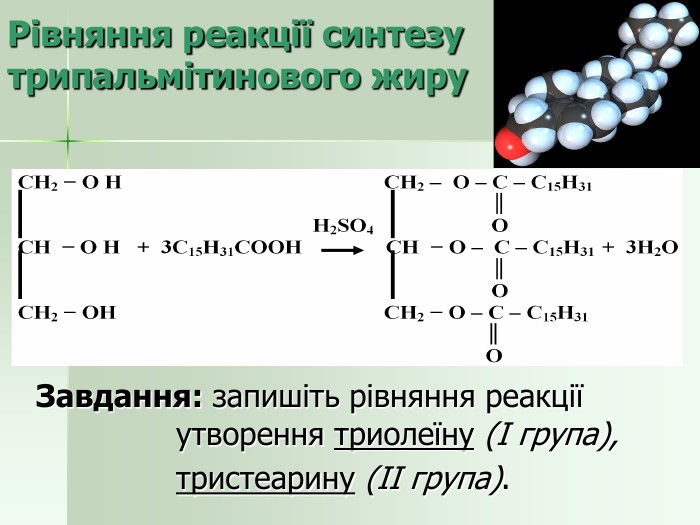
Добування жирів Штучний синтез: гліцерин + вища карбонова кислота (вперше здійснив французький вчений М. Бертло в 1854 р.) Вилучення із природної сировини Виробництво олії: Висушене насіння подрібнюють, нагрівають і пресують; Обробка насіння нагрітим летким розчинником, який потім видаляють перегонкою. Добування твердого жиру: витоплювання
Біологічна роль жирів Енергетична функція (при розщепленні 1 г жиру виділяється 39 кДж енергії) Захисна функція (захист внутрішніх органів від механічних пошкоджень) Терморегуляція (захист від переохолодження тварин) Джерело води (при окисленні 1 кг жиру виділяється 1,1 кг води) Розчинники вітамінів (А, D, Е)


про публікацію авторської розробки
Додати розробку