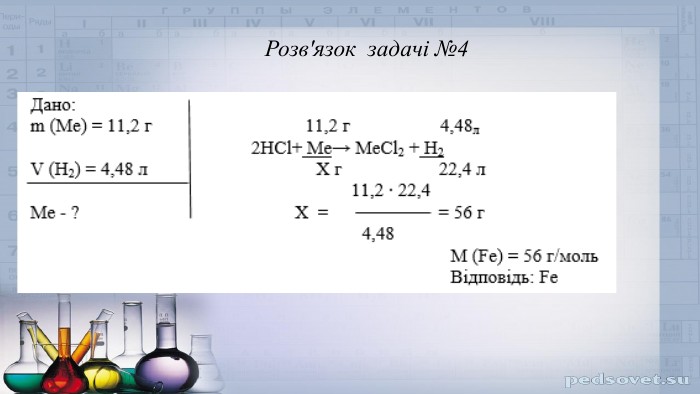
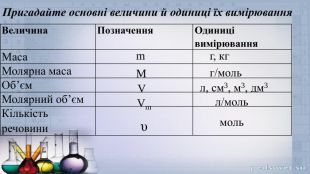
Презентаціядо уроку "Обчислення за хімічними рівняннями маси, кількості речовини, об’ємів газів (н.у.) за відомою масою, кількостю речовини, об’ємом реагентів чи продуктів реакції
Про матеріал
Презентація до уроку "Обчислення за хімічними рівняннями маси, кількості речовини, об’ємів газів (н.у.) за відомою масою, кількостю речовини, об’ємом реагентів чи продуктів реакції" Перегляд файлу
Зміст слайдів
pptx
Оцінка розробки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку