Розробка диференціованих завдань з теми "Основи МКТ"
ЗАКЛАД ПРОФЕСІЙНОЇ ОСВІТИ
« НІКОПОЛЬСКИЙ ЦЕНТР ПРОФЕСІЙНОЇ ОСВІТИ»
РОЗРОБКА ДИФЕРЕНЦІОВАНИХ ЗАВДАНЬ З ТЕМИ «ОСНОВИ МОЛЕКУЛЯРНО – КІНЕТИЧНОЇ ТЕОРІЇ.
ВІД ПРОСТОГО ДО СКЛАДНОГО
З УРАХУВАННЯМ РОЗУМОВИХ МОЖЛИВОСТЕЙ УЧНІВ»

2018 РІК
Розглянуто на засіданні Схвалено на засіданні
методичної комісії педагогічної ради
природничо – математичних протокол № 4 від 05.01.2018 дисциплін протокол №5 від 28.12.2017
Анотація
Збірник укладено відповідно до програми з фізики, підручників та методичних рекомендацій.
Збірник містить рівневі завдання з кожної теми «Основні положення молекулярно – кінетичної теорії» для контролю навчальних досягнень. Призначення збірника – відпрацювання практичних навичок учнів при підготовці поточного оцінювання, самостійних робіт, контрольних робіт та ЗНО.
Збірник розрахований на широке користування учнів і викладачів профосвіти, а також усіх, хто вивчає фізику.
Конспект до уроку
Основні положення молекулярно-кінетичної теорії будови речовини
Основні положення МКТ
Опорний конспект
Молекули
Розмір молекул Маса молекул
|
|
|
|
V d = V – об'єм шару олії, S – площа шару олії.
6000см
|
До конспекту учнів
Молекулярно-кінетична теорія
Вивчає властивості речовини, які визначаються її мікроскопічною будовою.
Макроскопічні Властивості тіл ![]() Мікроскопічні
Мікроскопічні
Розміри порівняні з розмірами
 Розміри достатньо великі молекул,
виявляється структура, для того, щоб не проявлялась несуцільність
речовини. несуцільність речовини.
Розміри достатньо великі молекул,
виявляється структура, для того, щоб не проявлялась несуцільність
речовини. несуцільність речовини.
Основні поняття молекулярно-кінетичної теорії.
В основі МКТ лежать три основних положення:
1. Речовина складається з частинок: молекул і атомів, іонів, між якими існують проміжки. 2. Атоми і молекули перебувають у безперервному хаотичному
русі(тепловому).
3. Атоми і молекули взаємодіють між собою.
КОНСПЕКТ ІЗОПРОЦЕСИ
Ізопроцеси — це процеси, за яких один із макроскопічних параметрів — температура, тиск або об'єм — залишаються сталими (від грец. «ізос» — рівний).
У середині XVII ст. два фізики англієць Р. Бойль і француз Е. Маріотт, експериментальне вивчивши ізотермічний процес в ідеальному газі даної маси, відкрили закон, який назвали, законом Бойля — Маріотта.
![]() Закон Бойля — Маріотта: за постійної температури тиск
даної маси ідеального газу обернено пропорційний його об'єму: T = const, р1 = V2 ; plVl = p2V2,
pV = const.
Закон Бойля — Маріотта: за постійної температури тиск
даної маси ідеального газу обернено пропорційний його об'єму: T = const, р1 = V2 ; plVl = p2V2,
pV = const.
р2 V1
Отже, за постійної температури добуток тиску даної маси ідеального газу і його об'єму є величина стала.


Ізобарний процес — це процес, який відбувається за постійного тиску (від грец. «барос» — тиск).
На початку XVIII ст. французький вчений Ж. Гей-Люссак експериментально відкрив закон, який встановлює залежність об'єму даної маси ідеального газу від його температури за постійного тиску.
Закон Гей -Люссака: за постійного тиску об'єм даної маси ідеального газу прямо пропорційний його абсолютній температурі:
![]() р = const, Т1 = V1 , V1 = V2 , V = const.
р = const, Т1 = V1 , V1 = V2 , V = const.
Т2 V2 Т1 T2 Т
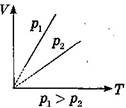
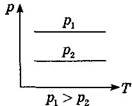
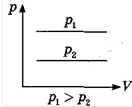
В середині XVIII ст. французький вчений Ж. Шарль експериментальне відкрив закон, який встановлює залежність тиску даної маси ідеального газу від його температури за постійного об'єму.
Закон Шарля: за постійного об'єму тиск даної маси ідеального газу прямо пропорційний його абсолютній температурі.
![]() V = const, Т1 = р1 , р1 = р2 р = const.
V = const, Т1 = р1 , р1 = р2 р = const.
Т2 р2 Т1 Т2 Т
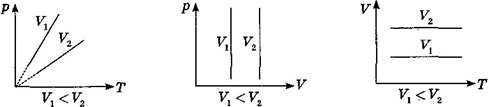
5. Межі застосування газових законів
Експериментальна перевірка з використання сучасних методів довела, що:
1) газові закони виконуються тільки для незмінної маси газу;
2) закони Бойля—Маріотта, Гей-Люссака та Шарля досить точно описують поводження реальних газів за невеликих тисків і високих температур; за високих тисків і низьких температур спостерігаються значні відхилення
РОЗВЯЗАННЯ ЗАДАЧ
Із газом деякої маси виконали замкнений процес, зображений на діаграмі в координатах р(Т). Накресліть цю діаграму в координатах p(V),V(T).
Примітка. Зручно заповнити таблицю, щоб зробити аналіз графіка.
|
Ділянка |
const |
Ізопроцеси |
Який закон відповідає процесу |
Як змінюється величини (↑ або ↓ ) |
|
1 – 2 |
Т |
ізотермічний |
Бойля – Маріотта |
↑ |
|
2 – 3 |
р |
ізобарний |
Гей – Люсака |
↑ |
|
3 – 1 |
V |
ізохорний |
Шарля |
↑ |
р V
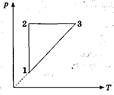 3
2 2 3
3
2 2 3
 1
1
V T
1
1
V T
ОПОРНІ КОНСПЕКТИ

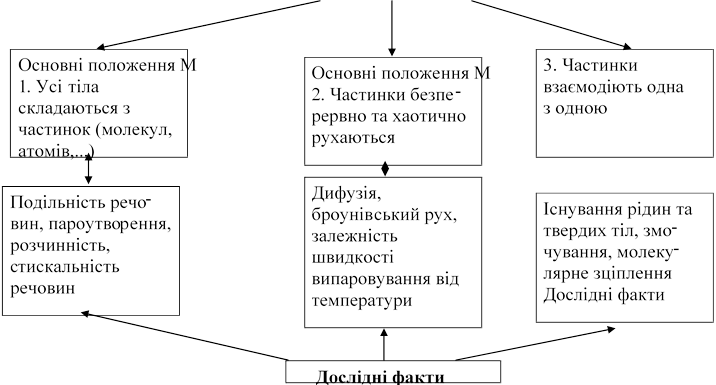
Основні положення МКТ і їх дослідне підтвердження
І. Усі тіла складаються з молекул, між якими існують проміжки. Гіпотеза Демокрит(греч.) – 2500 років тому
Непрямі докази Прямі докази подільність речовини фотографії окремих великих молекул (первокирпичик) визначення параметрів молекул(d,m,υ…) випаровування досвід Бриджмена
 або
деформації розчинність спирт
або
деформації розчинність спирт
об'єм тіла змінюється найдрібніша частка цієї речовини молекула - " маленька маса" лат. розміри молекули
10 000 000 молекула води
|
|
крапля олії на воді товщина шару = 0,000002 м |
в 1 см2 повітря ≈ 27∙1018 молекул |
Розмір і маса молекул досвід Ленгмюра :
 4 2
4 2
V r
![]() d = = 3 2 = 4 r32 d ~ 10-8
cм
d = = 3 2 = 4 r32 d ~ 10-8
cм
S R 3 R
різних однієї і тієї ж
різні ![]() МОЛЕКУЛИ
МОЛЕКУЛИ
![]() однакові речовин
речовини
однакові речовин
речовини
![]()
Молекула води АТОМИ Молекула водню
![]()
![]()
![]() О Атом кисню
О Атом кисню
Н Атом водню
Молекула кисню
![]()
ІІ. Частинки знаходяться у безперервному хаотичному русі
Броунівський рух 1827 р.
теорія Б.Р. – Ейнштейн 1905 р. дослідна перевірка – Перрен (фр)
ДИФУЗІЯ
явище, при якому відбувається взаємне проникнення молекул однієї речовини між молекулами іншого.
ПРИЧИНА ДИФУЗІЇ
молекули рухаються безперервно і безладно (Дифузія, броунівський рух, залежність швидкості випаровування від температури)
ДИФУЗІЯ ДИФУЗІЯ ДИФУЗІЯ В ТВЕРДИХ
В ГАЗАт В РІДИНАХ ТІЛАХ
(за декілька хвилин) (2 - 3 тижні) (за декілька років при

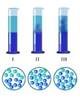
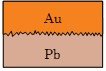 Вода при 20ОС)
Вода при 20ОС)
Мідний
купорос золото
свинець
Дифузія залежить від to (якщо to м )
БРОУНІВСЬКИЙ РУХ – тепловий рух мікроскопічних зважених частинок твердої речовини,які знаходяться в рідкому або газоподібному середовищі.
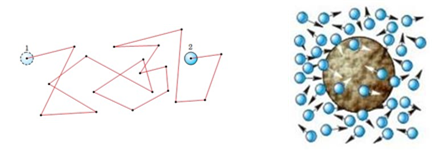
ІІІ. Частинки взаємодіють одна з одною
![]()
![]() Причина - електромагнітна
взаємодія і ядер молекул злипання свинцевих циліндриків
Причина - електромагнітна
взаємодія і ядер молекул злипання свинцевих циліндриків
(прилипання скла до води, опір до розтягування і стискування, наявність рідкого і твердого стану речовини, наявність рідкого і твердого стану речовини, мала стисливість твердих тіл і рідин, наявність сил пружності при зміні Vтіла, механічна міцність тіл
Моделі:
Газу Рідина Тверде тіло
r >> d r ~ d r ~ d
Хаотичний рух
прямолінійне коливання коливання
між зіткненнями + впорядкована безлад «перескоки» кристалічна безлад решітка
Маса молекул. Кількість речовини.
m0
Мr = - відносна молекулярна(атомна) маса.
![]()
12 0C
1а.о.м. = 1/12m12C=
1,66∙10-27 кг NA = ![]() 0,012кг/ моль ≈ 6∙1023моль-1
0,012кг/ моль ≈ 6∙1023моль-1
6 m0ru
N
Кількість речовини – ν = ![]() , ν
– ню NA
, ν
– ню NA
N – число молекул в даній речовині якщо N = NA, то ν = 1
NA– число Авогадро – число атомів в 12 г С NA– число атомів в молі
будь якої речовини
M –молярна маса(маса одного моля). M = Mr·10–3 кг/моль
|
m = m0 ∙ N М = m0 ∙ NA m N ν = M NA m N
= ν ∙ NА
= NА ∙ M |
m М = М – молярна маса [M] = кг/моль. m m M
М = m0 ∙ NA |
n – концентрація N n = 1 n=
А = Z + N; N= А - Z
|
Ідеальний газ
Ідеальний газ – модель
|
|
|
|
![]()
 мікро макро
Модель тиску
газу m0 m,М d0 p
мікро макро
Модель тиску
газу m0 m,М d0 p
m0r T
m0r2 N, n = ![]() N . удари молекул
N . удари молекул
V
r
|
р = |
 Основне рівняння МКТ: р(m0, , n)
Теплова рівновага а) р , якщо удари «частіше» n ,
Основне рівняння МКТ: р(m0, , n)
Теплова рівновага а) р , якщо удари «частіше» n ,
б) р , якщо удари «сильніше» m0r ,
r
т.як f ~ ( m0r ) час
р ~ nm0∙;
міра основна хар - ка
нагрітості теплової рівноваги
напрям мимовільного теплообміну
Термометр – … Шкали Цельсія
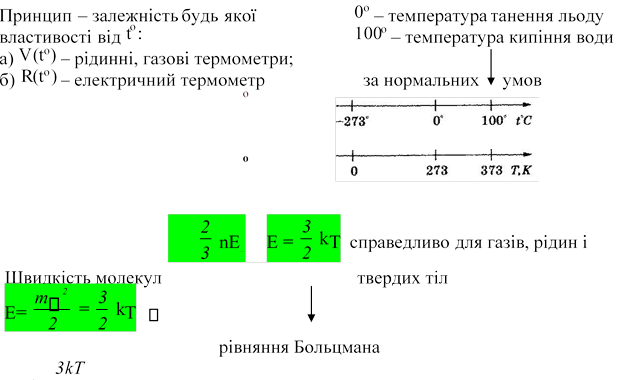 Т
– абсолютна температура К :
Т
– абсолютна температура К :
1) не залежить від речовини;
2) міра Wк
Т = t С + 273
k - стала Больцмана k =1,38 ∙1023 Дж/К р =
r
 швидше снаряду!
швидше снаряду!
m0
Газові закони
![]()
|
R = 8,31 |
 Epr
233 nEr
p = nkT= VN) kT pV=
Epr
233 nEr
p = nkT= VN) kT pV= ![]() Mm NA kT(NA k = R
– універсальна газова стала)
Mm NA kT(NA k = R
– універсальна газова стала)
![]() kT
kT
2
- рів. Менделєєва - Клапейрона
m
|
T1 T2 |
![]()
![]() P1V1 M RT1 - рівняння Клапейрона
P1V1 M RT1 - рівняння Клапейрона
m, M – const:
P2V2 m M RT2
Ізотермічний закон (Закон Бойля - Маріотта)
Ізопроцеси (від грец. «ізос» — рівний).
m = const а) T = const – ізотермічний (термостат)
M = const б) p = const – ізобарний (в циліндрі з рухливим поршнем) в) V = const – ізохорний (у закритій посудині)
Ізотермічний закон (закон Бойля - Маріотта) - розширення або стискування газу при T, m, M – const.
У циліндрі під поршнем - повітря в об'ємі V1 при p1 і Т1.
Повільним підняттям поршня на h збільшують обсяг до V2.
При Т2 = Т1 тиск р2 < p1.
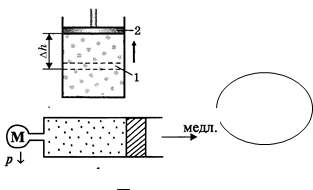 pV = m RT pV =
const або p1V1 = p2V2; (p
, V
).
pV = m RT pV =
const або p1V1 = p2V2; (p
, V
).
M
Добуток «p» даної маси газу на його р ~ 1 «V»постійно, якщо «Т»газу не міняється.
V
pV = const
Розширення
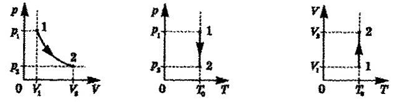
Стискання
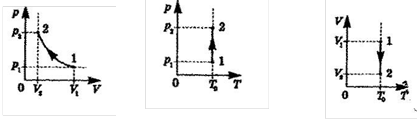
Ізобарний закон – греч. барос — тиск - простір(закон Гей – Люсака ) – розширення або стискування газу при р, m, M – const.
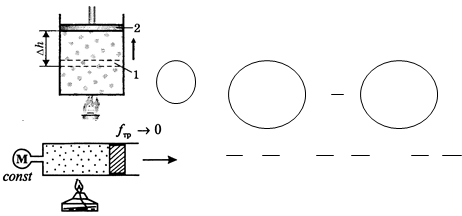 Розширення газу від V1 до
V2– результат нагрівання. В скільки
разів збільшується V в стільки разів зростає Т для
зберігання p.
Розширення газу від V1 до
V2– результат нагрівання. В скільки
разів збільшується V в стільки разів зростає Т для
зберігання p.
|
V = const. T |
|
р V= m R Т; V = m ;
M T Mр
V1 = V2 або V1 = Т1 або V2 =Т2 ;(V , Т ). або
T1 T2 V2 T2 V1 T1
«V» даної маси газу при постійному «р» пропорційний «Т».
V~ Т
Нагрівання (розширення)

 Охолодження(стискання)
Охолодження(стискання) 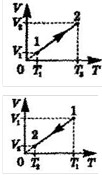
V = V0(1 + αt) – термічний коефіцієнт об'ємного розширення
Ізохорний закон – греч. chora - простір(закон Гей – Люссака ) – нагрівання або охолодження газу в замкнутому об'ємі, тобто при m, M, V = const.
В скільки разів збільшується Т, в стільки разів зростає р.
|
р const. T |
|
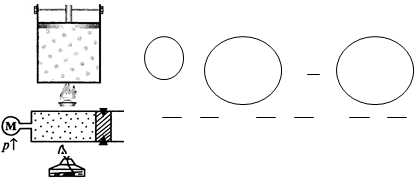 Р V =
Р V = m
R Т; р m M T = MV ;
або p1 = Т1 або p2 = Т2 або pR2 = p1 ; (p ; T )
p2 T2 p1 T1 Т2 Т1
«p» даної маси газу при остійному «V» пропорційний «Т».
р ~ Т
Нагрівання Охолодження
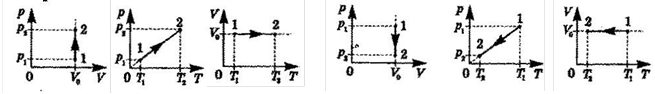
p = p0(1 + t) – термічний коефіцієнт тиску
Вчимося розв'язувати задачі
1. Основні положення молекулярно – кінетичної теорії будови речовини та її дослідне обґрунтування. Маса та розміри атомів та молекул.
Кількість речовини.
1. Магнію, Міді, Індію (в а.о.м).
Розв'язування Аг(Li) = 7-а.о.м; Аг(Мg) = 24 а.о.м; Аг(Сu) = 64 а.о.м; Аг(Іn) = 115 а.о.м.
2. Визначте відносну молекулярну масу молекули води (в а. о. м. та кг).
Розв'язування
З хімічної формули води Н2О, видно, що до її складу входять два атоми Гідрогену та один атом Оксигену. Молярну масу молекули води можна обчислити за формулою:
Мr(Н2O) = 2∙ Аг (Н) + Аг(O), Мr(Н2O) = 2∙1+16 = 2+16 =18 (а.о.м).
1а. о.м. =1,66∙10-27 кг.
Мr(Н2O) = 18∙1,66∙10-27 =29,88∙10-27 =30∙10-27 (кг). 3. Визначте молярну масу цукру С12Н22О11. Розв'язування
Визначимо відносну молекулярну масу молекули цукру С12Н22О11. Мr (С12Н22О11.) = 12∙ Аг (С) +22∙ Аг (Н) +11∙ Аг (O), Мг(С12Н22О11) = 12∙12 + 22∙1 + 11∙16 = 342 (а.о.м).
М= Мг ∙10-3, М = 342∙10-3 = 0,342 (кг/моль).
4. Скільки моль міститься в 4 г водню?


6. Яка маса молекули водню?
|
Дано: Н2
|
|
Розв’язання: За
формулою: т0 = NA стала Авогадро: N A = 6,02·1023 моль-1. М = М r · 10-3 кг/моль. М r = 2 а.о.м., 2103 -26 -25 М = 2·10-3 кг/моль. т0= 6 10 Відповідь: 3·10 -25 кг.
|
|
|
т0 -? |
7. Скільки молекул міститься у 210 г Нітрогену N2
|
Дано: N2 m = 210 г
|
СІ
0,21 кг
|
m Розв’язання:
N = M m Нітрогену. m0 = NA M З таблиці М = 28∙10-3(кг/моль), NА = 6, 02 ∙1023 моль-1
моль моль моль кг
N = = 0,045∙10 2810
Відповідь: N = 45 ∙ 1023.
|
|
N – ? |
8. Який об'єм займають 4 моль алюмінію?
|
Дано: Al v = 4 моль |
СІ
0,21 кг
|
Розв'язання. Об'єм алюмінію можна виразити через його масу й
густину: V = виразити через v кількість речовини й молярну
масу: т = ν·М. Звідси маємо: V = V = 2,7 10 кг моль Відповідь: V = 40см3.
|
|
V– ?
|
9. В посудині місткістю V = 12 л знаходиться газ, число N молекул якого рівно 1,44∙1018. Визначити концентрацію n молекул газу.
|
Дано: V = 12 л N = 1,44∙1018 |
СІ 12∙10-3 м3
|
n = ; n = = 0,12∙10 м V 1210 |
|
|
||
|
n – ? |
|
Виведемо розмірність шуканої фізичної величини: 1 n=
Відповідь: n = 1,2∙1020м-3.
|
10. На дзеркало площею 1м2 напилили 0,1 г срібла. Оцініть розмір (діаметр) атомів Арґентуму, якщо в дзеркальному покритті міститься 100 атомних шарів.
|
Дано: Аg S = 1м2 m = 0,1 г N = 100 |
СІ
10-4 кг |
Розв’язання: На дзеркало напилено шар срібла h = N ∙ d. Маса шару m = ρсрібла∙V, а об'єм V = S∙h. З таблиці: ρсрібла = 10500 кг/м3. Отже, m = ρсрібла∙ S∙h. m m m
Виведемо розмірність шуканої фізичної величини:
d = м м м кг d = 9,5∙ 10-3∙10-4∙10-4 = 10-10 м
Відповідь: d =10-10 м
|
Властивості газів. Ідеальний газ. Тиск газу.
1. Який тиск на стінки посудини чинить ідеальний газ із концентрацією 100 мільярдів молекул у кубічному міліметрі, якщо маса однієї молекули 3∙10-27 кг, ат середня квадратична швидкість руху молекул 1 км/с.
|
Дано: n = 1011мм-3 mr0 = 3∙10-27 кг = 1 км/с |
СІ 1020 м-3
103 м/с
|
Розв'язання: Основне рівняння МКТ : р = кг м2 кг м Н р=
|
|
р – ? |
2. Задача. Густина газу в балоні газопаливної електричної лампочки
ρ = 0,9 кг/м3. Коли лампочка світиться, тиск газу зростає з р1 = 8·104 Па до р2 = 1,1·105 Па. На скільки збільшилась при цьому середня швидкість молекул газу?
|
Дано: ρ = 0,9 кг/м3 р1 = 8·104Па р2 = 1,1·105Па |
= 1,8∙3∙104 = 5,4∙104 м/c. r2 r1 4 м/c. Відповідь: - =5,4∙10
|
|
r2 -r1- ? |
3. Визначити масу гідрогену, що знаходиться в балоні місткістю 20 л за тиску 830 кПа, якщо температура газу дорівнює 17 °С.
|
Дано: Н2 V= 20л р = 830 кПа t = 17оС |
Сі 20∙10-3м3 830∙103 Па 290 °К |
Розв’язання: Рівняння Мендєлєєва – Клапейрона: m рV = M М
– молярна маса: М = 2∙10-3кг/моль. m= RT Н м3 кг моль К фізичної
величини:m= = Н м 830 103 20 103 2103 33200 103
8,31290 24090,9 =13,8·10-3кг. Відповідь: m=13,8·10-3кг.
|
|
m- ? |
3. У балоні знаходиться газ під тиском 40 Па і за температури 27 °С. Коли з балона випустили3/5 газу, що містився в ньому, його температура знизилася до -33 °С. Визначити тиск газу, що залишився в посудині.
|
Дано: р1 = 40 МПа t1 = 300 °С t2 = -33 °С m2 = 2/5m1 |
Сі 40∙106Па 300°К 240°К
|
Розв’язання: m Рівняння Мендєлєєва – Клапейрона: рV = M m1 m2 р1 m1T1
р = 12,8МПа. Відповідь: р2 = 12,8 Па. |
|
р2 — ? |
4. Скільки молекул повітря виходить з кімнати об’ємом 120 м3, якщо температура підвищується від 15 до 25 °С? Атмосферний тиск дорівнює 105 Па.
|
Дано: V= 120м3 t1 = 15 °С t2 = 25 °С р = 105Па |
Сі 288°К 298°К
|
Розв’язання: Кількість молекул визначимо за формулою: N=
M де NA = 6·1023 моль-1 — число Авогадро; R = 8,31 Дж/(моль·К) — універсальна газова стала; m Рівняння Мендєлєєва – Клапейрона: рV = M M M 1 1 M T
RT R T Значення Δm підставляємо в рівняння (1): M T N= pV R MT1T2R T1T2R Виведемо розмірність шуканої фізичної величини: |
|
N — ? |
N=
![]() Па
м3 К 2моль К = Н2 м3 = 1; моль
К Дж
м Н м
Па
м3 К 2моль К = Н2 м3 = 1; моль
К Дж
м Н м
298 288 721030
N= 105∙120∙6·1023
![]() 298
299 8,31=713197,4 = 0,0001∙1030 = 1∙1026(молекул)
298
299 8,31=713197,4 = 0,0001∙1030 = 1∙1026(молекул)
Відповідь: N = 1·1026 молекул.
Газові закони
Перш ніж розв'язувати задачу на побудову графіка перебігу процесу в інших системах координат, слід з'ясувати:
1) що являє кожний етап процесу, тобто який ізопроцес він відображає;
2) як змінюються параметри газу на кожній ділянці — збільшуються чи зменшуються; ці закономірності мають зберігатися і на перебудованому 1. На рис. 1, а зображено дві ізобари для двох газів. Маси газів сталі.
Порівняйте тиски pl і р2
Розв'язання
У випадку фіксованої незмінної температури Т1 (рис. 1, б) маємо: V2 > V1, а отже, p2 < pl.
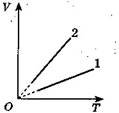
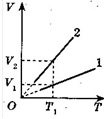
а б
Рис. 1
Відповідь: р2 < р1.
2. На рис. 2, а зображено дві ізотерми для двох газів. Маси газів сталі. Порівняйте температури Т1 і Т2.
Розв'язання
У випадку фіксованого незмінного об'єму V1 (рис. 2, б) маємо: р2 < р1, а отже, Т1 > Т2.

а б
Рис. 2
Відповідь: Т1 > Т2.
3. На рис. 3. а зображено дві ізохори для двох газів. Маси газів сталі. Порівняйте об'єми V1 і V 2. Розв'язання
У випадку фіксованої незмінної температури Т1 (рис. 3. б) маємо: р1 > р2, а отже, V1< V2.
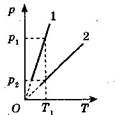
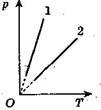 а
б
а
б
Рис. 3
Відповідь: V1 < V2.
4. На діаграмі V, Т (рис. 4, а) зображено точки, що відповідають трьом станам даної маси газу. Визначте, у якій точці тиск газу найбільший, а в якій найменший.
Розв'язання
У точці 1 (рис. 4, б) найменша температура і найбільший об'єм, отже, тиск найменший; у точці 3 висока температура і найменший об'єм, отже, тиск найбільший.

а б
Рис. 4
5. Побудуйте графік даного процесу (рис. 5, а) в координатах р, V і V, Т (m = const).
Розв'язання: Аналіз процесу:
1) 1-2: р = const, від точки 1 до точки 2 температура зменшується; 2) 2-3: V = const, від точки 2 до точки 3 тиск збільшується, температура
збільшується;
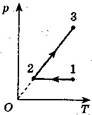
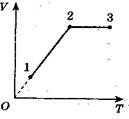
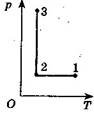 3) процес
незамкнений.
3) процес
незамкнений.
а б в
Рис. 5
6. Побудуйте графік даного процесу (рис. 6, а) в координатах р, Т і V, Т (m = const).
Розв'язання: Аналіз процесу:
1) 1 - 2: T = const, від точки 1 до точки 2 тиск зменшується, об'єм зростає;
2) 2 - 3: р = const, від точки 2 до точки 3 об'єм зменшується;
3) 3 - 4: V = const, тиск збільшується; 4) процес замкнений.
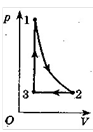
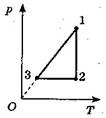
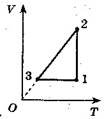
а б в
7. Газ міститься в закритому балоні за температури 294 К і тиску 810 кПа. За якої температури тиск газу дорівнюватиме 1,12 МПа?

![]()
8. Газ, який має температуру 306 К, охолоджується на 32 К. При цьому об'єм газу зменшується на 24 дм2. Який початковий об'єм даної маси газу? Тиск газу вважати сталим.

9. Під час ізотермічного стиснення об'єм газу зменшився на 5 л, а тиск збільшився в 3 рази. Яким був початковий об'єм газу?
|
Дано: Т = const ∆V = 5л V2 = V1 -∆V р2 = 3р1 |
СІ
∆V = 5∙10-3м3
|
Розв’язання: Т = const, процес ізотермічний
plVl = p2V2, plVl = 3p1(V1 -∆V ), Vl = 3(V1 -∆V ),
Vl = 3V1 -3∆V, 2 Vl =
3∆V, Vl [Vl] = м3 ,
Vl Відповідь: 7,5∙10-3 м3. |
 Збірник задач
Збірник задач
Розв'язати задачі.
1) Скориставшись таблицею Менделєєва, визначити відносну молекулярну масу кисню О2, метану СН4, сірководню Н2S 2) Визначити молярну масу (N2; CO2).
3) Яку масу мають 33∙1023 атомів Меркурію (Нg)?
4) Відомо, що маса 1,5∙1023 молекул газу становить 11 кг. Який це газ?
6) Налита у блюдце вода масою 50 г повністю випарувалась за 6 діб.
Скільки молекул у середньому випаровувалося з поверхні води за 1 с? 7) Яка кількість речовини міститься в 2,7 кг алюмінію?(0,8 кг кальцію) 8) Маса якої молекули більша — амоніаку (NH3) чи нітратної кислоти (HNO3)?
9) Визначити масу молекули аміаку(NH3)( mo =2,7∙10-26кг ) 10) Скільки молекул міститься в кисні масою 0,16 кг?(N = 3∙1024) 11) Який об’єм займають 100 моль ртуті? (V = 1,5∙10-3м3 = 1,5 л).
12) Знайти число атомів в алюмінію предмет масою 135 г. (N = 3∙1024). 13) Підрахувати число молекул, що містяться 1 кг вуглекислого газу; знайти масу однієї молекули. (N = 1,37∙1025 mо =7,3∙10-26кг).
14) Густина алмазу 3500 кг/м3. Який об’єм займуть 1022 атомів цієї речовини.
15) Скільки молекул у 10 г кисню?
16) В ампулі міститься водень (Н2). Визначте тиск газу, якщо його концентрація дорівнює 2 ∙1022 м -3, а середня квадратична швидкість руху молекул водню 500 м / с.
17) Чому дорівнює середня кінетична енергія поступального руху молекул ідеального газу за температурою 300 К?
18) У балоні міститься газ за температури 200 К. Концентрація газу становить 5∙1023м-3. Визначити тиск газу(k = 1, 38∙10-23 Дж/кг )
19) Середня кінетична енергія поступального руху молекул ідеального газу Дорівнює 5,6∙10-21Дж. Концентрація молекул становить 2,7 ∙1025 м -3. Який тиск створює такий газ на стінки посудини?
20) Газ, що займає об’єм 8 л, чинить тиск 100 кПа. Чому дорівнює його об’єм за тиску 160 кПа? Процес ізотермічний.
21) У балоні, об’єм якого дорівнює 200л, міститься газ під тиском 4,9 ∙105Па. Який об’єм займає газ за нормального атмосферного тиску?
(105Па, Т= const).
22) За температури 5оС тиск повітря у балоні дорівнює 1∙104 Па. За якої температури тиск у ньому дорівнює 2,6∙104 Па?
23) Балони електричних ламп заповнюють азотом за тиску 50,7 кПа і температури 17 °С . Яким стане тиск у ввімкненій лампі в момент, коли температура газу досягне 360 К?
24) Об'єм газу внаслідок ізобарного процесу зменшився на 10 л, а температура знизилась в 1,2 раза. Визначити початковий об'єм газу. 25) Сучасні вакуумні насоси дозволяють знизити тиск до 1,3·10-10 Па (10-12 мм рт. ст.). Скільки молекул газу міститься в 1см3 за певних тиску і температури 27 °С?
25) Порівняти тиск газу в точці 1- 2 (рис. 1). Маса газу стала.
26) Побудувати на рис. 2 графік даного процесу в координатах р, Т і V, Т (Т= const).
3) Побудувати на рис. 3 графік даного процесу в координатах р, Т і р, V (m = const).
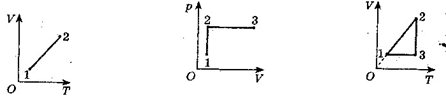 Рис.
1 Рис. 2 Рис. 3
Рис.
1 Рис. 2 Рис. 3
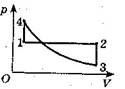
4. Виконати творче завдання. Побудувати на рис. 4 графік даного
процесу в координатах р, Т і V, Т
(m = const). Рис. 4

 Диктанти
Диктанти
Варіант 1
1. Які із зазначених властивостей належать гам? А. Мають власну форму. Б. Зберігають об'єм.
В. Не мають власної форми і постійного об'єму.
2. Як розташовані молекули газу?
А. Рухаючись безладно у всіх напрямках, майже не притягуються один до одного.
Б. Не розходяться на великі відстані. В. Розташовані в певному порядку.
3. У якому стані може перебувати ртуть? А. Тільки в рідкому.
Б. В рідкому, твердому, газоподібному.
В. Тільки в твердому.
4. Можна відкритий посудину заповнити газом на 40% його місткості? А. Так, можна. Б. Ні, не можна.
В. Певної відповіді немає.
5. Вода замерзла і перетворилася в лід. Змінилися при цьому самі молекули води?
А. Ні, не змінилися. Б. Так, змінилися. В. Певної відповіді немає.
Варіант 2
1. Які із зазначених властивостей належать рідинам? А. Мають власну форму і об'єм.
Б. Легко змінюють форму, але зберігають об'єм.
В. Не мають власної форми і постійного об'єму.
2. Як розташовані молекули у твердих тілах?
А. Рухаючись безладно у всіх напрямках, майже не притягуються один до одного.
Б. Не розходяться на великі відстані. В. Розташовані в певному (суворій) порядку.
3. У якому стані може перебувати чавун? А. Тільки в рідкому.
Б. В рідкому, твердому, газоподібному.
В. Тільки в твердому.
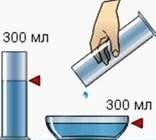
4. В пляшці перебуває вода об'ємом 0,2 л. Її переливають у колбу місткістю 0,5 літра. Чи зміниться об'єм води? А. Не зміниться. Б. Збільшиться.
В. Зменшиться.
5. У приміщеннях, де користуються медичним ефіром, зазвичай сильно їм пахне. В якому стані знаходиться ефір в приміщенні? А. Тільки в рідкому.
Б. В рідкому, твердому, газоподібному. В. Тільки в газоподібному.
 Фізичний диктант 2
Фізичний диктант 2
1. Закінчіть речення так, щоб отримати правильне твердження.
1) Відношення маси молекули до 1/12 частини маси атома
Карбону — це... (відносна молекулярна маса)
2) Кількість речовини, яка містить стільки ж молекул і атомів, скільки їх міститься в 12 г Карбону, називається... (молем) 3) Фізичний зміст молярної маси: молярна маса — це маса одного моля... (речовини)
4) Фізичний зміст сталої Авогадро: число Авогадро показує, що в одному молі речовини будь-якої речовини міститься... (молекул) 2. Запишіть формулу:
1) молярної маси;
2) об'єму моля речовини;
3) маси молекул (три формули);
4) кількості молекул в речовині (три формули).
Диктант перевіряється методом взаємоперевірки в парах.

Фізичний диктант 3
Варіант 1
1. Як називаються явища, обумовлені зміною температури тіла?
а) електричні, б) теплові, в) магнітні, г) механічні.
2. Розставити частинки в міру зростання складності їх будови.
1. Молекула. 2. Ядро атома. 3.Атом. 4.
Електрон. 3. Ким була створена теорія броунівського руху?
а) И.Ньютоном, б) М.В.Ломоносовим,
в) Т.Юнгом, г) А.Ейнштейном
4. Явище проникнення молекул однієї речовини в міжмолекулярний простір іншого називається ...
а) конвекція, б) деформація, в) дифракція, г) дифузія.
5 Процес зміни стану термодинамічної системи при постійному тиску називають ...
а) ізотермічним, б) адіабатних, в) ізобарним, г) ізохорним.
6. Перевести температуру в градусах Кельвіна в градуси Цельсія 274К
Варіант 2
1. Температура Т називається ...
а) нульовою, б) абсолютною (термодинамічною),
в) граничною, г) кінцевою.
2. Розташуйте ці твердження в тому порядку, в якому вони дані в вашому конспекті.
1. Молекули речовини взаємодіють один з одним.
2. Речовини складаються з молекул.
3. Молекули всіх тіл рухаються безперервно.
4. Всі молекули однієї речовини однакові.
3. Поставте прізвища вчених, які внесли вклад в розвиток МКТ, в тій послідовності, в якій ви знайомилися з їх відкриттями на уроках фізики.
1. А. Ейнштейн. 2. Р.Броун. 3. М.В. Ломоносов. 4. А. Авогадро.
4. Які речовини не зберігають ні форми, ні об'єму?
5. Газ, взаємодія між молекулами якого дуже малий, називається ...
а) реальним, б) абсолютним, в) ідеальним, г) вільним.
6.Перевесті температуру в градусах Цельсія в градуси Кельвіна 35С Доповніть речення
Диктант агрегатний стен
І. Тіла, у яких частинки розташовуються у певному порядку, називаються ...
ІІ. Відстань між двома молекулами менша розмірів молекул, якщо речовина знаходиться в ... агрегатному стані.
ІІІ. В умовах дії сили тяжіння речовина приймає форму судини, в якому воно знаходиться, так як тяжіння між молекулами не настільки велика, щоб зберегти свою форму. Це речовина знаходиться в .... агрегатному стані.
ІV. Рух частинок являє собою коливання біля певних точок до (положень рівноваги), частки не можуть піти від цих точок. Речовина знаходиться в ..... агрегатному стані.
V. Відстані між молекулами багато більше розмірів самих молекул, тому молекули слабо притягуються один до одного. Речовина знаходиться ... агрегатному стані.
VI. Молекули розташовані майже впритул один до одного, сили взаємодії утримують їх один біля одного. Речовина знаходиться в ...агрегатному стані. VІІ. Речовина заповнює весь наданий об'єм, якщо перебуває в ...агрегатному стані.
Відповіді до тесту. I-кристалічними; II-рідкому; III-рідкому; IV-твердому; Vгазоподібному; VI-твердому. VII-газоподібному.
1. Кількість речовини. Молярна маса
1. Доповніть речення в зошит запишіть пропозиції цілком:
• А. Щоб відміряти 1 моль речовини, потрібно взяти стільки грамів його, яка ____ або ________ маса речовини.
• Б. Встановлено, що 1 моль ________ речовини завжди містить ____________ число молекул. Це число дорівнює ________ .
• В. Таким чином, 1 моль води має масу _____ і містить _______ молекул Н2О.
• Р. Моль – це така кількість речовини, в якому міститься _____ молекул цієї речовини
• Д. Масу 1 моль речовини називають його ___________ і позначають буквою ____ . Відповідь.
А. Щоб відміряти 1 моль речовини, потрібно взяти стільки грамів його, яка відносна атомна (Ar) або відносна молекулярна (Mr) маса речовини.
Б. Встановлено, що 1 моль будь-якої речовини завжди містить однакове число молекул. Це число дорівнює 6 · 10 23 .
В. Таким чином, 1 моль води має масу 18 г і містить 6 · 10 23 молекул Н2О. Г. Моль – це така кількість речовини, в якій міститься 6 ·10 23 молекул цієї речовини
Д. Масу 1 моль речовини називають його молярною масою і позначають буквою М . Тест
Основи МКТ
1. Як залежить швидкість дифузії від температури для даного агрегатного стану речовини?
1. Не залежить
2. Збільшується з підвищенням температури
3. Зменшується з підвищенням температури
4. Відповідь неоднозначна
2. Як рухаються молекули в твердих тілах?
1. Молекули в основному обертаються
2. Молекули в основному коливаються біля положення рівноваги.
3. Молекули в основному рухаються поступально
4. Молекули рухаються рівномірно від зіткнення до зіткнення
3. В яких одиницях вимірюється кількість речовини?
1. кг 2. моль 3. кг / моль 4. см
4. Молярна маса М пов'язана з відносною молекулярною масою М чисельним співвідношенням:
1. M = Mr ∙10 -3 кг / моль 2. Mr = M ∙ 10-3 кг∙моль 3. M = Mr кг / моль
5. Яка величина характеризує стан термодинамічної рівноваги? 1. Тиск 2. Тиск і температура 3. Температура
4. Тиск, об’єм, температура 6. Який вираз відповідає формулі кількості речовини?
1. М/NA 2. m/m0 т 3. N/ Na 4. v ∙ Na
7. Броунівським рухом є …
1. Розчинення твердих речовин в рідині
2. Безладний рух дрібних пилинок в повітрі
3. Проникнення поживних речовин із ґрунту в корні рослин
8. Визначте значення маси молекули кисню
1. 1,79∙10-25 кг 2. 4,65∙10-26 кг 3. 5,31∙10 -27 кг 4. 3,3∙10 -26 кг
9.Яка природа молекулярних сил?
1. електромагнітна 2. гравітаційна 3. електромагнітна та гравітаційна
10. Яке явище найбільш переконливо доводить, що між молекулами існують сили тяжіння?
1. Газ тисне на стінки посудини 2. Дифузія
3. Існування рідин і твердих тіл 4. Броунівський рух
11. Вираз рV = m / М ∙ RT називають
1. Законом Бойля-Маріотта 2. Рівнянням Менделєєва-Клапейрона
3. Рівнянням Клапейрона 4. Законом Шарля
12. Одиниця термодинамічної температури в СІ
1. Кельвін т 2. Градуси Цельсія 3. Джоулі
Тест
Молекули і атоми
1) Виберіть правильне твердження:
1. Тільки вода і кисень складаються з молекул
2. Тільки тверді тіла складаються з молекул
3. Всі речовини складаються з молекул
4. Тільки повітря складається з молекул
2)Чи відрізняються молекули духів у флаконі від молекул духів, що літають в повітрі?
1.Відрізняються формою
2. Відрізняються запахом
3. Не відрізняються
4. Молекули в повітрі легше молекул у флаконі
3) Чим відрізняються молекули гарячої і холодної води?
1. Молекули холодної води менше молекул гарячої води
2. Молекули холодної води більше молекул гарячої води
3. Молекули однакові
4. Молекули холодної води кулясті, а молекули гарячої витягнуті 4) Чи можна побачити молекулу?
1. Так, під звичайним мікроскопом
2. Так, вони ледве помітні оком
3. Можливо отримати її знімок за допомогою електронного мікроскопа 4. Ні, оскільки вони занадто малі 5) Яке з тверджень вірно?
1. Молекули складаються з атомів
2. Атоми складаються з молекул
3. Молекула води складається з двох атомів кисню
4. Молекула кисню складається з двох молекул води
1. Основні положення МКТ.
Варіант 1
1. Явище дифузії в рідинах свідчить про те, що молекули рідин
1) коливаються біля своїх положень рівноваги
2) рухаються хаотично
3) притягуються один до одного 4) складаються з атомів
2. Дим являє собою частинки сажі, зважені в повітрі. Тверді частинки сажі довго не падають вниз тому, що
1) температура частинок сажі вища за температуру повітря
2) частки сажі здійснюють броунівський рух в повітрі
3) повітря виштовхує їх вгору відповідно до закону Архімеда
4) Земля не притягує настільки дрібні частинки
3. Частинки речовини беруть участь в безперервному тепловому хаотичному русі. Це положення молекулярно-кінетичної теорії будови речовини відноситься до
1) газам і твердих тіл
2) твердих тіл і рідин
3) газам і рідинам
4) газам, рідин і твердих тіл
4. Хаотичність теплового руху молекул газу призводить до того, що… 1) щільність речовини в газоподібному стані менше щільності цієї речовини в рідкому стані
2) газ набагато легше стиснути, ніж рідину
3) щільність газу однакова у всіх місцях займаного ним судини
4) при одночасному охолодженні і стисненні газ перетворюється в рідину
5. Частинки барвника в розчиннику довго не осідають на дно. Це можна пояснити ... 1) змочуванням
2) дифузією
3) силами взаємодії між молекулами
4) броунівським рухом
6. Яке явище доводить, що між молекулами діють сили відштовхування?
1) дифузія
2) броунівський рух
3) існування сил пружності
4) змочування
7. Дискретний характер будови речовини проявляється в процесі
1) поширення світла у вакуумі
2) дифузії в газах, рідинах і твердих тілах
3) тяжіння тіл Землею
4) зміна швидкості тіла під дією інших тіл
8. Дифузія в твердих тілах відбувається повільніше, ніж в газах так як
1) молекули твердого тіла взаємодіють слабкіше, ніж молекули газу
2) молекули твердого тіла менш рухливі, ніж молекули газу
3) молекули твердого тіла важче, ніж молекули газу. 4) молекули твердого тіла більше, ніж молекули газу
Варіант 2
1.Що є найбільш наочним досвідченим підтвердженням взаємодії між молекулами? Виберіть правильне твердження.
1)Броунівський рух.
2)Дифузія.
3) Виникнення сил пружності при деформації твердого тіла.
2. Що є найбільш наочним досвідченим підтвердженням руху молекул?
Виберіть правильне твердження.
1) Броунівський рух.
2) Спостереження за допомогою оптичного мікроскопа.
3 )Існування твердих тіл
3. Що є найбільш наочним досвідченим підтвердженням існування проміжків між молекулами? Виберіть правильне твердження.
1. Броунівський рух.
2. Спостереження за допомогою оптичного мікроскопа.
3. Дифузія.
4. Що є найбільш наочним досвідченим підтвердженням існування атомів і молекул? Виберіть правильне твердження.
1) Виникнення сил пружності при деформації твердого тіла.
2) Спостереження за допомогою оптичного мікроскопа.
3) Крапля олії розтікається на поверхні води так, що товщина масляної плівки має деякий мінімальне значення.
5.Які сили діють між нейтральними атомами? Виберіть правильне твердження.
1. Тільки сили тяжіння.
2. Тільки сили відштовхування
3. Сили тяжіння і відштовхування. Сили відштовхування більші, ніж сили тяжіння, на малих відстанях.
6.На поверхню води впала крапелька гасу і розтеклася, утворивши тонку плівку. За допомогою цього досвіду можна оцінити (виберіть правильне твердження) ...
1. …сили взаємодії молекул.
2. ... швидкість хаотичного руху молекул гасу.
3. ... середній розмір молекул гасу.
7. При спостереженні в мікроскоп за броунівський частинки можна помітити, що вони рухаються (виберіть правильне твердження) ...
1. ... в одному напрямку з однаковими по модулю швидкостями.
2. ... в різних напрямках з однаковими по модулю швидкостями.
3. ... в різних напрямках з різними по модулю швидкостями
8. За якою формулою можна обчислити кількість речовини в тілі? Виберіть правильну відповідь.
![]()
3. m0∙N
Температура-міра середньої кінетичної енергії
1.Абсолютная температура газу збільшилася в 2 рази. Середня кінетична енергія поступального руху молекул
1) збільшилася в 2 рази 3) збільшилася в 4 рази
2) зменшилася в 2 рази 4) зменшилася в 4 рази
2. Є два відкритих судини. В одному з них знаходиться киплячий ефір при температурі 35 ° С, а в іншому - вода при тій же температурі.
Відомо, що молярна маса ефіру більше молярної маси води.
Як співвідносяться значення середніх кінетичних енергій молекул цих речовин?
А. Е (ефіру)> Е (води) В. Е (ефіру) = Е (води)
Б. Е (ефіру) <Е (води) Г. можливі варіанти
3. Є два відкритих судини. В одному з них знаходиться киплячий ефір, а в іншому - вода. Відомо, що значення середніх кінетичних енергій молекул цих речовин однакові. Як співвідносяться абсолютні температури цих речовин?
1) можливі варіанти 3) Т (ефіру)> Т (води)
2) Т (ефіру) <Т (води) 4) Т (ефіру) = Т (води)
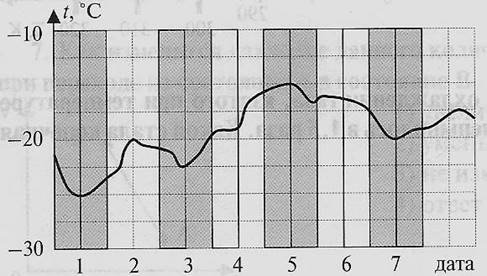
4. На малюнку представлений графік зміни температури повітря в січні. Користуючись графіком, визначте максимальне значення абсолютної температури 2 січня.
1) 293 К 3) 253 К
2) -20 ° С 4) -253 К
5. Воду нагріли на 27 ° С. Чому дорівнює зміна температури води за шкалою Кельвіна?
1) 27 К 3) – 27 К
2) 300 К 4) 256 К
Тест з фізики за темою "Будова речовини" Варіант 1. 1. В яких одиницях вимірюється молярна маса в СІ?
а) кг б) кг/моль в) моль г) г
2. Чому дорівнює стала Авогадро?
а) 6,022∙1023 моль б) 6,022∙1022 моль
в) 6,022∙1023 моль-1 г) 6,022∙10-22 моль-1
3 Чому дорівнює зарядове число атому натрію 11 23Na?
а) 11 б) 12 с) 23 д) 34
4. Чому дорівнює заряд усіх електронів в атомі неону 10 20Ne?
а) -1,6∙10-18 Кл б) -1,6∙10-20 Кл
в) 1,6∙10-19 Кл г) -1,6∙1018 Кл
5. Знайдіть правильне опис складу атома натрію 11 23Na
а) 11 електронів 11 протонів 23 нейтрона
б) 11 електронів 11 нейтронів 23 протона
в) 11 електронів 11 протонів 12 нейтронів
г) 11 електронів 11 нейтронів 12 протонів
6. Атом втратив один електрон. Як називається залишилася частинка?
а) позитивний іон б) негативний іон в) ізотоп
7. Ізотопи атома відрізняються один від одного ...
а) числом електронів б) числом протонів
в) числом нейтронів г) зарядом ядра
8. Чому дорівнює відносна молекулярна маса C3Н8 ?
а) 44 г/моль б) 44 г в) 44 кг/моль г) 44
9. В посудині 6∙1023 молекул гелію 2 4Не. Чому дорівнює кількість речовини?
а) 0,1 моль б) 1 моль в) 2 моль г) 10 моль
10. В посудині міститься 2 г водню 1 1Н. Чому дорівнює кількість речовини?
а) 1 моль б) 2 моль в) 0,001 моль г) 0,002 моль
11. Чому дорівнює число молекул в 10 г водню? Відповідь округлити до цілих.
а) 6∙1024 б) 3∙1024 в) 2∙1024 г) 1024
12. * (бонус) На виріб, поверхня якого 20 см2, нанесений шар срібла завтовшки 1 мкм. Скільки атомів срібла міститься в покритті?
а) 1,2∙1020 б) 2∙1020 в) 4,7∙1021 г) 9,4 ∙10 21
Тест з фізики за темою "Будова речовини" Варіант 2.
1. В яких одиницях вимірюється кількість речовини в СІ?
а) кг б) кг/моль в) моль г) г/моль
2. Знайдіть невірну формулу:
а) ν = N/Na б) m = ν Mr в) N= mNa/M г) M=ma Na
3. Чому дорівнює масове число атома алюмінію 13 27Al?
а) 13 б) 14 в) 27 г) 40
4. Чому дорівнює заряд ядра в атомі неону 2 4Нe?
а) + е б) + 2е в) + 3е г) + 4 е
27Al 5. Знайдіть правильний опис складу атома алюмінію 13
а) 13 електронів 13 протонів 27 нейтрона
б) 13 електронів 13 нейтронів 27 протона
в) 13 електронів 13 протонів 14 нейтронів
г) 13 електронів 14 нейтронів 13 протонів
6. Атом становится отрицательным ионом, если …
а) потеряет один или несколько электронов
б) приобретет один или несколько электронов
в) потеряет или приобретет один или несколько протонов
г) потеряет один или несколько нейтронов
д) приобретет один или несколько нейтронов
7. У водню є ізотопи 11Н (протій), 21 Н (дейтерій), 31Н (тритій). У якого ізотопу найбільше число протонів в атомі?
а) у протію б) у дейтерію в) у тритію
г) число протонів у всіх ізотопів однакове2,3∙10-10 м, 8. Чому дорівнює молярна маса С2 Н4 ?
а) 28 г/моль б) 28 г в) 28 кг г) 28 кг/моль
9. Чому дорівнює маса одного благаючи водню?
а) 1 г б) 2 г в) 0,001 г г) 6,022∙1023 г
10. Масса одной молекулы хлора 6*10-26 кг. Чему равна масса 1000 молекул хлора?
а) 6∙10 -29 кг б) 6∙10-23 кг
в) 213∙10-23 кг г) 2,13 ∙1027 кг
11. У посудині знаходиться гелій, кількість речовини якого 2 моль.
Скільки приблизно атомів гелію в посудині? Відповідь округлите до цілих
а) 10 23 б) 2∙1023 с) 6∙1023 д) 12∙1023
12. * (бонус) Вважаючи, що діаметр молекули водню становить близько 2,3∙10-10 м, підрахуйте, якої довжини вийшла б нитка, якби всі молекули, що містяться в 1 мг цього газу, були розташовані в один ряд впритул один до одного. Відповідь округлите до цілих
а)7∙10 10 м б) 9 ∙10 10 м в) 5∙1011 м г) 2∙1012 м
Тест
Основне рівняння МКТ
1. Тиск газу на стінку посудини обумовлено
А. тяжінням молекул один до одного
Б. зіткненнями молекул зі стінками судин
В. зіткненням молекул газу між собою
Г. проникненням молекул крізь стінки судини
2. Як змінилося тиск ідеального газу, якщо в даному об’ємі швидкість кожної молекули газу збільшилася в 2 рази, а концентрація молекул залишилася без зміни?
А. збільшилася в 2 рази
Б. збільшилася в 4 рази
В. зменшилася в 2 рази
Г. зменшилася в 4 рази
3. При підвищенні температури ідеального газу в запаяному посудині його тиск збільшується. Це пояснюється тим, що з ростом температури ...
А. збільшуються розміри молекул газу
Б. збільшується енергія руху молекул газу
В. збільшується потенційна енергія молекул газу
Г. збільшується хаотичність руху молекул газу
4. Як зміниться концентрація молекул газу при зменшенні об’єму посудини в 2 рази?
А. збільшиться в 2 рази
Б. зменшиться в 2 рази В. не зміниться
Г. зменшиться в 4 рази
5. При зменшенні температури середня кінетична енергія молекул
А. збільшиться
Б. зменшиться
В. не зміниться
Г. іноді збільшиться, іноді зменшиться
6. Яке твердження неправильне? При незмінних умовах
А. тиск газу постійний
Б. швидкості всіх молекул однакові
В. внутрішня енергія газу постійна
Г. температура газу постійна
7. У посудині водень. Як зміниться тиск газу, якщо водень замінити киснем так, що кількість молекул і температура залишаться незмінними? А. збільшиться 4 рази
Б. зменшиться в 16 разів
В. не зміниться
Г. збільшиться в 16 разів
Правильні відповіді: 1 - Б, 2 - Б, 3 - Б, 4 - А, 5 - Б, 6 - Б, 7 - Г
Тест по теме "Основы МКТ" Варіант 1.
1. Одиниця термодинамічної температури в СІ
а) градуси Цельсія б) Кельвіна в) Джоулі г) градуси Фаренгейта 2. Чому дорівнює значення постійної Больцмана?
а) 1,83 ∙ 1023 Дж / К б) 1,38 ∙10-23 Дж / кг в) 8,31 ∙10-23 Дж / кг
г) 1,38∙1023 Дж / кг д) 1,83 ∙ 10-23 Дж / кг є) 8,31 Дж / кг
3. Виразіть 50 градусів Цельсія в Кельвіна
а) 50 К б) -50 К в) 323 К г) -223 К
4. У якого з газів (водень, вуглець, азот, кисень) середня квадратична швидкість руху молекул найбільша?
а) водень б) вуглець в) азот г) кисень
5. При якій температурі має припинитися рух молекул?
а) 0 градусів Цельсія б) -100 градусів Цельсія
в) 0 До д) - 100 К г) -273 К
д) такої температури не існує
6. Яка з констант дає значення концентрації молекул ідеального газу при нормальних умовах?
а) постійна Больцмана б) постійна Лошмідта
в) постійна Авогадро г) молярна газова стала
7. Знайдіть невірну формулу:
а) n = p / (kT) б) T = p / (kn) в) E = 3kT / 2 г) ν = pV / (RT)
д) всі вірні
8. Як зміниться тиск ідеального газу при збільшенні температури газу в 3 рази?
а) збільшиться в 3 рази б) збільшиться в √ 3 рази в) не зміниться
г) зменшиться в 3 рази д) зменшиться в √3 рази
9. Як зміниться тиск ідеального газу при збільшенні середньої квадратичної швидкості молекул в 2 рази?
а) збільшиться в 2 рази б) зменшиться в 2 рази
в) не зміниться г) збільшиться в 4 рази е) зменшиться в 4 рази
д) збільшиться в √ 2 рази є) зменшиться в √ 2 рази.
10. Знайдіть тиск ідеального газу при температурі 23 градуси Цельсія і концентрації 2 ∙ 1023 м-3
а) 63,5 Па б) 382,3 Па в) 828 Па г) 4986 Па
Варіант 2.
1. Единица концентрации в СИ
а) м3 б) м-3 в) кг/м3 г) м-1
2. Чему равно значение постоянной Авогадро?
а) 6,022 ∙ 1023 моль-1 б) 6,022∙10-23 моль-1 в) 8,31∙ 10-23 Дж/кг
г) 1,38∙ 1023 моль д) 1,38∙ 10-23 Дж/кг є) 8,31 Дж/(К моль)
3. Выразите 30 Кельвин в градусах Цельсия
а) 303 б) 243 в) -243 г) 30
4. У какого из газов ( водород, азот, аргон, неон) средняя квадратичная скорость движения молекул наименьшая?
а) водень б) азот в) аргон г) неон
5.Какие из величин не могут быть отрицательными?
(Может быть несколько правильных ответов)
а) средняя кинетическая энергия молекул
б) термодинамическая температура
в) давление идеального газа
г) температура по Цельсию
6. Какая из констант связывает температуру в энергетических единицах
(Дж) и Кельвинах?
а) стала Больцмана б) стала Лошмідта
в) стала Авогадро г) молярна газова стала
7. Найдите неверную формулу:
а) р = ν RT/(MV) б) R = k Na в) p = n k T г) p = 3 n E / 2
8. Как изменится давление идеального газа при увеличении объема в 3 раза при постоянной температуре?
а) збільшиться у 3 рази б) збільшиться у √ 3 рази в) не зміниться
г) зменшиться у 3 рази д) зменшиться у √3 рази
9. Как изменилась средняя квадратичная скорость молекул, если давление идеального газа уменьшилось в 3 раза?
а) зменшиться у √3 рази б) зменшиться у 3 рази
в) не зміниться г) збільшиться у 3 рази д) збільшиться у √ 3 рази
є) збільшиться у 9 раз з) зменшиться у 9 раз.
10. В сосуде объемом 4 м3 находится газ под давлением 831 Па при температуре 400 К. Чему равно количество вещества данного газа?
а) 0,01 моль б) 1 моль в) 1 кг г) 100 моль
Тест «Ізопроцеси в газах»
1. Яке з наведених нижче рівнянь відповідає ізобаричному процесу в ідеальному газі? Виберіть правильне твердження.
![]()
![]() р1 = р2 Б) р1 = Т1 В) р1V1
= р2V2
р1 = р2 Б) р1 = Т1 В) р1V1
= р2V2
А)
Т1 Т2 р2 Т2
2. Яке з наведених нижче рівнянь відповідає ізотермічному процесу в ідеальному газі? Виберіть правильне твердження.
![]()
![]()
![]() р1 =V2 Б) р1 = Т1 В) V1 = Т1
р1 =V2 Б) р1 = Т1 В) V1 = Т1
А) р2 V1 р2 Т2 V2 Т2
3. Яка з наведених нижче рівнянь відповідає Ізобаричний процесу в ідеальному газі? Виберіть правильне твердження.
А) V1 Т2 = V2 Т 1 Б) р 1 Т2= р 2 Т1 В) р1V2 = р2V1
4. При здійсненні, якого ізопроцесами збільшення абсолютної температури ідеального газу в 2 рази призводить до збільшення тиску газу теж в 2 рази?
Виберіть правильну відповідь.
А. ізобарного . Б. ізохорного В. ізотермічного 5. При здійсненні, якого ізопроцесів збільшення абсолютної температури ідеального газу в 2 рази призводить до збільшення об’єму газу теж в 2 рази? Виберіть правильну відповідь.
А. ізобарного . Б. ізохорного В. ізотермічного
6. При здійсненні, якого ізопроцесів збільшення об’єму ідеального газу в 2 рази призводить до зменшення тиску газу теж в 2 рази?
Виберіть правильну відповідь.
А. ізобарного . Б. ізохорного В. ізотермічного
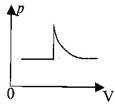
7. Ідеальний газ спочатку нагрівався при постійному тиску, потім його тиск збільшувалася при постійному обсязі, потім при постійній температурі тиск газу зменшувалася до початкового значення. Який з графіків в осяx p-V відповідає цим змінам стану газу?
а) б) в)
![]()
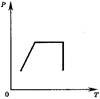
8.Ідеальний газ спочатку нагрівався при постійному тиску, потім його тиск збільшувалася при постійному обсязі, потім при постійній температурі тиск газу зменшилася до початкового значення. Який з графіків в координатах р-Т відповідає цим змінам стану газу?
а) б) в)
![]()
Індивідуальна робота щодо заповнення таблиць. Взаємоперевірка по готовій таблиці на дошці.
1. Виберіть зі списку речовини, що знаходяться
у твердому стані у рідкому стані
в газоподібному стані і запишіть їх у таблицю
Залізо, кисень, лід, бензин, вуглекислий газ, дерево, вода, пластмаса, водяна пара, спирт, скло, нафту.
|
Тверді тіла |
Рідина |
Гази |
|
|
|
|
2. Заповніть таблицю
|
Величина |
Буква |
Одиниця вим. |
|
|
|
Па |
|
маса однієї частинки |
|
|
|
|
n |
|
|
|
|
кг/м3 |
|
швидкість молекул |
|
|
|
|
k |
|
|
|
|
К |
|
число Авогадро |
|
|
|
|
R |
|
|
Величина |
Буква |
Одиниця вим. |
|
тиск |
р |
Па |
|
маса однієї частинки |
m0 |
кг |
|
концентрація молекул |
n |
м-3 |
|
густина |
|
кг/м3 |
|
швидкість молекул |
|
м/с |
|
стала Больцмана |
k |
1,38∙10-23Дж/К |
|
температура |
Т |
К |
|
число Авогадро |
NA |
6,022∙1023 моль-1 |
|
універсальна газова стала |
R |
8,31 Дж/(кг∙К) |
1. Заповніть таблицю, вказавши відмінність в розташуванні і характері русі частини в різних агрегатних станах речовини
|
Питання |
|
Агрегатний стан |
|
|
Газ |
Рідина |
Тверде тіло |
|
|
1.Яка відстань між частками (порівняно з розмірами самих часток) |
|
|
|
|
2.Що можна сказати про взаємодію самих часток. |
|
|
|
|
3. Який порядок розташування часток |
|
|
|
|
4. Який порядок руху часток |
|
|
|
|
1.Яка відстань між частками (порівняно з розмірами самих часток) |
Відстані між молекулами значно більше розмірів молекул |
Порядку не існує, відстань між молекулами дорівнює розміру молекул |
Молекули розташовані в певному порядку, впритул один до одного |
|
2.Що можна сказати про взаємодію самих часток. |
Слабке притягання, відштовхування під час зіткнень. Сили притягання між молекулами відсутні |
Трохи слабша. Сили притягання між молекулами слабкі |
Сильна. Сили притягання між молекулами дуже великі |
|
3. Який порядок розташування часток |
Відстані набагато більші від розміру молекул |
Відстані спів мірні з розмірами молекул, порядок відсутній |
Утворюють кристалічну решітку |
|
4. Який порядок руху часток |
Літають по всьому об’єму, інколи зазнають зіткнень |
Коливання, інколи «стрибки» |
Коливання |
|
№ |
Назва |
Позначення |
Одиниці вимірювання |
|
1 |
Температура |
|
|
|
2 |
Тиск |
|
|
|
3 |
Теплота |
|
|
|
4 |
Об’єм |
|
|
|
5 |
Маса |
|
|
|
6 |
Маса атома |
|
|
|
7 |
Відносна атомна маса |
|
|
|
8 |
Відносна молекулярна маса |
|
|
|
9 |
Кількість речовини |
|
|
|
10 |
Молярна маса |
|
|
|
11 |
Число Авогадро |
|
|
|
№ |
Назва |
Позначення |
Одиниці вимірювання |
|
1 |
Температура |
t0 |
градус |
|
2 |
Тиск |
р |
Па |
|
3 |
Теплота |
Q |
Дж |
|
4 |
Об’єм |
V |
м 3 |
|
5 |
Маса |
m |
кг |
|
6 |
Маса атома |
ma |
а.е.м. |
|
7 |
Відносна атомна маса |
Ar |
1 |
|
8 |
Відносна молекулярна маса |
Mr |
1 |
|
9 |
Кількість речовини |
ν |
моль |
|
10 |
Молярна маса |
M |
кг/моль |
|
11 |
Число Авогадро |
NA |
6,02 . 10 23 моль-1 |
ФОРМУЛИ
|
№ з/п |
Величина |
Позначення |
Одиниці вимірювання |
Формула |
|
1 |
Маса молекули |
m0 |
кг |
m m 0 = N |
|
2 |
Відносна молекулярна маса |
Mr |
а.о.м |
по таблиці Менделєєва |
|
3 |
Кількість речовини |
ν |
моль |
m ν = M N ν = NA |
|
4 |
Маса речовини |
m |
кг |
m = m 0·N |
|
5 |
Об’єм |
V |
м3 |
m V = |
|
6 |
Кількість молекул |
N |
молекул |
N = n·V; m N = |
|
7 |
Молярна маса |
M |
кг / моль |
M = Mr·10-3 |
|
8 |
Стала Авогадро |
NA |
моль-1 |
6·10 23 моль-1 |
|
9 |
Концентрація молекул |
n |
м -3 |
N n = V |
|
№ з/п |
Величина |
Позначення |
Одиниці вимірювання |
Формула |
|
1 |
Маса молекули |
|
|
|
|
2 |
Відносна молекулярна маса |
|
|
|
|
3 |
Кількість речовини |
|
|
|
|
4 |
Маса речовини |
|
|
|
|
5 |
Об’єм |
|
|
|
|
6 |
Кількість молекул |
|
|
|
|
7 |
Молярна маса |
|
|
|
|
8 |
Стала Авогадро |
|
|
|
|
9 |
Концентрація молекул |
|
|
|
|
№ з/п |
Величина |
Позначення |
Одиниці вимірюв. |
|
1 |
Тиск |
р |
Па |
|
2 |
Кількість речовини |
ν |
моль |
|
4 |
Маса речовини |
m |
кг |
|
5 |
Об’єм |
V |
м3 |
|
6 |
Кількість молекул |
N |
молекул |
|
7 |
Відносна молекулярна маса |
Mr |
а.о.м |
|
8 |
Стала Авогадро |
NA |
6∙1023моль-1 |
|
9 |
Універсальна стала |
R |
Дж
|
|
|
Температура |
T |
K |
|
Молярна маса |
M |
кг / моль |
|
|
Енергія |
Ек |
Дж |
|
|
13 |
Стала Больцмана |
k |
1,38∙10-23 Дж/К |
|
14 |
Маса молекули |
m0 |
кг |
|
15 |
Концентрація молекул |
n |
м -3 |
|
№ з/п |
Величина |
Позначення |
Одиниці вимірюв. |
|
1 |
Тиск |
|
|
|
2 |
Кількість речовини |
|
|
|
4 |
Маса речовини |
|
|
|
5 |
Об’єм |
|
|
|
6 |
Кількість молекул |
|
|
|
7 |
Відносна молекулярна маса |
|
|
|
8 |
Стала Авогадро |
|
|
|
9 |
Універсальна стала |
|
|
|
10 |
Температура |
|
|
|
11 |
Молярна маса |
|
|
|
12 |
Енергія |
|
|
|
13 |
Стала Больцмана |
|
|
|
14 |
Маса молекули |
|
|
|
15 |
Концентрація молекул |
|
|
|
№ з/п |
Величина |
Позначення |
Одиниці вимірюв. |
Формула |
|
1 |
Тиск (Основне рівняння МКТ) |
р |
Па |
р |
|
2 |
Кількість речовини |
ν |
моль |
m ν = M N ν = NA |
|
3 |
Залежність тиску від середньої кинетичної енергії |
р |
Па |
2
3 |
|
4 |
Маса речовини |
m |
кг |
m = m 0·N |
|
5 |
Об’єм |
V |
м3 |
V = |
|
6 |
Кількість молекул |
N |
молекул |
N = n·V; N = |
|
7 |
Залежність тиску від густини |
р |
Па |
p |
|
8 |
Стала Авогадро |
NA |
моль-1 |
6·10 23 моль-1 |
|
9 |
Універсальна стала |
R |
Дж
|
8,31∙10-23 |
|
10 |
Температура |
T |
K |
T = t0 + 2730 |
|
11 |
Молярна маса |
M |
кг / моль |
M = Mr·10-3 |
|
12 |
Залежність тиску від температури |
p |
Па |
pT |
|
13 |
Маса молекули |
m0 |
кг |
m 0
= N |
|
14 |
Рівняння стану ідеального стану |
- |
- |
m PV |
|
15 |
Концентрація молекул |
n |
м -3 |
N n = V |
|
16 |
Рівняння Клапейрона |
- |
- |
T1 T2 |
|
17 |
Закон Бойля Маріотта |
- |
- |
P1 V2 V 1 P2 |
|
18 |
Закон Шарля |
- |
- |
P1 T1 V2 P2 |
|
19 |
Закон Гей - Люссака |
- |
- |
V1 T1 T2 V2 |
|
№ з/п |
Величина |
Позначення |
Одиниці вимірюв. |
Формула |
|
1 |
Тиск (Основне рівняння МКТ) |
|
|
|
|
2 |
Кількість речовини |
|
|
|
|
3 |
Залежність тиску від середньої кинетичної енергії |
|
|
|
|
4 |
Маса речовини |
|
|
|
|
5 |
Об’єм |
|
|
|
|
6 |
Кількість молекул |
|
|
|
|
7 |
Залежність тиску від густини |
|
|
|
|
8 |
Стала Авогадро |
|
|
|
|
9 |
Універсальна стала |
|
|
|
|
10 |
Температура |
|
|
|
|
11 |
Молярна маса |
|
|
|
|
12 |
Залежність тиску від температури |
|
|
|
|
13 |
Маса молекули |
|
|
|
|
14 |
Рівняння стану ідеального стану |
|
|
|
|
15 |
Концентрація молекул |
|
|
|
|
16 |
Рівняння Клапейрона |
|
|
|
|
17 |
Закон Бойля Маріотта |
|
|
|
|
18 |
Закон Шарля |
|
|
|
|
19 |
Закон Гей - Люссака |
|
|
|
Доміно Перед вами - доміно, Чи не складено воно. З цифри першої починаємо, Фрази швидко складаємо.
Пропозиції - ланцюжком,
А закінчимо жирною крапкою
|
1 |
При однаковій температурі розміри проміжків між молекулами в газах і рідинах... |
|
...відрізняються. Проміжки між молекулами газу більше, ніж між молекулами рідини. |
При однаковій температурі розміри проміжків між молекулами в газах і твердих тілах... |
|
...відрізняються. Проміжки між молекулами газу більше, ніж між молекулами твердого тіла. |
При однаковій температурі розміри проміжків між молекулами в рідинах і твердих тілах... |
|
...відрізняються. Проміжки між молекулами рідини більше, ніж між молекулами твердого тіла. |
У твердих тілах тяжіння між молекулами дуже велике, .... |
|
...тому що дуже малі проміжки між молекулами. |
У газах тяжіння між молекулами газу дуже мало, ... |
|
...тому що великі проміжки між молекулами. |
Швидкість руху молекул льоду в порівнянні з молекулами води... |
|
...менше. |
Швидкість руху молекул водяної пари в порівнянні з молекулами води... |
|
…більше. |
Перехід з рідкого стану речовини в твердий стан здійснюється.... |
|
... шляхом охолодження. |
Перехід з твердого стану речовини в рідкий стан здійснюється.... |
|
... шляхом нагрівання. |
|
|
Початок
|
Універсальна газова стала |
|
Дж/(кг∙К) |
Маса |
|
кг
|
Швидкість |
|
м/с |
Молярна маса |
|
|
|
||||||||||||||||||||
|
|
|||||||||||||||||||||
|
|
|||||||||||||||||||||
|
|
|||||||||||||||||||||
|
|
|
Дж/К |
Тиск
|
|
Па |
Кінець |
|
|
|
|||||||||||||||||||||
|
|
||||||||||||||||||||||
|
|
||||||||||||||||||||||
|
|
||||||||||||||||||||||
|
|
|
|
|
|||||||||||||||||||||||||||||||||
|
|
||||||||||||||||||||||||||||||||||
|
|
||||||||||||||||||||||||||||||||||
Газові закони
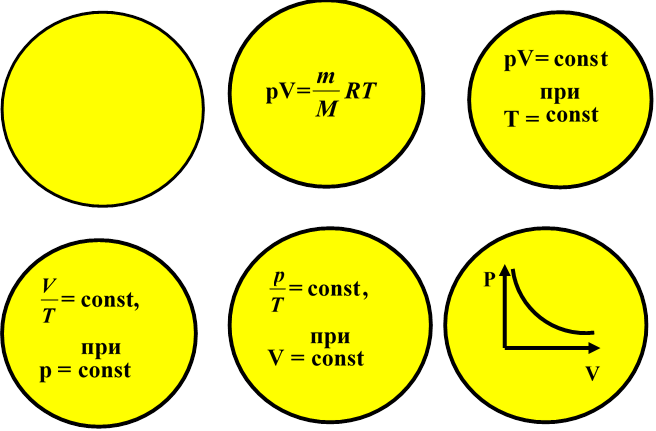
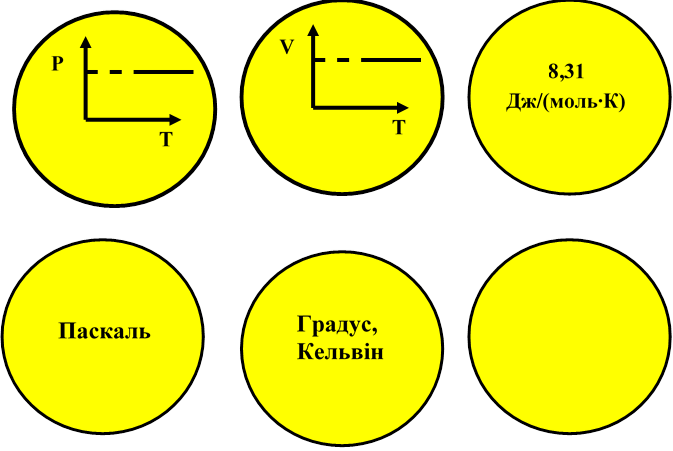
|
|
Рівняння Мендєлєєва - Клапейрона |
Закон Бойля - Маріотта |
|
Закон Гей - Люссака
|
Закон Шарля
|
Графік ізотермічного процесу в координатах Р V
|
|
Графік ізобарного процесу в координатах VТ
|
Графік ізохорного процесу в координатах рТ
|
Числове значення R |
|
Одиниця вимірювання тиску
|
Одиниця вимірювання температури
|
|
Самостійні роботи
Самостійна робота «Основні положення МКТ. Маса та розміри молекул. Будова твердих тіл, рідин і газів»
Варіант 1 1.(2 бали) Заповніть порожні місця в таблиці.
|
Назва фізичної величини |
Символ для позначення |
Найменування одиниці в Сі |
Вираз для визначення |
|
|
|
моль |
|
|
|
|
|
m/Na |
|
Концентрація |
|
|
|
2. (2 бали) Установіть відповідність «основне положення МКТ – явище або властивість, що підтверджує це положення».
А) Усі речовини складаються 1. Тварина навіть у безвітряну погоду здалеку з молекул відчуває запах
Б) Молекули перебувають у 2. Тверде тіло зберігає свою форму безперервному хаотичному 3. Гальмівна колодка під час гальмування русі нагрівається
В) Молекули взаємодіють 4. Рідина у відкритій посудині випаровується
одна з одною
3.
(2 бали) Позначте всі правильні відповіді. Яке твердження є правильним?

Самостійна робота «Основні положення МКТ. Маса та розміри молекул. Будова твердих тіл, рідин і газів»
Варіант 2
1.(2 бали) Заповніть порожні місця в таблиці.
|
Назва фізичної величини |
Символ для позначення |
Найменування одиниці в Сі |
Вираз для визначення |
|
|
М |
|
|
|
|
|
|
m/V |
|
Кількість молекул |
|
|
|
2. (2 бали) Установіть відповідність «основне положення МКТ – спостереження або експеримент що підтверджує це положення».
А) Усі речовини складаються 1. Спостереження за броунівською частинкою з молекул 2. Якщо міцно притиснути один до одного Б) Молекули перебувають у свинцеві циліндри, то вони злипнуться безперервному хаотичному 3. Вивчення фотографії кристала, отриманих за русі допомогою електронного мікроскопа В) Молекули взаємодіють 4. Якщо пропустити струм через провідник, то одна з одною провідник нагріється
3.
(2 бали) Позначте всі правильні відповіді. Яке твердження є правильним?
![]()
Самостійна робота Позначте правильну, на вашу думку, відповідь.
pV
1. Рівність
![]() =
const виконується за умови:
=
const виконується за умови:
T
А нормального атмосферного тиску В сталої маси газу
Б сталої концентрації молекул Г сталої швидкості руху
молекул
2. Процес змінення стану газу сталої маси за незмінного тиску називається:
А адіабатним В ізобарним Б ізотермічним Г ізохорним
8. Визначте процес, зображений на графіку (рис. 1).
![]() А
Адіабатний В Ізобарний Б Ізотермічний
Г Ізохорний
А
Адіабатний В Ізобарний Б Ізотермічний
Г Ізохорний
4. Ізотермічний процес описує закон: А Бойля—Маріотта В Дальтона
Б Гей-Люссака Г Шарля
5. Визначте, на якому графіку зображено ізотермічний процес (рис. 2).
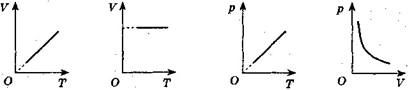
1 2 3 4 рис. 2
6. Під час ізотермічного процесу тиск газу збільшився в 3 рази. Визначте, як і у скільки разів змінився об'єм газу:
А збільшився у 4 рази В збільшився у 3 рази
Б зменшився у 3 рази Г зменшився у 4 рази
7. Під час ізохорного процесу тиск газу збільшився в 3 рази. Визначте, як і у скільки разів змінився об'єм газу.
![]() А Збільшився в 3
рази В Збільшився в 3 Б Не
змінився Г Зменшився в 3
А Збільшився в 3
рази В Збільшився в 3 Б Не
змінився Г Зменшився в 3
8. Укажіть процес, зображений на графіку (рис. 3).
А Ізотермічний
Б Ізобарний
В Ізохорний
Г Даний процес не належить до ізопроцесів
9. Установіть відповідність між законами, що описують ізопроцеси, і назвами ізопроцесів.
1 Закон Бойля—Маріотта А ізобарний
2 Закон Шарля Б ізохорний
3 Закон Гей-Люссака В адіабатний
Г ізотермічний
10. Установіть відповідність між законами, що описують ізопроцеси, та їхнім формулюванням.
1 Закон Бойля— Маріотта А За постійної температури тиск
даної маси ідеального газу прямо пропорційний його абсолютній температурі. 2 Закон Шарля Б За постійного тиску об'єм
3 Закон Гей-Люссака даної маси ідеального газу обернено пропорційний його абсолютній температурі. В У разі теплопередачі неможливий самодовільний процес передачі тепла від менш нагрітих тіл більш нагрітим.
Г За постійного об'єму тиск даної маси ідеального газу прямо пропорційний його абсолютній температурі.
11. Установіть відповідність між законами, що описують ізопроцеси, та їхніми математичними записами.
|
1 Закон Бойля—Маріотта |
Т2 V2 |
|
2 Закон Шарля |
Т2 р2 |
|
3 Закон Гей-Люссака |
pV В T |
|
|
Г plVl = p2V2 |
V
САМОСТІЙНА РОБОТА
ОСНОВНІ ПОЛОЖЕННЯ МОЛЕКУЛЯРНО-КІНЕТИЧНОЇ ТЕОРІЇ (MKT)
Початковий і середній рівні (6 балів) 1. Що є найбільш наочним доказом
Варіант 1 Варіант 2 руху молекул? взаємодії молекул?
2. Визначте молярну масу
Варіант 1 Варіант 2 азоту N2 вуглекислого газу СО2
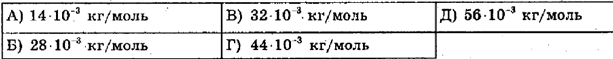
3. Яка кількість речовини міститься в
Варіант 1 Варіант 2 2,7кг алюмінію? 0,8 кг кальцію?
![]()
Достатній рівень (3 бали) 4. Установіть відповідність між
Варіант 1
фізичними поняттями та математичними виразами.
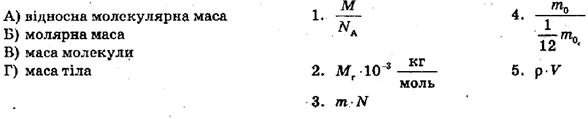
Варіант 2
фізичними поняттями та їх одиницями.

Високий рівень (3 бали)
5. Де міститься більше атомів
Варіанті Варіант 2 в 1 л води чи в 1 л ртуті? в1л води чи в 2 кг міді?
Розв’язок самостійної роботи
Варіант 1 1. Б – дифузія
2.
|
Дано: N2
|
Розв’язання: Молярна маса визначається за формулою М = М r · 10-3 кг/моль. М r (N2) = 28 а.о.м., М = 28·10-3 кг/моль. Відповідь: М = 28·10-3 кг/моль.Б
|
|
M(N2)-? |
3.
|
Дано: Al m = 2,7 кг
|
Розв’язання: Кількість речовини визначається за формулою ν = m /М. М = М r · 10-3 кг/моль. М = 27·10-3 кг/моль. ν = 2,7: 27·10-3 = 0,1·103 = 100 моль. Відповідь: ν = 100 моль. В
|
|
ν - ? |
4. А – 4; Б – 2; В – 1; Г – 5;
5.
|
Дано: V1(H2O) = 10-3 м3 V2(Hg) = 10-3 м3 V1 = V2 = V |
Розв’язання: Кількість речовини визначається за формулою N N m
NA NA M1 M1 M2 M2 Маса речовини m = ρ∙V. N
N2 2NA M12V M12 М = М r · 10-3 кг/моль. М(H2O) = 18·10-3кг/моль; М(Hg) = 201·10-3кг/моль. ρ(H2O)=103кг/м3; ρ(Hg)=13,5·103кг/м3; Виведемо розмірність шуканої фізичної величини:
N2 = м3 кг молькг
N2 13,510 18 10 Відповідь: 0,8 разів |
|
N
N2 |
Розв’язок самостійної роботи
Варіант 2
1. Г – виникнення сил пружності
2.
|
Дано: СО2
|
Розв’язання: Молярна маса визначається за формулою М = М r · 10-3 кг/моль. М r (N2) =(12 +16∙2) = 44 а.о.м., М = 44·10-3 кг/моль. Відповідь: М = 44·10-3 кг/моль.Г
|
|
M(СО2)-? |
3.
|
Дано: Са m = 0,8 кг
|
Розв’язання: Кількість речовини визначається за формулою ν = m /М. М = М r · 10-3 кг/моль. М = 40·10-3 кг/моль. ν = 0,8: 40·10-3 = 0,02·103 = 200 моль. Відповідь: ν =200 моль. Б
|
|
ν - ? |
4. А – 3; Б – 1; В – 2; Г – 4.
5.
|
Дано: V1(H2O) = 10-3 м3 m2 (Cu) = 2 кг |
Розв’язання: Кількість речовини визначається за формулою N N m
NA NA M1 M1 M2 Маса речовини m = ρ∙V. N
N2 2NA M1m2 М = М r · 10-3 кг/моль. М(H2O) = 18·10-3кг/моль; М(Cu) = 64·10-3кг/моль. ρ(H2O)=103кг/м3; ρ(Cu)=8,9·103кг/м3; Виведемо розмірність шуканої фізичної величини:
N2 м молькгкг
N2 2 18 10 Відповідь:1,8 разів |
|
N
N2 |
САМОСТІЙНА РОБОТА
ВЛАСТИВОСТІ ГАЗІВ. ГАЗОВІ ЗАКОНИ. РІВНЯННЯ СТАНУ ГАЗУ
Початковий і середній рівні (6 балів) 1. Як зміниться тиск газу, якщо
Варіант1 Варіант 2
концентрація молекул збільшиться в температура зменшиться в 3
3 рази? 3 рази?

2. Під легким поршнем у циліндрі знаходиться газ при температурі 27 °С. Як зміниться об'єм газу, якщо його
Варіант 1 Варіант 2 нагріти до 227 °С? охолодити до - 123 °С?

3. Який вигляд має поданий на рисунку графік у координатах
![]() Варіант 1 Варіант 2 р,Т?
V, Т?
Варіант 1 Варіант 2 р,Т?
V, Т?
Достатній рівень (3 бали)
4. Установіть відповідність між
Варіант 1
назвами законів та математичними виразами.
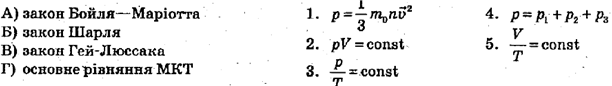
Варіант 2
назвами законів та назвами процесів.

Високий рівень (3 бали)
5. Газовий балон має об'єм 0,4 м3. У балоні знаходиться азот під тиском
105 Па при температурі 27 °С. Яку масу газу підкачали, якщо
Варіант 1 Варіант 2
тиск збільшився до 2∙105 Па тиск збільшився до 3∙105 Па, при сталій температурі? а температура зросла на 20 °С ?
Розв’язки
ВЛАСТИВОСТІ ГАЗІВ. ГАЗОВІ ЗАКОНИ. РІВНЯННЯ СТАНУ ГАЗУ
Варіант 1
1. Б – збільшиться в 3 рази
2. Б – збільшиться в 1,67 рази
|
Дано: t1 =27oC t2 = 227 oC |
Розв’язання. t = 273 + toC. Т1 =27oC +273= 300 oК. Т2 =227oC +273= 500 oК. V T V 500
V1 T1 V1 300 |
|
V
V1 |
![]()
3. Б
4. А– 2; Б – 3; В – 5; Г– 1.
5.
|
Дано: N2 V= 0,4м3 р1 = 105 Па t1 = t2 t = 27oC р2 = 2∙105 Па |
Розв’язання. t = 273 + toC. Т =27oC +273= 300 oК. m= m2 – m1. m Рівняння Мендєлєєва – Клапейрона рV = M m m m m Отже, р1V = M M M M m m RT
M M M ( m2 – m1 = m=
RT M(N2) = 28∙10-3 кг/моль. m = 0,45кг. Відповідь: 0,45кг.
|
|
m - ? |
Варіант 2
1. Г – зменшиться в 3 рази
2. Д – зменшиться в 2 рази
|
Дано: t1 =27oC t2 = -123 oC |
Розв’язання. t = 273 + toC. Т1 =27oC +273= 300 oК. Т2 =227oC - 123= 150 oК. V T V 150 1
V1 T1 V1 300 2 |
|
V
V1 |
![]()
3. В
4. А– 2; Б – 3; В – 5; Г– 1.
5.
|
Дано: N2 V= 0,4м3 р1 = 105 Па р1 = 3∙105 Па t = 20 oC t = 27oC р2 = 2∙105 Па |
Розв’язання. t = 273 + toC. Т1= 27oC +273 = 300 oК. t = 20 oC +273 = 293 oК. m= m2 – m1. m Рівняння Мендєлєєва – Клапейрона рV = M m m Отже, р1V = M M m m (р2 – р1) V = M M R R (р2 – р1) V = M M ( m2 – m1 = m=
RT M(N2) = 28∙10-3 кг/моль. m 0,0092·102кг = 0,92кг. Відповідь: 0,92кг.
|
|
m - ? |
Самостійна робота
Позначте правильну, на вашу думку, відповідь. 1. На якому з графіків а - в (рис. 7) зображено ізохорний процес?
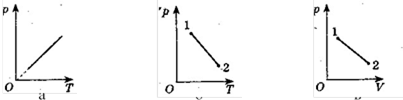
Рис. 7
2. На якому з графіків а - в (рис. 8) зображено ізобарний процес?
![]()
![]()
![]() а б
в
а б
в
Рис. 8
3. На якому з графіків а - в (рис. 9) зображено ізотермічний процес?
![]() а б
в
а б
в 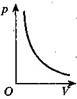
Рис. 9
4. На рис.10 наведено графік залежності тиску даної маси газу від об'єму. Виберіть правильне твердження.
А Графік 1- 2 відповідає ізотермічному процесу
Б Графік 2 - 3 відповідає ізобарному процесу
![]() В Графік 3 - 1 відповідає ізохорному
процесу Рис. 10
В Графік 3 - 1 відповідає ізохорному
процесу Рис. 10
5. На рис. 11 наведено графік залежності об'єму даної маси газу від тиску.
Виберіть правильне твердження.
А Графік 1- 2 відповідає ізотермічному процесу
Б Графік 3 - 4 відповідає ізохорному процесу
В Графік 4 - 5 відповідає ізобарному процесу Рис. 11
6. Газ переведено зі стану 1 у стан 2 (рис. 12). У якій із точок тиск газу більший? А У точці 1
![]() Б У точці 2
Б У точці 2
В У точках 1 і 2 однаковий. Рис. 12
Відповіді до самостійної роботи
1. А. 2. В. 3. В. 4. Б. 5. A. 6. Б.
Дифузія. Будова речовини. Приказки і прислів'я.
1. Вода з водою — не гора з горою: зливається.
2. Кожен цвіт має свій запах.
3. Не кожне зілля пахне.
4. На болоті все гнилим пахне.
5. Ворона за сім миль стерво чує.
6. Не розплакавшись, цибулі не почистиш.
7. Мабуть, добра цибуля, якщо такі добрі сльози.
8. Ну і хрін — сльози, як дзвін.
9. Так надухалась, що на все село розвонялась.
10. Бочка меду, та капля дьогтю.
11. І ложкою дьогтю можна бочку меду зіпсувати. Дим з чадом зійшовся.
12. Ведмідь у лісі броде, хоч погано баче, та мед находе.
13. Лис як не побаче, то нанюхає.
14. Стара лисиця нюхом прокормиться.
15. Лиса лиш димом з нори викуриш.
16. Собака і вночі кістку знайде.
17. Сліпе цуценя, а й те до матері лізе.
18. І сліпий собака господаря знає.
19. Вовки чують, де вівці ночують.
20. Прилип, як смола.
21. Прилип, як мокрий лист до тіла.
22. Сухе болото не пристане.
23. Одрізаного не приставиш.
Загадки
1. Як же вони називаються, що молекули з них складаються? (Атоми) 2. Ми малесенькі частинки, менші за дрібні пилинки, знаєш ти про нас, чи ні — в кожній ми речовині. (Молекули)
3. У воді росте, та води боїться. (Сіль)
4. Положив, як урюк; вийняв, як фляк. (Солоний огірок)
5. Кричить, верещить, як у ринці кипить. (Солоне сало)
6. Схожий на лід, та в річці шукати не слід, бо ж у воді розтане. (Цукор)
7. Все розкажу, хоч і без язика,
Коли буде ясно, а коли — хмарно. (Барометр)
8. Сидить баба на грядці вся в латках, хто зблизька гляне — той заплаче. (Цибуля) ,
10. Під яким кущем сидить заєць, коли дощить? (Під мокрим)
11. Живе — лежить,
Помре — біжить. (Сніг)
12. Прозорий мов скло,
а не-вставиш у вікно. (Лід)
Дифузія в природі (картки1-5).
Картка 1. Якісна задача
![]() Клопи,
сонечка, деякі листоїди озброїлися для свого захисту: запах від клопів огидний,
а сонечка виділяють жовту отруйну рідину. Поясніть передачу запахів.
Клопи,
сонечка, деякі листоїди озброїлися для свого захисту: запах від клопів огидний,
а сонечка виділяють жовту отруйну рідину. Поясніть передачу запахів.
![]()
Картка 2. Якісна задача
Риби дихають киснем, розчиненим у воді річок, озер і морів. Який фізичний процес дозволяє кисню з атмосфери потрапляти у воду?
Картка 3. Якісна задача
![]() Як бджоли
знаходять нектар та, виявивши
Як бджоли
знаходять нектар та, виявивши
солодкий об'єкт,
Картка 4. Якісна задача
![]() Чому, перш ніж зробити укол
пацієнтові, холодний розчин з ін'єкцією лікар нагріває до температури близької
до температури тіла людини?
Чому, перш ніж зробити укол
пацієнтові, холодний розчин з ін'єкцією лікар нагріває до температури близької
до температури тіла людини?
![]() Картка
5. Якісна задача
Картка
5. Якісна задача
Яке фізичне явище проявляється при митті рук? Як правильно мити руки?
Дифузія в побуті та техніці(картки5-10).
Картка 6. Якісна задача
![]() Чому чай заварюють
гарячою, а не холодною водою?
Чому чай заварюють
гарячою, а не холодною водою?
Картка 7. Якісна задача
![]() Чому не
рекомендується мокру тканину пофарбовану в темний колір, залишати
на тривалий час у зіткненні з білою тканиною?
Чому не
рекомендується мокру тканину пофарбовану в темний колір, залишати
на тривалий час у зіткненні з білою тканиною?
![]() Картка 8. Якісна задача
Картка 8. Якісна задача
Чому, щоб огірки вийшли малосольними, їх зберігати в холодному приміщенні?
Картка 9. Якісна задача
![]() Чому забороняється
перевозити разом
продукти і речовини з різким запахом.
наприклад, лаки, фарби?
Чому забороняється
перевозити разом
продукти і речовини з різким запахом.
наприклад, лаки, фарби?
Негативний вплив дифузії (картки 1-15).
Картка 10. Якісна задача
![]() При ремонті
дороги асфальт розігрівають. Чому запах розігрітого асфальту відчувається
здалеку?
При ремонті
дороги асфальт розігрівають. Чому запах розігрітого асфальту відчувається
здалеку?
![]() Картка 11. Якісна
задача
Картка 11. Якісна
задача
Чому дим з часом стає непомітним ?
Як він впливає на якість повітря?
Картка 12. Якісна задача
![]() Природний горючий газ, яким ми користуємося вдома, не
має ні кольору, ні запаху ... При витіканні помітити його неможливо, тому на
розподільних станціях газ змішують із особливою речовиною, що має різкий,
неприємний запах. Для чого це роблять?
Природний горючий газ, яким ми користуємося вдома, не
має ні кольору, ні запаху ... При витіканні помітити його неможливо, тому на
розподільних станціях газ змішують із особливою речовиною, що має різкий,
неприємний запах. Для чого це роблять?
Картка 13. Якісна задача
![]() Яке явище лежить в основі процесу паління?
Чи відбувається дифузія диму в
легені людини, що знаходиться поряд з
людиною, що палить?
Яке явище лежить в основі процесу паління?
Чи відбувається дифузія диму в
легені людини, що знаходиться поряд з
людиною, що палить?
Картка 14. Якісна задача
![]() Яке явище спричиняє забрудненню річок, морів і океанів,
ґрунту і атмосфери Землі? Як відбувається цей процес?
Яке явище спричиняє забрудненню річок, морів і океанів,
ґрунту і атмосфери Землі? Як відбувається цей процес?
Картка 15.Якісна задача

Яке явище об'єднує ці фото? Обґрунтувати його шкідливий вплив
Якісні задачі
1. Дитячий гумова куля, наповнена воднем(або гелієм) через кілька годин став слабо надутим. Чому? (Відбулася дифузія - с часом в результаті дифузії молекули водню проникають через проміжки між частинками гуми}
2. Всім повідає, хоч і без мови, коли буде ясно, а коли хмари. (Барометр)
3. Яке Речовини отримує іншу назву при переході з рідкого стану в твердий? (Вода)
5. Що спільного між парою, водою й льодом? (Молекули)
6. Чому розламаний олівець ми не можемо поєднати так, щоб він знову став цілим? (Сили тяжіння починають діяти при дуже малих відстанях) 7. Який фізичний зміст абсолютного нуля температур? (Припиняється тепловий рух молекул)
8. У якому випадку гаряча вода охолоне швидше: якщо в нього опустити срібну ложку або алюмінієву? (алюмінієву - у неї більше теплопровідність) 9. Альпіністи на великій висоті наготовлювали їжу. Після покладеного часу кип'ятіння вони виявили, що продукти не зварилися. У чому причина?
(Температура кипіння менше 100 °)
10. Як видалити вм'ятину оболонки м'яча настільного тенісу? (Опустити в гарячу воду)
11. У дві однакові каструлі налито по рівній кількості води при одній і тій же температурі, але в одну з них-сира вода, в іншу-кип'ячена. якщо поставити обидві каструлі на вогонь однакової сили, то в якій з них вода закипить швидше? (Сира вода закипить швидше, так як в кип'яченій менше розчиненого повітря.)
12. Чим пояснюється збільшення довжини дроту при її нагріванні. (При нагріванні проміжки між молекулами дроту збільшуються, обсяг тіла збільшується, і довжина проволоки теж; збільшується).
13. Чи однакові молекули води в гарячому чаї і в холодній газованій воді. (Молекули води однакові і в гарячому чаї, і в холодній воді. Вони відрізняються лише швидкістю руху: в гарячому чаї молекули рухаються швидше, ніж в холодній газованій воді, так як, чим вище температура тіла, тим більше швидкість молекул).
14. Чому для зварювання металевих деталей необхідні їх щільне зіткнення і дуже висока температура? (При високій температурі середня швидкість руху молекул дуже велика і при щільному зіткненні деталей, що зварюються дифузія, тобто переміщення молекул відбувається швидше і глибоко, що забезпечує необхідну швидкість і високу міцність зварювання) .
15. Чому, розламав олівець, ми не можемо з'єднає його частини так, щоб він знову став цілим?( Навіть при дуже близькому і щільному з'єднані частин олівця лише в небагатьох точках його частки зближуються на відстань дії взаємного тяжіння).
16. Чи однакові молекули льоду, води і водяної пари?'(Молекули води, льоду і пара однакові, вони відрізняються тільки взаємним розташуванням і швидкістю руху)
17. Чому молекули одного і того ж газу при постійній температурі рухаються з однаковими швидкостями?( Через взаємного зіткнення між: молекулами при їх хаотичному русі.)
18. Чому орли, яструби, шуліки і інші великі птахи, які летять високо в небі, можуть триматися на одній висоті, що не змахуючи при цьому крильми? (Нагріте у землі повітря піднімається на значну висоту. Ці теплі потоки повітря вдаряють знизу в розпростерті крила птаха і підтримують її).
19. Чому, коли скла з полірованою поверхнею кладуть одне на інше кладуть між ними папір? (Щоб скло не злипалось під дією сил тяжіння).
20. Чому не можна з'єднати в одну дві дерев'яні лінійки щільно притиснувши їх один до одного. (Дерев'яні поверхні, прикладені один до одного лінійок нерівні, тому число «точок дотику» в яких діють сили молекулярного притягання мало).
21. Стан газу, при якому молекули можуть пролетіти від однієї стінки посудини до іншої ні разу не стикаючись один з одним. (Ідеальний газ).
22. Чим пояснюється поширення в повітрі запахів бензину, диму, нафталіну, духів і інших пахучих речовині (Дифузією молекул даної речовини між: молекулами повітря).
23. Молекули газу рухаються зі швидкостями порядку кілька сотень метрів в секунду. Чому ж в повітрі запах пролитого близько нас бензину ми не відчуваємо миттєво?( З-за численних зіткнень молекула багаторазово змінює напрямок вектора швидкості (броунівський рух). В результаті цього середня швидкість молекули і, відповідно, швидкість поширення запаху, зменшується в сотні і тисячі разів).
24. Однією з умов готовності варення є рівномірне розташування ягід у сиропі. Як це иоясиити7(Спочатку густина ягід менша за густину сиропу, і вони плавають на поверхні. Через деякий час внаслідок дифузії, яка за високої температури проходить досить швидко, густина ягід збільшується і стає рівною густині сиропу).
25. Вода, що витікає з водопровідного крану, іноді буває біла, як молоко. Потім, налита в посудину, швидко світліє, стає прозорою. Поясніть це явище. (Вода здається білою від великою кількості бульбашок повітря, які виходять за геї. Внаслідок зменшення тиску бульбашки розширюються і виходять на поверхню).
26. Існує спосіб підживлення рослин через коріння, а також позакореневе. Як пояснити це підживлення7(Підживлення рослин здійснюється шляхом дифузії молекул поживних речовин через поверхню листя).
27. Чому в процесі обробки металів різанням на передній частині різального інструменту утворюється наріст з частинок оброблюваного металу? (Наріст утворюється через високі температури і тиски, що розвиваються на різальній кромці. За таких умов проявляються явища дифузії і взаємного притягання молекул).
28. Чому пил, що представляє частки твердої речовини, досить довго утримується в повітрі у зваженому стані?(Порошинки відчувають безперервні удари з боку хаотично рухаючих молекул повітря).
29. Чому балони зі стиснутими газами (киснем, воднем, ацетиленом) не можна нагрівати вище 35 °С? (В результаті підвищення температури, відповідно до закону Шарля, тиск у балоні зростає. Якщо температура буде більша 35 °С, то балон може розірватися)
30. Чому балон із будь-яким стисненим газом становить велику небезпеку при пожежі? (Зростаючи при нагріванні тиск газу може розірвати балон і надати його осколкам великої швидкості).
31. Чи може бути кухонна сіль рідкою, а вуглекислий газ твердим? (Так, при нормальному атмосферному тиску кухонна сіль стає рідкою при температурі 800 °С (а вуглекислий газ твердим - при 250 ° С).
32. ![]() Яка буде форма рідини, якщо перелити
її зі склянки в колбу, в мензурку ? Чи зміниться при цьому її обсяг?
Яка буде форма рідини, якщо перелити
її зі склянки в колбу, в мензурку ? Чи зміниться при цьому її обсяг?
33. Чому не вдається наповнити пляшку
рідиною, якщо воронка щільно притиснута до
стінок шийки пляшки?(Повітря займає весь об'єм пляшки, а сила, з якою налита в воронку вода тисне на повітря, недостатня, щоб стиснути його в значній мірі).
34. Чому при згинанні прутика паяльного олова чутний характерний тріск?
(Руйнуються зв'язку між; кристалами олова).
35. Як можна пояснити зникнення диму в повітрі?
(Частинки диму, потрапляючи в повітря, починають брати участь в броунівському русі (тепловий рух зважений в рідині або газі частинок в) і віддаляються один від одного. Таким чином, об'єм, займаний димом, збільшується, і, отже, щільність диму зменшуватись. Дим зникає в повітрі) 36. З сирого дерева виточили дві кулі. Поверхня одного з них покрили спиртовим лаком. Куля, поверхня якого не покрили лаком, через деякий час розтріснувся, а куля, покритий лаком, залишився цілий. Чому?
(Коли дерево "просихає", пари дифундують з його поверхні. Плівка лаку, що покриває куля, уповільнює цей процес. Куля "просихає"рівномірно по всій товщині, зберігаючи однорідність, не розтріскується) 37. Чи може маса якого - не будь тіла бути рівною нулю? (Ні, тому що будь-яка речовина складається з молекул, а кожна молекула має певну масу.)
38. У 1872 році англійський вчений Броун спостерігав під мікроскопом безладний рух зважених в рідини частинок. Як пояснити цей рух з точки зору молекулярної теорії? (Рух частинок викликається ударами невидимих в оптичний мікроскоп частками).
39. Чому тверді тіла, що складаються з величезного числа молекул зберігають свою форму і не розсипаються на окремі частки. (Міцність твердих тіл пояснюється силами молекулярного тяжіння)
40. З'єднайте два шматка свинцю або пластиліну. Поясніть, чому вони "прилипають" один до одного. Чому аналогічний досвід не вдається з шматками заліза і розбитого скла? (Шматки шматками заліза і розбитого скла стикаються тільки в декількох точках, і сили тяжіння виявляються недостатніми, щоб міцно з'єднати шматки).
41. У метрову скляну трубку налийте до половини води, а зверху спирту і потім перемішайте їх. Як змінився обсяг рідини після цього? Поясніть чому? (Загальний обсяг зменшився в результаті більш щільною упаковки молекул} 42. Якщо притиснути одну до одної пластинки свинцю і золота, то через деякий час в золоті можна виявити молекули свинцю, а в свинці - молекули золота. Поясніть чому? (В твердих тілах і рідинах між молекулами, незважаючи на їх щільну упаковку, є невеликі проміжки. Молекули здійснюють рух в першу чергу коливальні. Картина нагадує людей в наповненому автобусі, які, незважаючи на тісноту, переміщаються, міняючись місцями один з одним або проходячи в випадково утворивши проходи.)
42. Розбийте шматок вару і поясніть, чому на зламі завжди утворюється гладка поверхня. (Вар загусла рідина, тому його молекули не утворюють правильні шари, що чергуються як в кристалічному тілі).
43. Чому після дощу пил на дорозі не піднімається? (Частинки пилу, змочені водою, злипаються, і їх маса збільшується. Тому їх важче підняти в повітря).
44. Чому для розділення листів паперу, змочених водою, потрібно значно велике зусилля, чим при перегортанні сухих листів книги? (Взаємодія між молекулами мокрого листа сильніше за взаємодію між молекулами сухого листа).
45. Чому на класній дошці пишуть крейдою, а не шматком білого мармуру? 46. Що можна сказати про взаємодію між частками цих речовин? (Взаємодія між молекулами мармуру настільки сильніша, що сили тертя мармуру об дошку недостатньо для дроблення мармуру. Сила тяжіння між молекулами крейди значно менше, чим у мармуру
47. У яких речовин (свинець, віск, сталь) сила тяжіння між частками максимальна; мінімальна? (Максимальна -у сталі, мінімальна у-воску).
48. Молекули твердого тіла знаходяться у безперервному русі. Чому ж тверді тіла не розпадаються на окремі молекули.(Молекули твердого тіла досить сильно взаємодіють між; собою).
49.
Плоскопаралельні
кінцеві довжини відполірували так, що при контакті вони прилипають один до
одного і і взаємно ![]() утримуються.
Поясніть причину цього явища.
утримуються.
Поясніть причину цього явища.
(Зважаючи на гладкість пластин при їх зіткненні
багато часток поверхні зближуються до відстаней, на яких важливу роль починають грати сили міжмолекулярного тяжіння).
50. Зварювання металевих деталей можна виконати і холодним способом, якщо їх, з'єднавши, дуже сильно здавити. За якої умови таке зварювання може бути виконане? (Таке зварювання може бути виконане за умови, що
більшість часток на поверхні зварюваних деталей будуть зближені на відстані взаємного тяжіння).
51. Скляну пластинку, підвішену на гумовому шнурі, опустили до зіткнення з поверхнею води. Чому при підйомі пластинки шнур розтягується?
(Вода в результаті міжмолекулярної взаємодії змочує і притягує скляну пластину).
52. У якому стані - твердому або рідкому - сила тяжіння між молекулами свинцю більша? (У твердому)
52. Олія порівняно легко віддаляється з чистої поверхні міді. Видалити ртуть з тієї ж поверхні неможливо. Що можна сказати про взаємне тяжіння між молекулами олії і міді, ртуті і міді. (Молекули олії взаємодіють з міддю слабкіше за молекули ртуті).
53. Що є загального між склеюванням паперу і паянням металевих виробів? (При склеюванні паперу і паянні металевих виробів в поверхневий шар склеювання листів (тіл, що спаюються) проникають частки клею (припою). При цьому взаємодія між молекулами клею і паперу (частками металу і припою) більша, ніж між; молекулами склеюваних листів паперу (металевих виробів, що спаюються).
54. Чим відрізняється зварювання металевих деталей від паяння металевих виробів?(Л/ш зварюванні обходяться без припою, за рахунок дифузії молекул самих зварюваних тіл).
55. Чи можна відкриту посудину заповнити газом на 50% його місткості? (Ні, оскільки газ займає увесь наданий йому об'єм).
56. Закрита пляшка наполовину заповнена ртуттю.,Чи можна стверджувати, що у верхній половині пляшки ртуть відсутня? (Ні, в ній містяться пари ртуті).
57. Чи можуть бути в рідкому стані кисень, азот?
(Можуть (при низьких температурах і високих тисках)
58. Чи можуть бути в газоподібному стані ртуть, залізо, свинець?
Можуть (при високих температурах)
59. Літнім вечором над болотом утворився туман. Який цей стан води?
(Рідкий стан (туман - найдрібніші крапельки води))
60. У зимовий морозний день над ополонкою утворився туман. Який цей стан води? (Твердий стан (туман - найдрібніші кристали льоду))
61. Свіжий, хоча і невидимі слід собака "бере". Проте з часом вона його учути не може. Поясніть це явище. (Внаслідок дифузії молекул слід зайця поступово втрачає запах останнього).
62. У полістироловій флязі тривалий час зберігався гас. Якщо в цю, навіть дуже вимиту, флягу налити молоко, то в нім ми все ж відчуватимемо запах гасу. Поясніть чому? (Гас добре змочує флягу, вбирає в її внутрішню поверхню. Повністю видалити його простим миттям фляги неможливо). 63. Шматок олова нагрівали, і воно перейшло в рідкий стан. Як при цьому мінявся рух і розташування часток олова один відносно одного?
(Рух часток став інтенсивнішим, а відстань між молекулами збільшилася).
64. Вода випарувалася і перетворилася на пару. Чи змінилися при цьому самі молекули? Як змінилося їх розташування і рух?
(Самі молекули не змінилися, а відстань між; ними і швидкість їх руху збільшилася).
Контрольно робота «Основні положення МКТ»
Варіант 1
Початковий рівень
1. Чому молекули одного і того ж газу при постійній температурі рухаються з різними швидкостями?
2. Чому влітку на лузі після заходу сонця туман спочатку з'являється в низинах? Середній рівень
3. Визначити молярну масу ацетону (С3Н6О).(1б)
4. Визначити відносну вологість повітря в кімнаті при 20 °С , якщо точка роси становить 13 °С. Достатній рівень
5. В ідеальній тепловій машині за рахунок кожного кілоджоуля енергії, одержуваної від нагрівача, здійснюється робота 300Дж. Визначте ККД машини і температуру нагрівача, якщо температура холодильника 280К. Високий рівень
6. Тіло масою 6 т піднімають із прискоренням 0,2м/с2, Матеріал троса витримує максимальну механічну напругу 800 МПа. Який повинен бути діаметр троса при запасі міцності 5?
Варіант 2
Початковий рівень
1. До якому виду двигунів буде відноситься вогнепальна зброя?
2. Чому крапля води розтікається на підлозі, а крапля ртуті — ні? Середній рівень
2. Визначити масу водню, що знаходиться в балоні, об'ємом 20 л під тиском 8,3∙105 Па при температурі 17°С.
4. Під дією сили 100 Н дротина довжиною 4 м і перерізом 2∙10-4 м2 видовжилась на 4мм. Визначити механічну напругу і відносне видовження дротини. Достатній рівень
5. Кількість теплоти, яку передає нагрівник робочому тлу ідеальної теплової машини 37,3 кДж. Температура нагрівальника 373 К, а холодильника 273К. Визначити роботу, виконану машиною за цей час.
Високий рівень
6. Тіло масою 6 т піднімають із прискоренням 0,2м/с2, Матеріал троса витримує максимальну механічну напругу 800 МПа. Який повинен бути діаметр троса при запасі міцності 5?
Список літератури
1. Л.І. Вялих, Т.В. Чертищева. Тест – контроль. Фізика. Зошит для самостійних та контрольних робіт. 10 – 11 класи. Харьків., 2011.
2. О. Гончар. Збірник завдань. Тернопіль. Видавництво «Підручники і посібники»., 2015
3. Збірник задач з фізики для 9 – 11 класів. Укладач Г.Н.Степанова.
Москва 1977
4.М.Е. Тульчинський. Якісні задачі з фізики в середній школі. Москва.
«Просвещение» 1972 рік
http://yadi.sk/d/TuG5k8N7GfLYb
Зміст
Конспект до уроку……………………………………………….. 2
Опорні конспекти ……………………………………………….. 5
Вчимося розв’язувати задачі …………………………………… 13
Збірник задач ……………………………………………………. 23
Диктанти …………………………………………………………. 25
Тести ……………………………………………………………… 29
Індивідуальна робота с картками ……………………………….. 41
Лото ……………………………………………………………….. 50
Самостійні роботи ………………………………………………... 57 Якісні задачі …………………………………………………….... 69
Контрольна робота ………………………………………………. 79
Список літератури ……………………………………………….. 75

про публікацію авторської розробки
Додати розробку

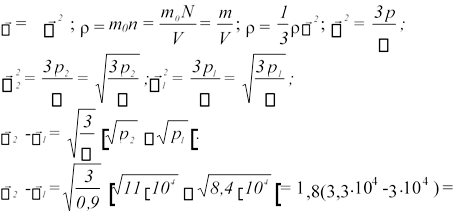
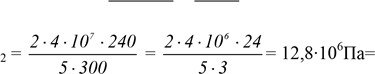 M M р
M M р