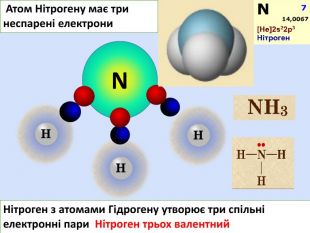
Тема уроку: "Ковалентний зв'язок"


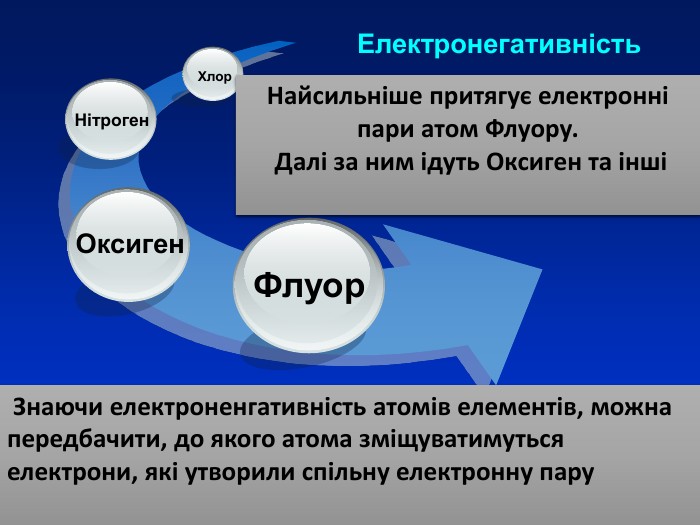
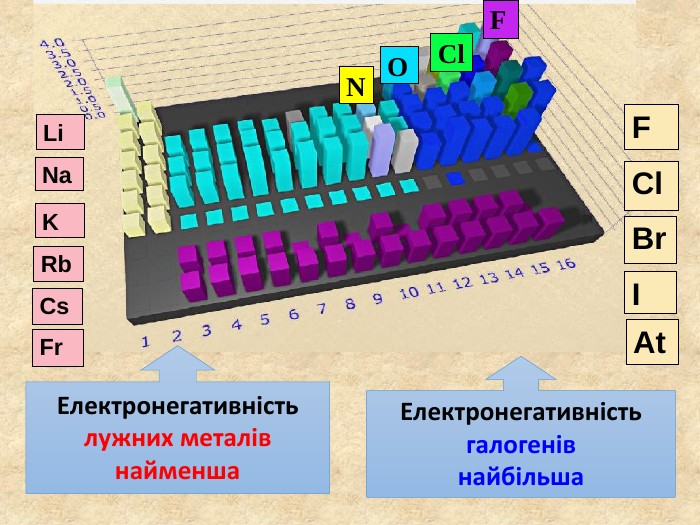














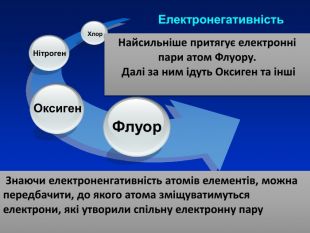
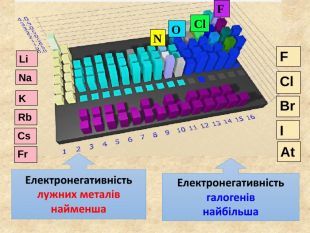
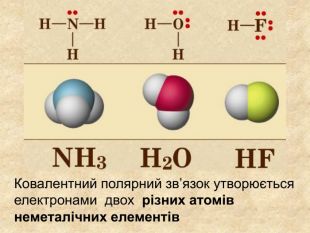
При утворенні спільної електроної пари двома атомами різних хімічних елементів один з них притягує її сильніше ніж інший. Електронегативність Електронегативність ― умовна величина, яка характеризує здатність атома в сполуці притягувати до себе електрони За одиницю електронегативності прийнято електронегативність Літію, і з нею порівнюють електронегативності інших елементів
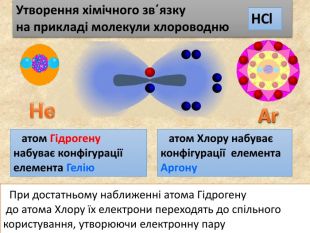
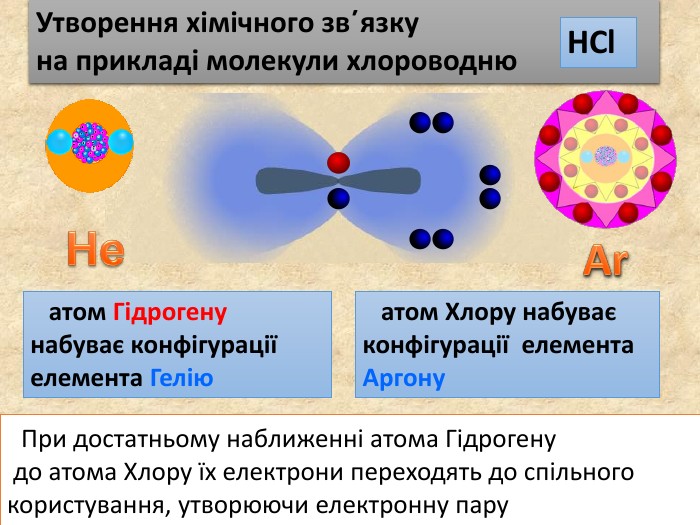
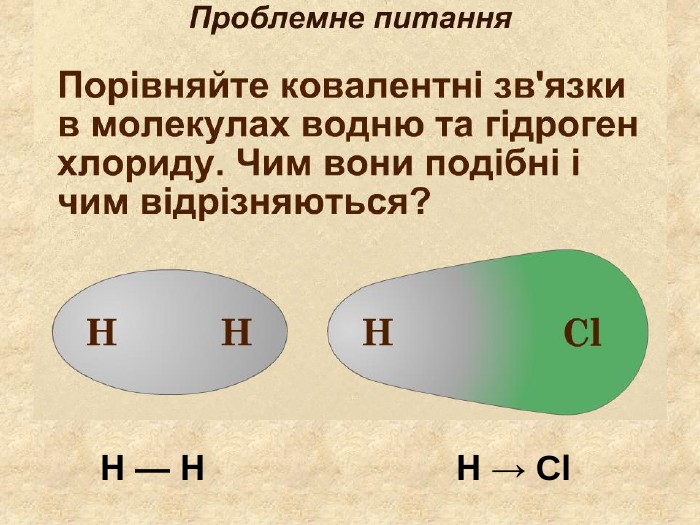
Утворення хімічного зв΄язку на прикладі молекули хлороводню При достатньому наближенні атома Гідрогену до атома Хлору їх електрони переходять до спільного користування, утворюючи електронну пару. Не атом Гідрогену набуває конфігурації елемента Гелію атом Хлору набуває конфігурації елемента Аргону Ar НCl. Cl. Н
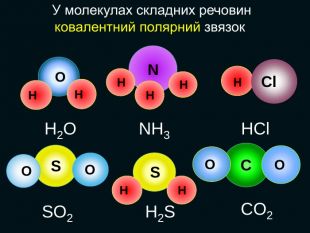
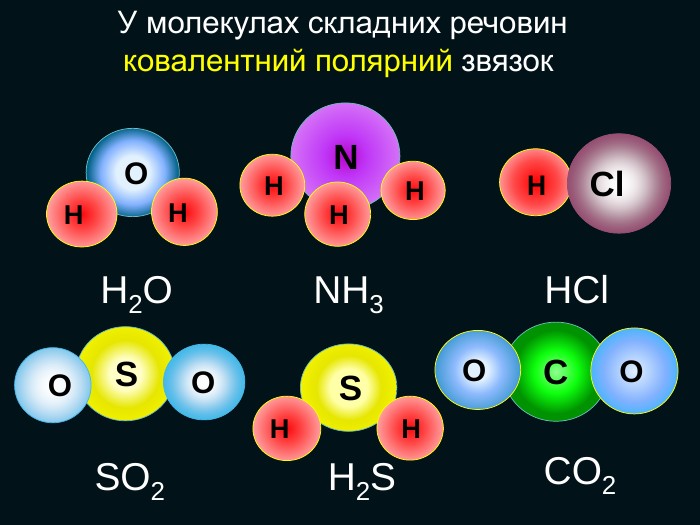
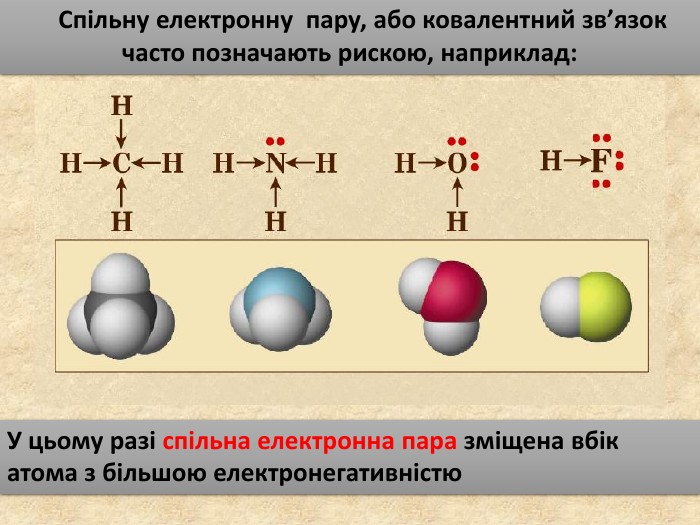
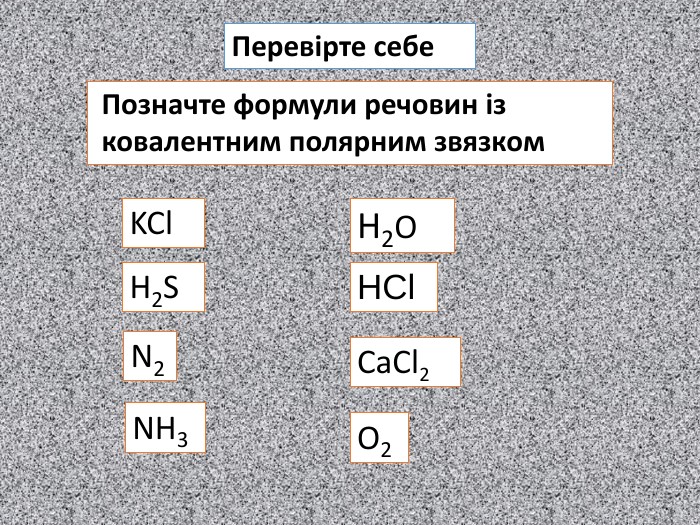
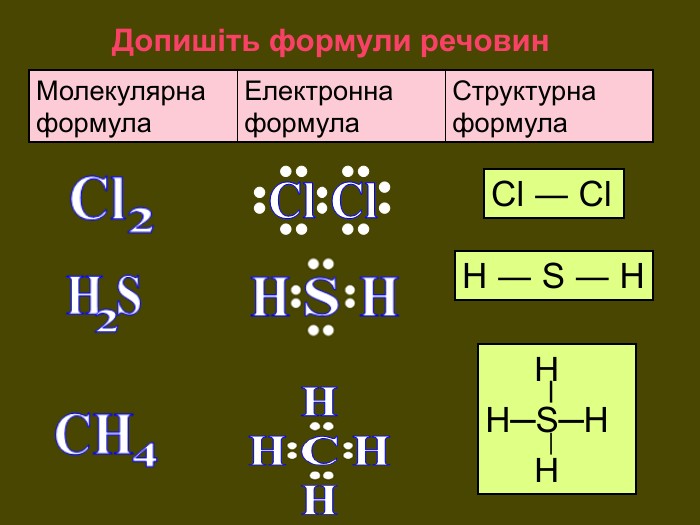
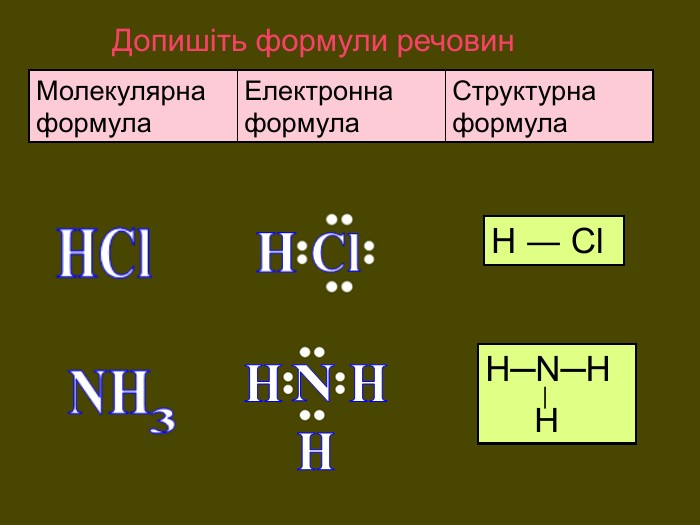
НCl N H H OHH H SH H S O O C O OH2 OSO2 H2 SCO2 NH3 HCl У молекулах складних речовин ковалентний полярний звязокstyle.colorfillcolorfill.typefill.onrrrrrstyle.colorfillcolorfill.typefill.onrrrrrstyle.colorfillcolorfill.typefill.onrrrrrstyle.colorfillcolorfill.typefill.onrrrrrstyle.colorfillcolorfill.typefill.onrrrrrstyle.colorfillcolorfill.typefill.onrrrrr
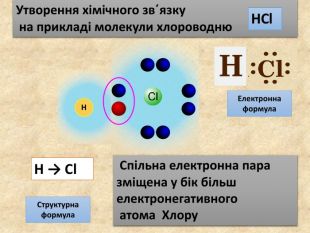
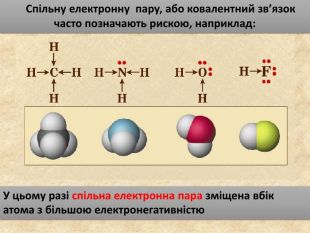
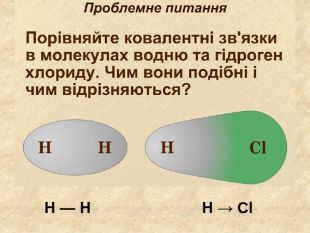
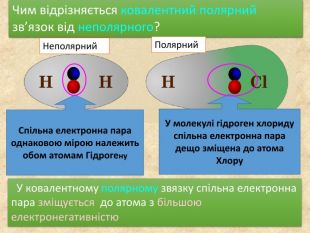
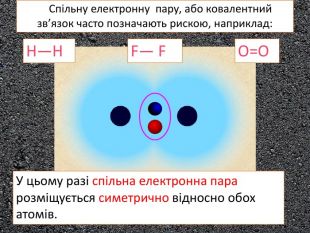
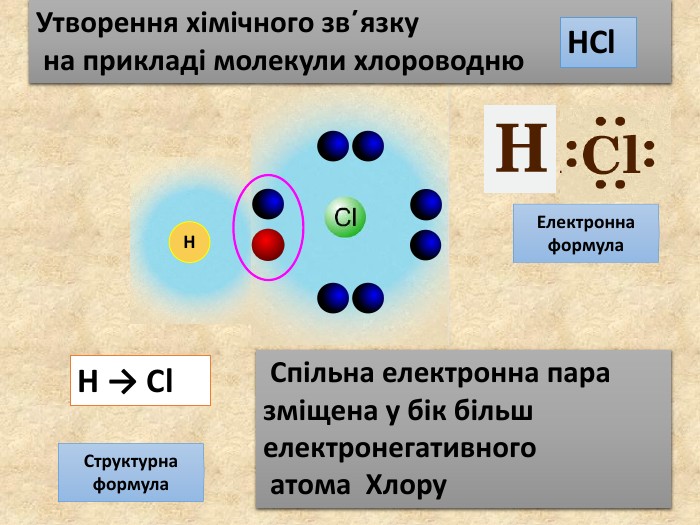
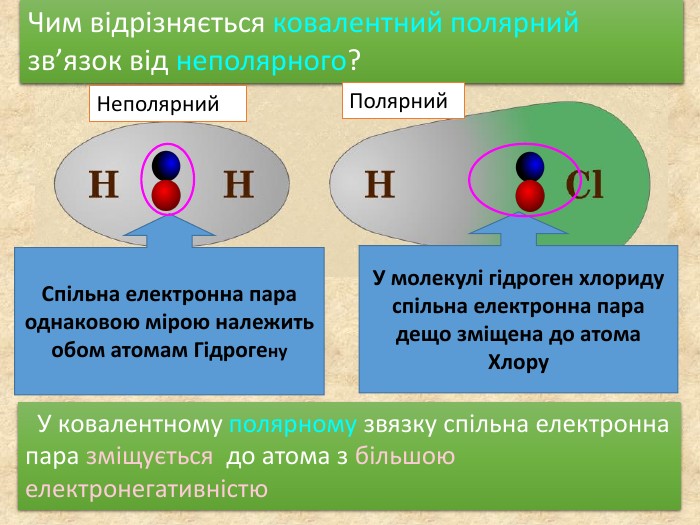
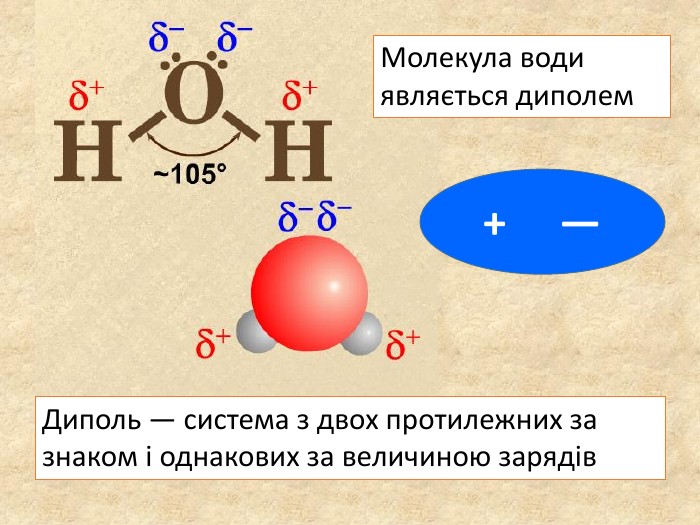
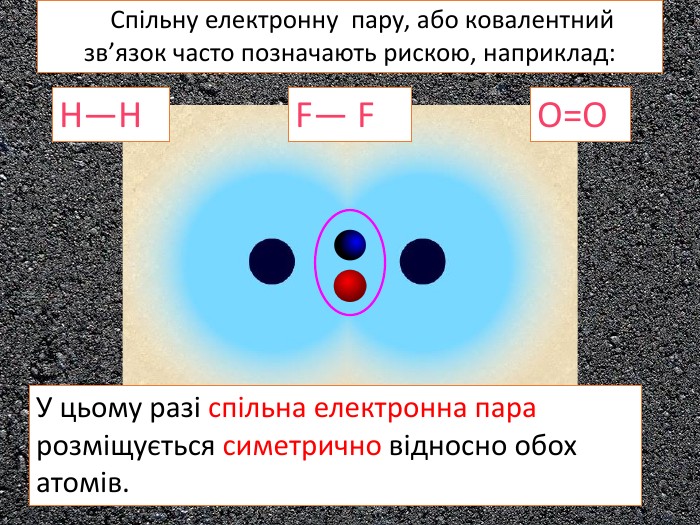
У ковалентному полярному звязку спільна електронна пара зміщується до атома з більшою електронегативністю. Чим відрізняється ковалентний полярний зв’язок від неполярного?Спільна електронна пара однаковою мірою належить обом атомам Гідрогену. У молекулі гідроген хлориду спільна електронна пара дещо зміщена до атома Хлору. Неполярний Полярний
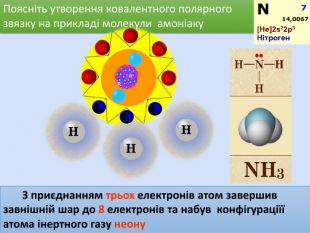
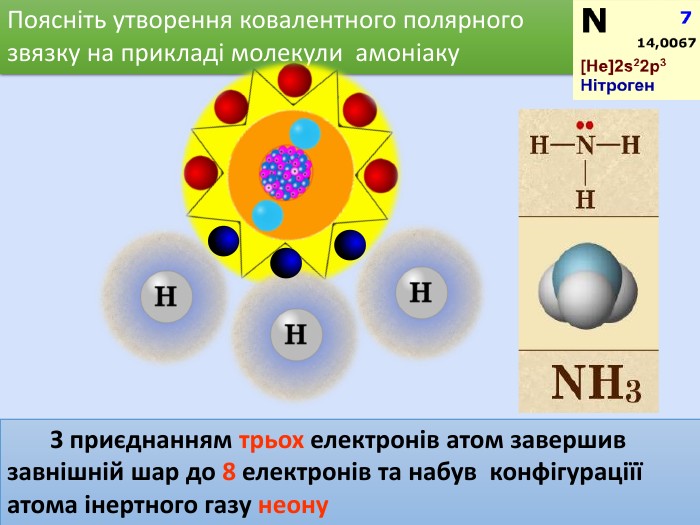
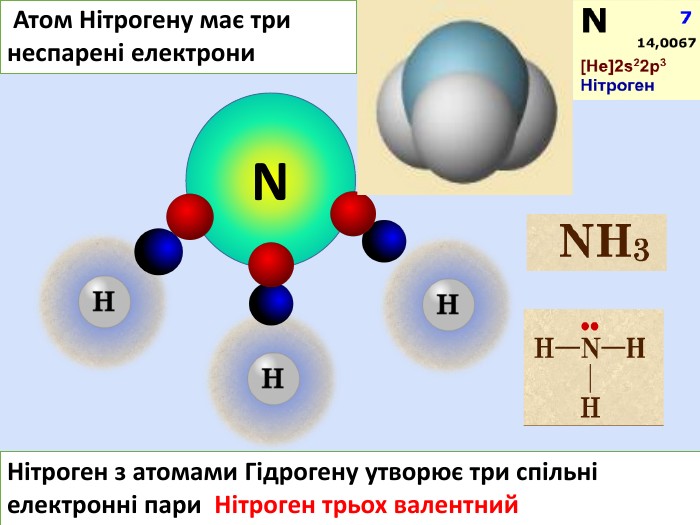
Поясніть утворення ковалентного полярного звязку на прикладі молекули хлороводню У молекул хлороводню НCl атом Гідрогену зарахунок “чужого” електрона завершує перший енергетичний рівень, а атом Хлору ― третій У цьому разі спільна електронна пара зміщується вбік до атома Хлору Такий зв’язок називається полярним.+→ Ar. НCl. Н→ Cl
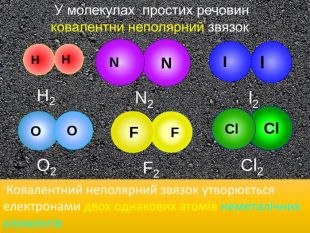
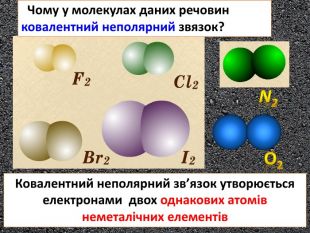
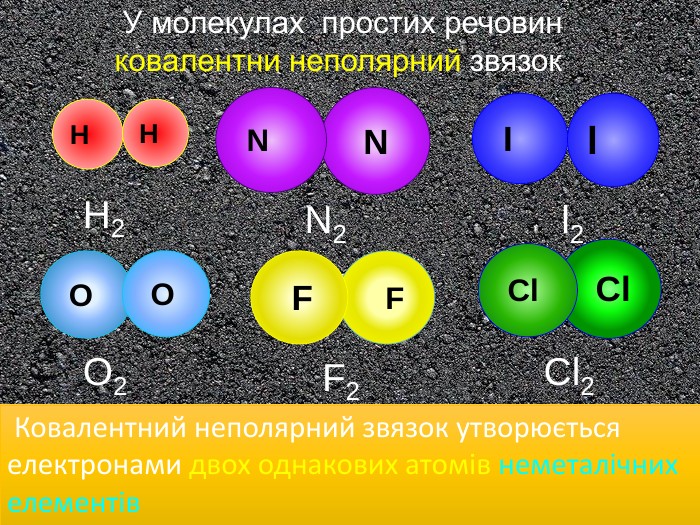
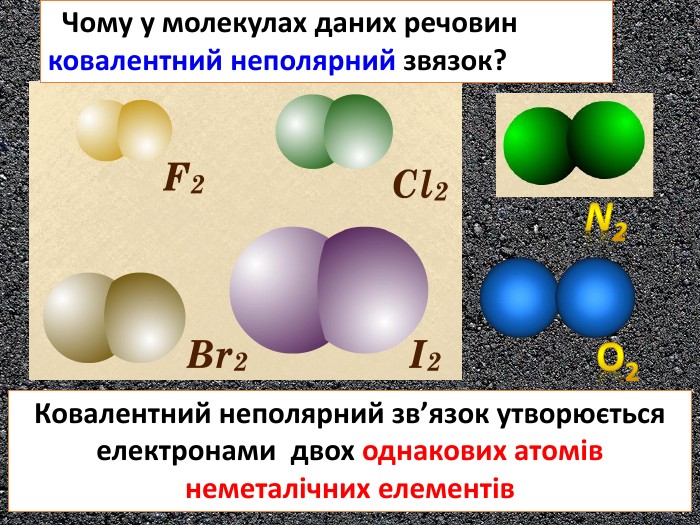
Il N NHH F F Cl Cl. H2 O2 F2 Cl2 N2l2 У молекулах простих речовин ковалентни неполярний звязок O O Ковалентний неполярний звязок утворюється електронами двох однакових атомів неметалічних елементівstyle.colorfillcolorfill.typefill.onrrrrrstyle.colorfillcolorfill.typefill.onrrrrrstyle.colorfillcolorfill.typefill.onrrrrrstyle.colorfillcolorfill.typefill.onrrrrrstyle.colorfillcolorfill.typefill.onrrrrrstyle.colorfillcolorfill.typefill.onrrrrr
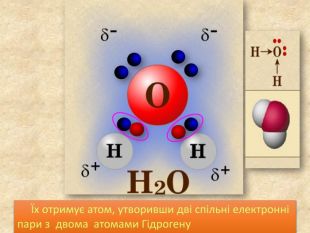
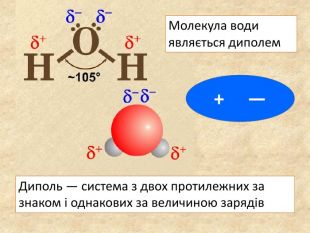
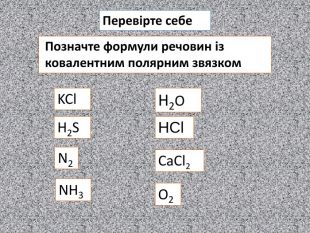
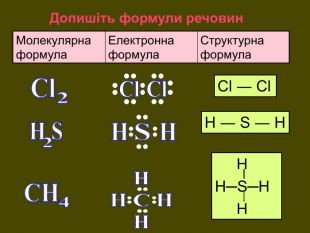
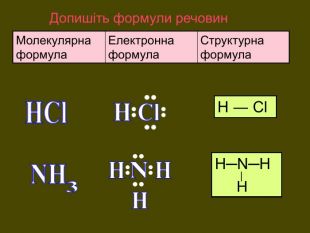
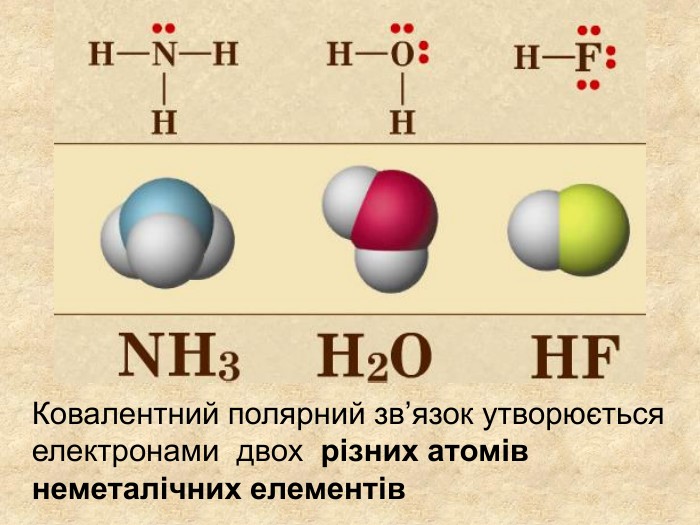
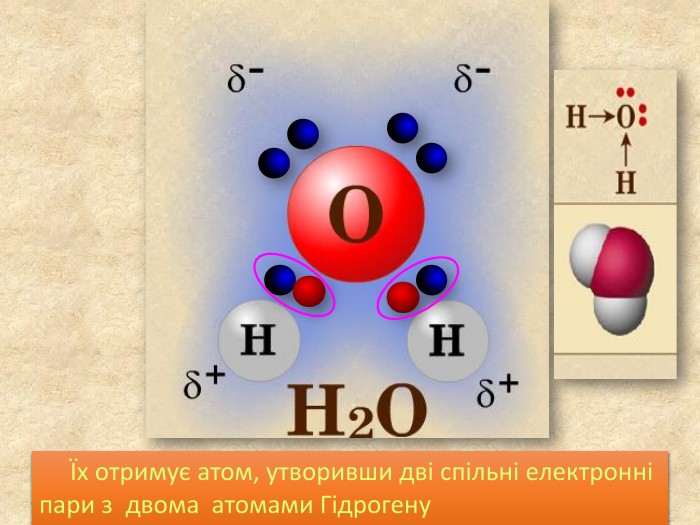
Хімічний зв’язок, який утворюється за допомогою спільних електронних пар, які зщміщені в бік електронгативного атома, називається ковалентним полярним зв'язком До речовин з ковалентним полярним зв’язоком відносяться речовини, утворені атомами неметалічних елементів, що мають різну електронегативність:хлороводень HCl, вода H2 O, сірководень H2 S, метан CH4


про публікацію авторської розробки
Додати розробку