ТЕМА УРОКУ. ПОНЯТТЯ ПРО ЯВИЩЕ ІЗОМЕРІЇ ТА ІЗОМЕРИ.
ДНЗ «Борщівський професійний ліцей.»
ТЕМА УРОКУ. ПОНЯТТЯ ПРО ЯВИЩЕ ІЗОМЕРІЇ ТА ІЗОМЕРИ.
Підготувала викладач хімії та біології
вищої категорії, старший вчитель
Фургач Т.Й.
Дата ___/___/___ Урок №
ТЕМА. ПОНЯТТЯ ПРО ЯВИЩЕ ІЗОМЕРІЇ ТА ІЗОМЕРИ.
Мета:
- Узагальнити й систематизувати знання учнів про склад, властивості, застосування окремих представників вуглеводнів, дати поняття про ізомерію та структурні формули ізомерів;
- розвивати вміння й навички учнів самостійно визначати ізомерів, використовувати раніше набуті знання в новій навчальній ситуації;
- виховувати творчу, допитливу особистість.
Обладнання та реактиви: підручник, картки із зразками ізомерів, моделі вуглеводнів.
Базові поняття та терміни: явище ізомерії, ізомери.
Тип уроку: комбінований.
Форми роботи: Метод «Мозковий штурм»; Лекція вчителя з елементами бесіди.
Прийоми «Творча лабораторія» «Бліц – фініш»;
Наскрізні змістовні лінії:
Громадянська відповідальність.
Навчатися працювати в команді, відповідально ставитись до завдань, визначених колективом, та ретельно виконувати свою частину роботи. У позаурочний час дбати про чистоту навколишнього середовища свого регіону, брати посильну участь у реалізації соціально значущих навчальних проектів.
Здоров’я і безпека.
Дотримання правил безпечного поводження з речовинами і матеріалами у лабораторії, побуті й довкіллі; усвідомлення залежності здоров’я від чистоти води, повітря, складу харчових продуктів; дотримання здорового способу життя.
Екологічна безпека і сталий розвиток
Значення ізомерів у природі і їхній вплив на здоров’я людей та довкілля за їх неправильного використання.
Забезпечення збереження довкілля під час одержання, зберігання, транспортування і застосування вуглеводнів та їхніх похідних
Підприємливість і фінансова грамотність
Одержання ізомерів, їх застосування.
Компетентності: предметна компетентність, ключова компетентність: інформаційно-цифрова, спілкування державною мовою, екологічна грамотність і здорове життя, обізнаність та самовираження у сфері культури, математична компетентність
Хід уроку
І. Організаційний момент
Привітання, побажання хорошого настрою.
II. Актуалізація опорних знань
На початку уроку необхідно актуалізувати знання про основні класи вуглеводнів.
Метод «Мозковий штурм»
• Вуглеводні з одним подвійним зв’язком називаються...
• Вуглеводні з одним потрійним зв’язком називаються...
• Вуглеводні з одинарними зв’язками називаються...
• Загальна формула алканів...
• Загальна формула алкінів...
• Загальна формула алкенів...
• Речовина складу С2Н6 називається...
• Речовина складу С2Н2 називається...
• Речовина складу С5Н12 називається...
• Формула пентіну...
• Формула бутену...
• Формула гексану...
Пропоную учням скласти структурні формули останніх трьох речовин.
На основі повтореного складаємо узагальнюючу схему:
|
|
Алкани |
Алкени |
Алкіни |
|
Загальна формула |
CnH2n+2 |
CnH2n |
CnH2n-2 |
|
Суфікс |
-ан |
-ен |
-ін |
|
Хімічні зв’язки |
одинарні
|
один подвійний
|
один потрійний
|
IІІ. Мотивація навчальної діяльності
Проблемне питання. У чому причини багатоманітності органічних речовин?
Чи може одній формулі відповідати декілька речовин з різною будовою?
ІV. Вивчення нового матеріалу
Лекція вчителя з елементами бесіди.
На дошці записані основні поняття теми:
• Теорія хімічної будови органічних речовин.
• Ізомери.
• Ізомерія.
• Структурна ізомерія.
• Міжнародна номенклатура.
• Радикал.
1. Нагадуємо учням про існування двох різних речовин з формулою С4Н10.
Пропонуємо записати їх структурні формули на дошці й у зошитах. Звертаємо увагу на те, що четвертий атом Карбону приєднаний не з краю, а всередині молекули, так щоб утворилася принципово нова будова молекули.

2. Далі пропонуємо учням об’єднатися в групи по чотири особи та спробувати записати ізомери пентану.
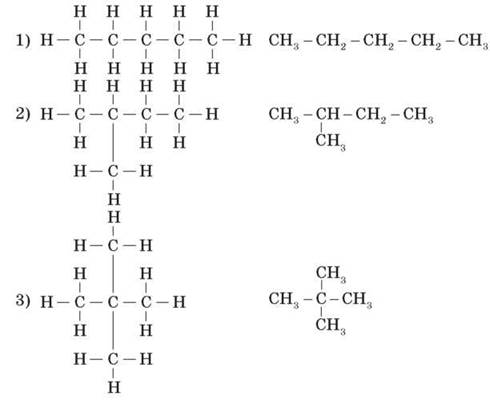
3. Пропонуємо учням скласти кулестрижневі моделі цих речовин. Це надасть дітям змогу зрозуміти порядок побудови молекул ізомерів.
4. Перевіряємо роботу груп. Якщо треба, пояснюємо принципи складання ізомерів:
1) Спочатку будуємо каркас (скелет) молекули;
2) Скорочуємо ланцюг спочатку на один атом Карбону і кріпимо цей атом усередину молекули;
3) Додаємо атоми Гідрогену згідно з валентністю Карбону (ІV);
4) Атоми Карбону об’єднані в ланцюг без відгалужень, то такі вуглеводні називаються нерозгалужені, а якщо атоми Карбону відходять угору, вниз від основного ланцюжка, тобто розгалужуються, то такі вуглеводні називають розгалуженими.
5. Вводимо поняття:
• «ізомерія» — явище існування речовин з однаковою молекулярною формулою, але різним порядком з’єднання атомів у молекулі, а тому й різними властивостями;
• «структурна ізомерія» — вид ізомерії, пов’язаний зі зміною будови карбонового ланцюга;
• «ізомери» — речовини, які мають однакову молекулярну формулу, але різний порядок з’єднання атомів у молекулі, а тому й різні властивості.
6. Даємо поняття про номенклатуру органічних речовин. Пояснюємо.
Кожна речовина має дві назви — тривіальну (ужиткову) та міжнародну (систематичну). Систематичну номенклатуру запропонувала Міжнародна спілка теоретичної та прикладної хімії — ІЮПАК. Правила номенклатури насичених вуглеводнів — алканів (парафінів) — такі:
1) У молекулі вибирають найдовший ланцюг і починають нумерувати його з того боку, де ближче стоїть радикал-замісник. Радикал — це хімічно активна частинка, яка утворюється з молекули насиченого вуглеводню, коли він відщеплює один атом Гідрогену. Наприклад: метан СН4 утворює радикал СН3- — метил, етан С2Н6 утворює радикал С2Н5- — етил, і т. д.
2) Цифрою вказують положення радикала-замісника в ланцюжку. Наприклад, 2-метил означає, що від другого атома Карбону відходить радикал метил СН3-. А якщо однакових радикалів декілька, то цифрою вказують кожний з них (2,3,4-), але перед назвою радикала ставлять префікс — ди-, три-, тетра- і т. д. Наприклад: 2,3,4-триметил — (три радикали СН3-, які відходять від 2, 3 і 4 атома Карбону в основному ланцюзі), 2,3,5,7-тетра (чотири). Отже, префікс, указує скільки однакових радикалів містить молекула.
3) Якщо радикали стоять біля одного й того самого атома Карбону, то цифру вказують двічі. Наприклад, 2,2-диметил, 2,3,3-триметил і т. д.
4) Якщо радикали різні, то називати їх починають за алфавіту: спочатку етил, метил, пропіл тощо.
5) Остаточну назву речовині дають за кількістю атомів Карбону в нумерованому ланцюзі, не забуваючи, що всі алкани мають суфікс -ан.
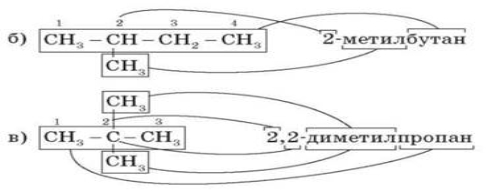
Розглянемо ці правила на ізомерах пентану.
а) СН3-СН2-СН2-СН2-СН3
н-пентан (н — нормальний, нерозгалужений)
V. Узагальнення та закріплення знань
«Творча лабораторія»
Учні продовжують роботу в групах і вчаться називати парафіни.
1) Спробуємо назвати речовину.
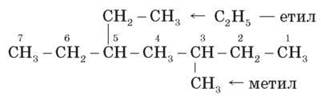
Знайдемо та пронумеруємо найдовший ланцюг з того боку, де ближче радикал. А у нас два радикали на однаковій відстані від обох боків, тому вибираємо той, що простіше, тобто метил, і нумеруємо з його боку, але називати починаємо за алфавітом з радикала етилу. Отже, отримуємо назву:5-етил-3-метилгептан.
2) Назвіть речовини:
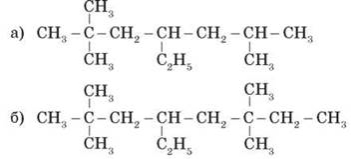
3) Складіть структурну формулу речовин з назвою:
а) 4-етил-3,3-диметилгептан;
б) 3-етил-2,3,5-триметилнонан.
«Бліц – фініш»
Так-ні
1. Більшість органічних сполук тверді, тугоплавкі речовини.
2. Органічні сполуки легкоплавкі, леткі
3. Органічні речовини здебільшого не розчиняються у воді
Закінчіть твердження:
4. Основою органічних сполук є …
5. До органогенних елементів належать….
6. Валентність Карбону в органічних сполуках становить …
7. Теорію будови органічних сполук сформулював ….
8. Ізомери – це речовини з ….
9. При згорянні органічних речовин утворюються ….
10. Властивості органічних речовин залежать від …
11. Знаючи будову речовини можна передбачити її ….
12. Спробуйте порівняти сполуки С2Н6 і С3Н6. Що спільного і відмінного у
них?
VI. Підбиття підсумків уроку
VII. Домашнє завдання
Опрацювати матеріал параграфа, відповісти на запитання
до нього, виконати вправи.


про публікацію авторської розробки
Додати розробку
