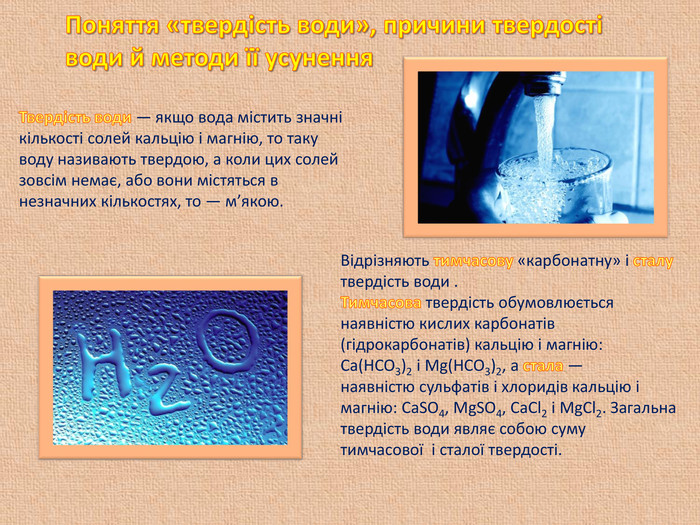
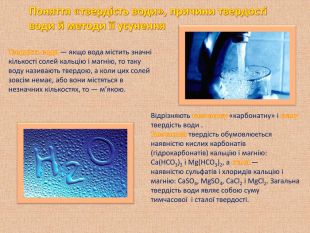
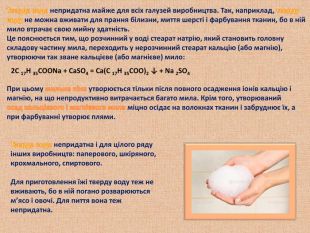
Урок - Презентація " Поняття жорсткість води" 10 клас
Про матеріал
При вивченні лужноземельних металів розглядається питання якості води тому рекомендую використовувати Презентацію ,яку учні виконують під керівництвом вчителя. Виконуючи презентацію учні набувають навички працювати в електронному просторі використовуючи додаткові матеріалами та електроні носії. При захисті своєї роботи учень використовує елементи науково-дослідницького напрямку.
Перегляд файлу
Зміст слайдів
pptx
Оцінка розробки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку