Урок: Хімічні властивості лугів: дія на індикатори, взаємодія з кислотними оксидами, кислотами, солями. Лабораторний дослід № 3: «Взаємодія лугів з кислотами у розчині»
Конспект уроку хімії в 8 класі
Автор: Бондар Катерина Олександрівна
Навчальний заклад: Харківська загальноосвітня школа № 164
Місто Харків
Тема уроку: Хімічні властивості лугів: дія на індикатори, взаємодія з кислотними оксидами, кислотами, солями. Лабораторний дослід № 3: «Взаємодія лугів з кислотами у розчині»
Мета: поглибити знання учнів про основні класи неорганічних сполук на прикладі лугів; закріпити знання про склад і назви основ, розглянути хімічні властивості лугів на прикладі взаємодії з кислотами, оксидами та солями; розвивати навички складати рівняння хімічних реакцій; виховувати самостійність та уважність.
Тип уроку: вивчення нового матеріалу
Обладнання: періодична система хімічних елементів, таблиця розчинності, розчин лугу, індикатор, презентація, комп’ютер.
Хід уроку
І. Організаційний етап
Оберіть смайлик, який відповідає вашому настрою на уроці



ІІ. Активізація опорних знань учнів
Поняття «основи» нам уже відоме. Давайте пригадаємо визначення терміну «основа» та їх загальну формулу.
1. Визначте фізичні властивості розчинних основ, склавши речення.

2. Одна із фізичних властивостей лугів – це розчинність у воді. Розподіліть формули основ за розчинністю на три групи.
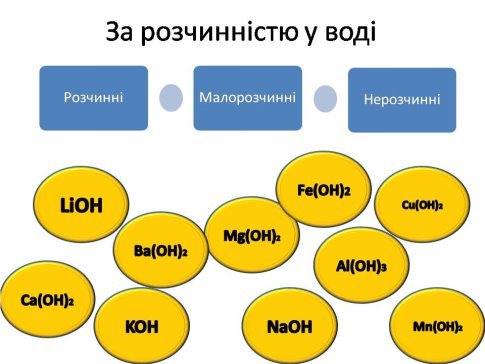
3. Визначте речовину, яка є зайвою в даному переліку і поясніть чому.
А) Al(OH)3, Ca(OH)2, Mn(OH)2
Б) NaOH, Cu(OH)2, LiOH
В) Al(OH)3, Fe(OH)3, Sn(OH)2
ІІІ. Мотивація навчальної діяльності
Розчинні у воді основи – луги, милкі на дотик, невелика їх кількість входить до складу побутових хімікатів, без яких ми не можемо уявити своє життя. А чи не становлять вони небезпеки нашому організму? Для цього потрібно знати властивості цих речовин і правила поводження з ними.
ІV. Оголошення теми і мети уроку
Тема нашого уроку: Хімічні властивості лугів: дія на індикатори, взаємодія з кислотними оксидами, кислотами, солями.
Мета уроку: розглянути лугів на індикатори, взаємодію лугів з кислотними оксидами, кислотами, солями.
V. Вивчення нового матеріалу
1. Дія лугів на індикатори
Для визначення певного класу сполук у хімії ми використовуємо індикатори.
- Пригадайте, що таке індикатори?
- Які індикатори Вам відомі? (Лакмус, фенолфталеїн, метилоранж)
- Як змінювали свій колір індикатори в кислотах? (лакмус – червоний, метилоранж – червоний, фенолфталеїн – не змінював колір)
В кожного з Вас на столі знаходиться розчин лугу натрій гідроксид і індикатори. Перевірте експериментальним шляхом дію індикаторів на луги і запишіть результати в зошит.
Правильність заповнення таблиці перевіримо на слайді.
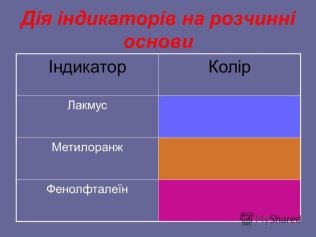
2. Взаємодія з кислотними оксидами
Зараз ми переглянемо відео взаємодії кислотних оксидів з основою і запишемо рівняння реакції.
https://www.youtube.com/watch?v=9OFZHf8WFy0
![]() CO2+ Ca(OH)2 = CaCO3 + H2O
CO2+ Ca(OH)2 = CaCO3 + H2O
Характерною ознакою даної реакції є утворення білого осаду.
Запишіть самостійно рівняння реакції між натрій гідроксидом і скльфур (VI) оксидом.
2NaOH + SO3 = Na2SO4 + H2O
3. Взаємодія лугів з кислотами. Лабораторний дослід № 3.
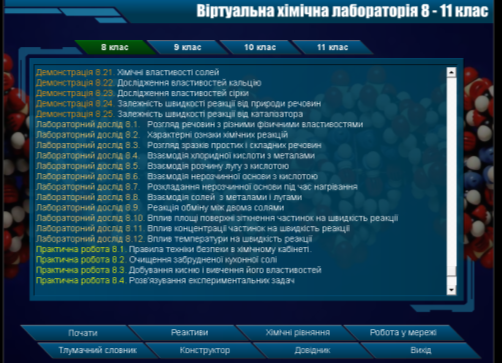
Взаємодію лугів з кислотами ми розглянемо за допомогою «Віртуальної хімічної лабораторії 8-11 класи» .
Лабораторний дослід 8.5. Взаємодія розчину лугу з кислотою.
Реакції взаємодії кислот з лугами називають реакціями нейтралізації. В пробірці з NaOH лужне середовище, що підтверджено розчином фенолфталеїну. HCl має кисле середовище. Внаслідок взаємодії цих речовин утворюється нейтральне середовище, про що свідчить зникнення забарвлення.
4. Взаємодія лугів із солями
Взаємодію лугів з солями ми розглянемо за допомогою «Віртуальної хімічної лабораторії 8-11 класи» .
Лабораторний дослід 8.8. Взаємодія солей з металами і лугами.
Запишіть рівняння хімічної реакції та ознаку, характерну для даної реакції.
VІ. Узагальнення і систематизації знань
1. Миючі засоби для очищення труб та дезінфекції містять в своєму складі речовини на основі лугів. При неправильному використанні таку засоби можуть спричинити опіки. Якими речовинами потрібно надати першу медичну допомогу при опіках лугами, ґрунтуючись на їх хімічних властивостях.
2. Здійсніть перетворення
![]()
![]()
![]()
![]() Li Li2O LiOH Li2S
Li Li2O LiOH Li2S
Li2SO3
3. Закінчіть рівняння реакції. Завдання виконується на швидкість за рядами.
1 ряд
1. Be(OH)2+HCl=
2. СuSO4+NaOH =
3. Ba(OH)2+H2CO3=
4. LiOH + SO3=
5. NaOH + CO2 =
2 ряд
1. Mn(OH)2+HI=
2. СuSO3+LiOH =
3. Ca(OH)2+H2SO3=
4. NaOH + SO2=
5. KOH + CO2 =
3 ряд
1. Mg(OH)2+HF=
2. СuSO4+KOH =
3. Ba(OH)2+H2CO3=
4. KOH + SO2=
5. LiOH + CO2 =
VІІ. Підбиття підсумків уроку
Рефлексія
Сьогодні я дізнався ….
На уроці я навчився ….
Найбільші труднощі у мене викликає….
VІІ. Домашнє завдання
Опрацювати параграф 33, письмово виконати завдання 3,4 на сторінці 180

про публікацію авторської розробки
Додати розробку
