Урок "Класифікація неорганічних сполук, їхні склад і номенклатура. Солі. Основи"
Розроблений конспект уроку розрахований для учнів 8-х класів. Мета уроку: ознайомити учнів зі складом солей та основ, їх назвами; розвивати логічне мислення, пам'ять.
Тема. Класифікація неорганічних сполук, їхні склад і номенклатура. Солі. Основи
Мета: ознайомити учнів зі складом солей та основ, їх назвами; вивчити алгоритм складання назв солей та основ; розвивати логічне мислення, пам’ять, вміння встановлювати причинно-наслідкові зв’язки, розвивати творчі здібності, критичне мислення; виховувати відповідальність, спостережливість, допитливість.
Тип уроку: урок засвоєння нових знань
Обладнання: таблиця, роздатковий матеріал.
Хід уроку
І. Організаційний етап
Вправа : “Психологічна настанова” – “До успіху”
Усміхніться один одному, подумки побажайте успіхів на цілий день. Для того, щоб впоратися на уроці з завданнями, будьте старанними і слухняними. Завдання наші такі, як епіграф уроку:
ЕПІГРАФ:
Не просто слухати, а чути.
Не просто дивитися, а бачити.
Не просто відповідати, а міркувати.
Дружно і плідно працювати.
ІІ. Актуалізація опорних знань
Бліц-опитування
- Які класи складних неорганічних сполук ви знаєте?
- Що таке Оксиди?
- Оксиди поділяються на…
- Що таке кислоти?
- Як поділяються кислоти?
Самостійна робота
За назвами сполук, що знаходяться в хмарині слів скласти формули сполук.

ІІІ. Мотивація навчальної діяльності
Загадка «Що знаходить в коробці?»
У ній знаходиться надзвичайна речовина. Колись її вважали милістю богів, символом миру у східних країнах. Та не така вона вже і мирна! Через неї навіть море може стати мертвим. Обійтися без неї неможливо. Металургія, кераміка, шкіряне взуття, с/г, медицина… (Сіль)
Слово вчителя
До складу миючих засобів (наприклад, для чищення поверхні кухонних плит) входять небезпечні їдкі речовини, наприклад, їдкий натр, їдке калі, які належать до класу – основи.
ІV. Вивчення нового матеріалу
Розповідь учителя
Подивіться уважно на дошку. Що спільного ви побачили?
КCl Na2 CO3 BaSO4 Na2SO3
( На першому місці – метал, на другому – кислотний залишок )
А тепер, самостійно попробуйте дати визначення, що ж таке сіль?
Солі – це складні речовини, утворені атомами металів і кислотними залишками.
Схема назви солей:
Назва металу (валентність, якщо змінна) + назва кислотного залишку.
Завдання: назвати солі, формули яких зображені на дошці.
Основи – це складні речовини, в яких атоми металів сполучені з однією або кількома гідроксильними групами.
Загальна формула основ:
n I де Ме – позначення металу,
Ме(ОН)n n – його валентність.
Назви основ складаються шляхом використання двох слів: перше – назва металу, друге “гідроксид”. Якщо метал має змінну валентність, то її позначають римською цифрою в дужках після назви металу: СuОН – купрум (І) гідроксид, Сu(ОН)2 – купрум (ІІ) гідроксид.
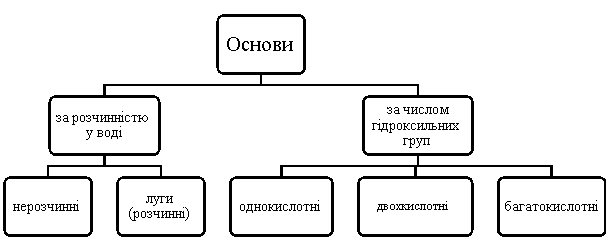
Класифікація основ
V. Узагальнення і систематизація знань
«Хімічна естафета»
- Заповніть пропуски в таблиці (учні по черзі виходять і записують формули біля дошки)
Формули солей
|
Формула кислоти |
К |
Fe(ІІ) |
|
H2SO4 |
К2SO4 |
|
|
HNO3 |
|
Fe(NO3)2 |
|
H3РО4 |
|
|
- Складіть формули основ, утворених металами: Li, Mg, Fe(III), Ni(II). Назвіть їх.
Робота в групах. «Хто швидше»
Завдання виконують всі члени команди в своїх зошитах, спілкуватись і допомагати не забороняється.
Перемагає команда всі члени якої записали правильні відповіді.
1. Виберіть із п’ятого ряду таблиці формули оксидів.
2. Виберіть зі стовпця В усі формули основ.
3. Виберіть із восьмого ряду формули кислот.
4. Зі стовпця Г виберіть формули солей і підкресліть кислотний залишок.
Таблиця
для кожного учня
|
№ з/п |
А |
Б |
В |
Г |
Д |
E |
|
1 |
S |
P |
K2SO3 |
CO |
FeCl2 |
CO2 |
|
2 |
HNO3 |
Li |
Ag2O |
CuSO3 |
H2SO4 |
CaO |
|
3 |
NaCl |
Ca(OH)2 |
Sr(OH)2 |
Na2SіO3 |
Hg |
HgO |
|
4 |
C4H10 |
H2SO3 |
Mg |
FeCl3 |
C6H12O6 |
Al2O3 |
|
5 |
К2O |
Na2O |
ZnO |
BaCl2 |
FeS |
SnO2 |
|
6 |
FeS2 |
Fe |
BaSO4 |
C3H8 |
N2 |
LiOH |
|
7 |
К3РO4 |
MgSO4 |
P2O5 |
Cu(OH)2 |
Rb |
SnF4 |
|
8 |
Вr2 |
Cl2O7 |
NaCl |
HI |
KMnO4 |
H3РO4 |
|
9 |
Fe(OH)3 |
Cr2O3 |
Ca |
PbS |
Mg(OH)2 |
CаСO3 |
|
10 |
LiCl |
K2ZnO2 |
Fe2O3 |
AgCl |
N2O5 |
Cl2 |
|
11 |
HF |
H2S |
NaOH |
O2 |
FeO |
SrSO4 |
|
12 |
ZnS |
Ca3P2 |
Al4C3 |
CH4 |
Mn |
FeO |
V. Підведення підсумків уроку
VІ. Домашнє завдання
Опрацювати §23, виконати завд. 6 (с.132).


про публікацію авторської розробки
Додати розробку
