Урок на тему «Білки: склад і будова.Гідроліз, денатурація, кольорові реакції білків»
Чернівецька загальноосвітня школа №3
Розробка уроку з хімії на тему:
«Білки: склад і будова.Гідроліз, денатурація,
кольорові реакції білків» (9 клас)
Підготувала
Вчитель хімії
Багрій Д.Р.
Чернівці 2018
Тема: Білки: склад і будова. Гідроліз, денатурація, кольорові реакції білків.
Мета:
Навчальна: Формувати поняття про білки як виисокомолекулярні сполуки, їх елементарний і амінокислотний склад; будову і структуру молекул білків. Ознайомити учнів із хімічними властивостями білків.
Розвиваюча: розвивати знання учнів про структуру та властивості білків; розвивати вміння одержувати та обробляти інформацію з різних джерел, уміння порівнювати свої думки, почуття, враження.
Виховна: сприяти формуванню в учнів наукового світогляду.
Обладнання: Періодична система хімічних елементів, набір хімічних реактивів, куряче яйце.
Тип уроку: Вивчення нового матеріалу.
План уроку:
I. Організація класу
ІІ. Актуалізація опорних знань
ІІІ. Мотивація навчальної діяльності
ІV. Вивчення нового матеріалу:
1. Дослідження білків.
2. Будова і склад білків.
3. Властивості білків.
4. Хімічний склад білка.
5. Функції білків.
V. Узагальнення і систематизація знань учнів
VI. Підбиття підсумків уроку
VII. Домашнє завдання
Хід уроку:
І. Організація класу
ІІ. Актуалізація опорних знань
Евристична бесіда:
1. До якого типу сполук належать амінокислоти?
Нітрогеновмісні органічні сполуки
2. Що таке амінокислота?
Це складна органічна сполука до складу молекули якої входить аміногрупа та карбоксильна група.
3. Які властивості проявляють амінокислоти? Чому? До якого класу сполук їх відносять?
Амінокислоти проявляють амфотерні властивості, тому їх відносять до амфотерних сполук. Аміногрупа - основні властивості
Карбоксильна - кислотні властивості.
Амінокислоти проявляють такі самі властивості як і карбонові кислоти, а також взаємодіють з кислотами, лугами, та між собою.
4. Яка амінокислота є найпростішим представником амінокислот?
Амінооцтова кислота або її інша назва гліцин. (Учні роблять запис на дошці молекулярної, структурної та електронної формули сполуки)
5. Як називається зв'язок, який утворюється в результаті реакції амінокислот між собою?
Пептидний або амідний. (Учень записує на дошці взаємодію амінооцтової кислоти з амінооцтовою кислотою і коментує принципи утворення пептидного зв'язку.
ІІІ. Мотивація навчальної діяльності
З якими матеріальними об'єктами пов'язана таємниця життя? Це одне з головних питань, на яке намагалися дати відповідь наука біологія протягом своєї історії. І вже досить давно вчені зрозуміли, що найважливішу роль в усіх життєвих процесах відіграють білки.
Символом початку життя було яйце. Ось чому білок пташинних яєць дав назву всьому класові білків.
Коли в XIX ст. відкрили, що білки - головні компоненти клітин, усі прояви життя почали пов'язувати лише з ними.
Німецький вчений Е. Гекель сказав: "Якщо ви, хіміки створите справжній білок, то він заворушиться!"
Темою нашого уроку будуть "Білки: склад і будова. Гідроліз, денатурація, кольорові реакції білків "
ІV. Вивчення нового матеріалу:
«Життя - це спосіб існування білкових тіл …»
Ф.Енгельс
1. Дослідження білків. (Повідомлення учнів)
2. Будова і склад білків
Молекули білків утворюються у клітині організму з альфа амінокислот (20 амінокислот. Їх ще називають золотими). Вісім із амінокислот (триптофан, лейцин, ізолейцин, лізин метіонін, фенілаланін, треоніт валін ) належить до незамінних - їх людина одержує з їжею, тому що організмом вони не синтезуються.
Білки - це складні високомолекулярні природні сполуки, побудовані із залишків альфа амінокислот,з'єднаних у певній послідовності пептидним зв'язком.
Білки можна розглядати як поліпептиди (дипептиди, трипептиди...), тому що їх молекулярна маса більша за 10000.
За хімічним складом білки поділяють на:
- Прості (протеїни) - гідролізуються до амінокислот
- Складні (протеїди) - при гідролізі утворюють крім амінокислот речовини небілкової природи (вуглеводи, фосфатну кислоту, нуклеїнові кислоти)
Білки мають історичні назви. Наприклад, білок складу (C738H1166O208S2Fe)4 − гемоглобін.
Структура білка (Схема «Структура білків»)
- Первинна;
- Вторинна;
- Третинна;
- Четвертинна.
Первинна − хімічна структура білка, тобто послідовність чергування амінокислотних залишків у поліпептидному ланцюгу даного білка.
Вторинна − форма поліпептидного ланцюга в просторі. Вона може бути ниткоподібною, спіралеподібною та ін. форми .
Третинна − реальна тривимірна конфігурація, утворена складанням вторинних структур (одна глобула).
Третинну структуру можна уявити собі як спіраль, яка згорнута, у свою чергу спіраллю!!!
Четвертинна − поєднання в просторі кількох макромолекул (кілька глобул).
Глобулярні білки − білки, які мають форму клубка.
3. Властивості білків
1) Денатурація − руйнування вторинної і третинної структури білка під дією нагрівання, радіації, сильних кислот, лугів, сильного струшування.
2) Кольорові реакції на білок:
- Біуретова реакція
Готуємо осад Купрум (ІІ) гідроксид: до розчину Калій гідроксиду додаємо кілька крапель розчину Купрум (ІІ) сульфату
KOH + Cu(OH)2↓ + K2SO4
синій осад
До розчину білка додаємо кілька крапель Купрум (ІІ) гідроксиду і спостерігаємо характерне фіолетове забарвлення.
- Ксантопротеїнова реакція
Внаслідок дії на білок концентрованої нітратної кислоти виникає жовте забарвлення, яке при додаванні лугу змінюється на оранжеве. Ця реакція доводить, що білок містить у своєму складі бензольне кільце.
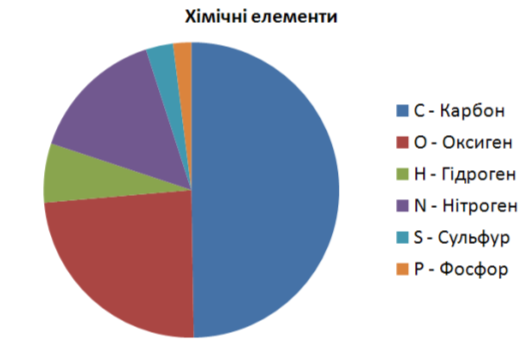
4. Хімічний склад білка
Білки містять наступні хімічні елементи: C, H, O, N, S, P, Fe.
Масова частка елементів:
С − 50% - 55%
О − 19% - 24%
Н − 6,5% - 7,3%
N − 15% - 19%
S − 0,3% - 2,5%
P − 0,1% - 2%
Функції білків:
- Структурна;
- Транспортна;
- Ферментативна;
- Захисна;
- Рецепторна;
- Регуляторна, гормональна;
- Скорочувальна;
- Запасаюча;
- Енергетична.
V. Узагальненя і систематизація учнів
- Біологічна роль амінокислот та білків
- Амінокислоти − це будівельний матеріал для білків.
- Знання властивостей білків допомагає зберегти життя людям: у разі отруєння солями важких металів вживають молоко, білки якого зв’язують ці сполуки.
- Білки їжі не засвоюються організмом, спочатку вони розщеплюються до амінокислот, а потім амінокислоти всмоктуються в кров, а вже з нею переноситься до клітин, де організм синтезує білки.
- Організм людини не здатний синтезувати амінокислоти тому для поповнення їх запасу потрібно вживати білкову їжу.
Можемо зробити висновок, що життя напевно не було б можливим без білків.
- Заслуховуються виступи учнів.
VI. Підбиття підсумків уроку
Проблемне питання: «Вегетаріанство − ви за чи проти? »
«Я завжди говорив і не втомлююся
повторювати,
що світ не міг би існувати,
якби був так просто влаштований»
Гете
VI. Домашнє завдання
Опрацювати матеріал параграфа в підручнику.
Творче завдання:
Дати відповідь на запитання « Чи можна повністю замінити білкову їжу на вуглеводну? Чому? »


про публікацію авторської розробки
Додати розробку
