Урок "Оксиди: склад, поняття, класифікація."
Класифікація неорганічних сполук, їхній склад і номенклатура.
Оксиди.
Навчальна мета: формувати знання про класифікацію неорганічних сполук, поняття про склад основних класів складних неорганічних сполук та їх номенклатуру на прикладі оксидів; формувати вміння складати формули оксидів та давати їм назви .
Розвивальна мета: розвивати хімічну мову.
Виховна мета: формувати інформаційну компетентність; виховувати інтерес до вивчення хімії.
Базові поняття і терміни: прості і складні речовини, метали, неметали, органічні та неорганічні речовини, оксиди.
Тип уроку: вивчення нового матеріалу.
Хід уроку.
І. Організаційний момент. Вітання з учнями. Створення робочого настрою.
ІІ. Мотивація і актуалізація опорних знань.
Сьогодні ми починаємо вивчати нову тему: «Основні класи неорганічних сполук» де ознайомимося з класифікацією складних речовин, дозволить дізнатися, як склад і будова речовин впливають на їхні властивості, способи одержання і застосування.
Бесіда.
1.На які групи можна розподілити всі речовини? ( органічні та неорганічні)
2.На які дві групи поділяються речовини за складом? . (Прості, складні.)
Як визначити, що речовина проста чи складна?(За кількістю елементів у складі. Складається з одного типу атомів – проста, два і більше – складна.)
3.На які групи поділяють прості речовини ? (Метали й неметали.).
4. Розподіліть прості речовини, що написані на дошці на метали й неметали.
( використовуємо періодичну таблицю)
ІІІ. Вивчення нового матеріалу.
Вам дано перелік сполук: NaOH, HCl, CaBr2 , H2SO4 , Ca(OH)2 , CuO, H3PO4 , H2S , ZnO, Fe(OH)2 , Fe(OH)3 , K2SO4 , CuCO3 , CO2 , Mg(OH)2 , AlPO4 , SO3 , Ba(NO3)2 , H2SiO3 , Na2O. Виписати окремо речовини, які мають подібний склад.
Класифікація неорганічних сполук
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() Прості Складні
Прості Складні
Метали Неметали Оксиди Кислоти Основи Солі
Оксиди — це складні речовини, утворені двома елементами, один із яких є Оксиген. Нам відомо, що елементи поділяються на метали і неметали, враховуючи те, який елемент (метал чи неметал) утворив оксид, можна дати найпростішу класифікацію оксидів.
![]()
![]()
![]() Оксиди
Оксиди
Оксиди металів Оксиди неметалів
(основні) (кислотні)
Амфотерні оксиди
( це оксиди, що проявляють властивості
кислотних і основних оксидів)
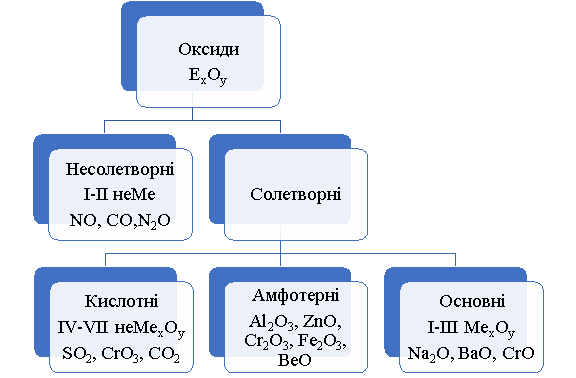
СОЛЕТВОРНИЙ ОКСИД – оксид, якому відповідає певна кислота, або сіль.
НЕСОЛЕТВОРНИЙ ОКСИД – оксид, який не утворює відповідної кислоти, або солі.Не виявляють ні кислотних, ні основних властивостей, тобто не утворюють солей, кількість таких оксидів незначна. Приклади: N2O (нітроген (І) оксид), CO(карбон (ІІ) оксид) та ін.
КИСЛОТНИЙ ОКСИД – оксид, якому відповідає певна кислота (декілька кислот). Кислотні оксиди здатні реагувати з основними оксидами та основами. Оксиди неметалічних елементів та оксиди металічних елементів у вищому ступені окиснення, яким відповідають кислоти. Приклади: SO2 (сульфур (IV) оксид), CrO3 (хром (VI) оксид), CO2 (карбон (IV) оксид).
ОСНОВНИЙ ОКСИД – оксид, якому відповідає певна основа. Основні оксиди здатні реагувати з кислотними оксидами та кислотами. Оксиди металічних елементів у ступені окиснення +1, +2, яким відповідають основи. Приклади: Na2O (натрій оксид), BaO (барій оксид), CrO(хром (ІІ) оксид).
АМФОТЕРНИЙ ОКСИД – оксид, який здатний взаємодіяти як з кислотами, так і з основами. Оксиди металічних елементів, яким відповідають амфотерні гідроксиди; здатні виявляти як кислотні, так і основні властивості. Приклади: Al2O3 (алюміній оксид), ZnO (цинк оксид), Cr2O3 (хром (ІІІ) оксид), Fe2O3 (ферум (ІІІ) оксид), BeO (берилій оксид).
Назви оксидів за сучасною українською номенклатурою складаються за схемою:
Назва елемента (валентність, якщо вона змінна) + Оксид.
Наприклад:
Назва елемента Валентність (взята в дужки) Оксид. Формула
нітроген (ІІ) оксид NО
нітроген (ІІІ) оксид N2О3
нітроген (V) оксид N2O5
Демонстрація. Зразки оксидів. Фізичні властивості

Прийом «Мікрофон»
По ланцюжку складіть формули оксидів написаних на карточці:
- бор оксид
- ферум (ІІI) оксид
- кальцій оксид
- фосфор (III) оксид
- сульфур (VI) оксид
- натрій оксид
- фосфор (V) оксид
- калій оксид
- карбон (ІІ)( оксид
Індивідуальне завдання (3-5 хв)
- Виписати з періодичної системи формули вищих оксидів Алюмінію,Гідрогену, Натрію, Карбону, Магнію, Силіцію, Сульфуру, Барію. Фосфору,
- Складіть формули оксидів за їх назвою: калій оксид, літій оксид, барій оксид, нітроген (І) оксид, хлор (VІІ) оксид, сульфур (VІ) оксид.
- Скласти хімічні пазли -формули оксидів.
Підсумок уроку, оцінювання, повідомлення домашнього завдання
Параграф підручника
Із переліку формул випишіть окремо основні і кислотні оксиди: СО2, NaNO3, NO2, MgSO4, SiO2, Na2O, А12O3, СuО, LiОН, Н2CO3, ZnО, Р2O5, HCl, FеО, H2O, Zn(ОH)2


про публікацію авторської розробки
Додати розробку
