Урок "Основи, склад, назви, класиіфікація, фізичні властивості основ"
Мета: сформувати поняття про основи, визначити особливості їх складу та назв, ознайомитися з класифікацією основ та їх розчинності, розглянути фізичні властивості основ, сформувати вміння складати формули основ, давати їм назви та вміння виявляти луги за допомогою індикаторів; розвивати вміння творчо використовувати отриману інформацію.
Урок з хімії для 8 класу
Тема. Основи.
Мета: сформувати поняття про основи, визначити особливості їх складу та назв, ознайомитися з класифікацією основ та їх розчинності, розглянути фізичні властивості основ, сформувати вміння складати формули основ, давати їм назви та вміння виявляти луги за допомогою індикаторів; розвивати вміння творчо використовувати отриману інформацію.
Обладнання: комп’ютер, мультимедійний проектор або телевізор, таблиці «Основні класи неорганічних сполук», «Розчинності кислот, основ, солей», Періодична система хімічних елементів Д.І. Менделєєва.
Тип уроку: комбінований.
ХІД УРОКУ
І. Організаційний етап.
Привітання з учнями, перевірка готовності до уроку.
ІІ. Перевірка домашнього завдання
Хімічний диктант (вчитель диктує назву кислот – учні пишуть формулу)
HCl, H2SO4, H2S, HBr, H3PO4, HNO3, HClO4, H2CO3, H2SO3, HF, HNO2, H3BO3.
ІІІ. Актуалізація опорних знань
- Бесіда
- Назвіть основні класи неорганічних сполук.
- Дайте визначення оксидів.
- Дайте визначення кислот.
- Які елементи – металічні чи неметалічні – входять до складу кислот?
- Мотивація
Кислоти входять до складу деяких миючих засобів. Але є миючі засоби, до складу яких входять не менш небезпечні їдкі речовини, ніж кислоти. На етикетках таких засобів написано, що до їх складу входять, наприклад їдкий натр, їдке калі. Ці речовини є протилежними за своїми властивостями до кислот.
Як ви думаєте, до якого класу неорганічних сполук вони можуть належати?
Учитель оголошує тему уроку і просить учнів сформувати мету уроку.
V. Вивчення нового матеріалу
Розповідь вчителя. Основи є хімічними протилежностями кислот. Неорганічні основи ще називають гідроксидами, тому що вони складаються з двох частин: атомів металічних елементів і гідроксигруп ОН.
Демонстрація. Зразки основ (демонстрація завдяки телевізору або мультимедійного проектора).
Учні за зразками основ описують їх фізичні властивості.
Основи – складні речовини, що складаються з атома металічного елемента і однією або декількох гідроксигруп ОН.
Загальна формула основ (![]() . Гідроксигрупа є одновалентною, тому число гідроксигруп у складі основи дорівнює валентності металічного елемента. Назви гідроксидам давати досить просто: назва складається з двох слів: перше – назва металічного елемента, а друге – слово «гідроксид». Якщо металічний елемент може виявляти декілька валентностей, то в назві також вказується його валентність римськими цифрами в дужках.
. Гідроксигрупа є одновалентною, тому число гідроксигруп у складі основи дорівнює валентності металічного елемента. Назви гідроксидам давати досить просто: назва складається з двох слів: перше – назва металічного елемента, а друге – слово «гідроксид». Якщо металічний елемент може виявляти декілька валентностей, то в назві також вказується його валентність римськими цифрами в дужках.
Тренувальні вправи. Вчитель пише на дошці формули гідроксидів, учні повинні дати їм назви, а потім навпаки: вчитель пише або вимовляє назви гідроксидів, а учні складають формули.
Класифікація основ (схему можна проектувати на екрані/телевізорі і коментують).
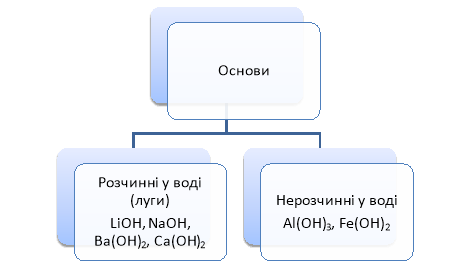
Так само як і кислоти, луги можна виявити у водних розчинах за допомогою індикаторів (вчитель демонструю на екрані/телевізорі «Дія розчинів лугів на індикатори»).
V. Закріплення вивченого матеріалу
1. Підкресліть основи в наведеному переліку: KOH, CaCO3, Ca(OH)2, H2CO3, K2S, NaOH, HF, Ba(OH)2, SO2, H2PO4, Al(OH)3, LiOH, Zn(OH)2, H2SO4, Fe(OH)3, HBr.
2. Складіть формули гідроксидів Калію, Магнію, Стануму(ІІ), Цину, Алюмінію, Купруму(ІІ), Плюмбуму(ІV), Барію. Формули лугів підкресліть.
VI. Домашнє завдання
Опрацювати відповідний параграф.


про публікацію авторської розробки
Додати розробку
