Урок "Основні класи неорганічних сполук . Оксиди, їх склад, назви. Класифікація оксидів"
Мета :
- сформувати уявлення про загальну класифікацію неорганічних речовин на підставі отриманих раніше знань про прості та сладні речовини ;
- розширити знання учнів про класифікацію неорганічних речовин на прикладі оксидів та їх класифікацію за складом ;
- ознайомити учнів із сучасною українською номенклатурою оксидів;
- формувати вміння й навички використання номенклатури на прикладі назв оксидів ;
- розвивати навички учнів у складанні формул бінарних сполук на прикладі складання формул оксидів ;
- продовжувати формувати науковий світогляд на основі знань теорії про хімічні властивості основ і перенесення їх на практику ;
- вдосконалювати хімічну мову учнів;
- формувати активну пізнавальну діяльність учнів на уроці;
- розвивати соціальну та комунікативну компетентність, логічне мислення , пам`ять, увагу, уяву, самостійність, аналізувати та робити висновки ;
- виховувати інтерес до вивчення хімії, як природничої науки.
Методи : фронтальне опитування, розповідь з елементами бесіди,
робота з ЛОСом , робота групами.
Тип уроку : засвоєння нових знань, умінь та навичок.
Обладнання : Періодична система хімічних елементів Д.І.Менделєєва, хімічні реактиви ,картки , ноутбук.
Хід уроку
І. Актуалізація опорних знань учнів
1. На які два класи поділяються всі хімічні елементи ? Наведіть приклади з
Періодична система хімічних елементів Д.І.Менделєєва .
( Учні відповідають: на прості та складні).
2. Прості речовини поділяють ще на дві групи. Які саме?
( Учні відповідають: метали та неметали, наводять приклади).
3. На які дві групи можна розподілити складні речовини ?
( органічні та неорганічні ) . ( слайд 1 )
4. Складних чи простих речовин більше в природі?
( Учні відповідають: складних, тому що вони складаються з атомів кількох
хімічних елементів).
ІІ. Мотивація навчально-пізнавальної діяльності учнів. Оголошення теми, мети, завдань уроку
За якою ознакою можна класифікувати речовини ? ( слайд 2 )
( за складом, будовою, застосуванням, властивостями )
Тема уроку : Основні класи неорганічних сполук . Оксиди, їх склад, назви.
Класифікація оксидів. ( слайд 3 )
Сьогодні ми розпочинаємо вивчати нову тему. Виходячи з теми , давайте визначимо завдання уроку . ( слайд 4 )
- Як класифікують неорганічні речовини ?
- Як склад і будова впливає на властивості , способи одержання й застосування ?
- Які сполуки називаються оксидами ?
- Який склад і як утворюються назви оксидів ?
- Як класифікують оксиди ?
ІІІ. Матеріал нової теми
Із курсу 7 класу, вам відомо, що всі речовини поділяються на органічні ( сполуки Карбону ) та неорганічні. Галузь хімічної науки, яка вивчає неорганічні речовини називається неорганічною хімією.
Відомі сотні тисяч неорганічних речовин. Щоб в них розібратися вчені розділили ці речовини на групи , які назвали класами.
За складом неорганічні сполуки поділяються на чотири класи : оксиди, основи, кислоти, солі. ( слайд 5 )
Згадайте, де ми зустрічалися з оксидами в процесі вивчення хімії ?
У 7 класі під час вивчення простої речовини кисню. Унаслідок згоряння різних речовин у кисні утворюється продукт їх взаємодії – оксид. Тому невід`ємна частина будь-якого оксиду – Оксиген .
Оксиди – це складні речовини, що складаються з атомів двох хімічних елементів, один з яких є Оксиген .
( наводимо приклади )
Основи - це складні речовини, що складаються, з атом металів та однієї чи кількох гідроксильних груп – ОН.
( NaOH, Mg(OH)2, LiOH , Са(HO)2 )
Кислоти - це складні речовини, що складаються, з атомів Гідрогену й кислотних залишків.
( H2SO4 , H2S, НNO3 )
Солі - це складні речовини, що складаються, з атом металів і кислотних залишків.
( LiCl , NaCl , K3PO4 )
Які найпоширені оксиди ви знаєте ? ( слайд 6 )
Що ж таке оксиди ? ( слайд 7 )
Як класифікують оксиди ? ( слайд 8 )
Оксиди металів Оксиди неметалів Амфотерні Несолетворні
(основні) (кислотні) Аl2O3 СО
СаО SO2 ТiO2 N2O
СuО СO2 ZnO N0
К2O Мn2O7
Назви оксидів за сучасною українською номенклатурою
( слайд 9 )
- Назва елемента + Оксид.
- CaO – кальцій оксид ;
- Na2O – натрій оксид ;
- Al2O3 - алюміній оксид.
- Назва елемента + (валентність, якщо вона змінна) + Оксид.
- Р205 - фосфор (V) оксид ;
- CO – карбон ( ІІ ) оксид ;
- SO3 - сульфур(VI) оксид.
Виконаємо ланцюжок оксидів : ( слайд 10 )
- барій оксид -
- фосфор (ІІІ) оксид-
- ферум (II) оксид -
- сульфур (IV) оксид -
- калій оксид -
- сульфур(VI) оксид -
- ферум (IIІ) оксид –
- натрій оксид –
- силіцій оксид -
ІV. Узагальнення та систематизація вивченого матеріалу
І. Робота з таблицею : ( слайд 11 )
|
№ |
А |
Б |
В |
Г |
Д |
Е |
|
1 |
S |
P |
K2SO4 |
CO |
FeCl2 |
CO2 |
|
2 |
НNO3 |
Li |
Ag2О |
CuSO4 |
H2SO4 |
CaO |
|
3 |
NaCl |
Са(HO)2 |
Sr(OH)2 |
Na2SiO3 |
Hg |
HgO |
|
4 |
C4H10 |
H2SO3 |
Mg |
FeCl3 |
C6H12O6 |
Al2O3 |
|
5 |
K2O |
Na2O |
ZnO |
BaCl2 |
FeS |
SnO2 |
|
6 |
FeS 2 |
Fe |
BaSO3 |
C3H8 |
N2 |
LiOH |
|
7 |
K3PO4 |
MgSO4 |
Р205 |
Cu(OH)2 |
Rb |
SnF4 |
|
8 |
Br2 |
Cl2O7 |
NaCl |
HI |
KMnO4 |
H3PO4 |
|
9 |
Fe(OH)2 |
Cr2O3 |
Ca |
PbS |
Mg(OH)2 |
CaCO3 |
|
10 |
LiCl |
K2ZnO2 |
Fe2O3 |
AgCl |
N2O5 |
Cl2 |
|
11 |
HF |
H2S |
NaOH |
O2 |
FeO |
SrSO4 |
|
12 |
ZnS |
Ca3P2 |
Al4C3 |
CH4 |
Mn |
Fe2O3 |
1. Виберіть із 5 ряду таблиці формули оксидів.
2. Виберіть із стовпця В усі формули основ.
3. Виберіть із 8 ряду формули кислот.
4. Виберіть із стовпця Г формули солей.
ІІ. Заповнити таблицю : ( слайд 12 )
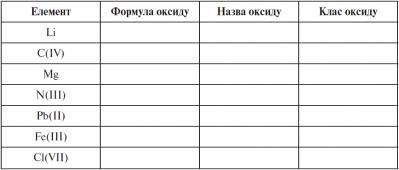
ІІІ. Задачі :
1. Яку масу сульфур(VI) оксиду можна одержати з сульфур(IV) оксиду і 5,6 л
кисню (н. у.)?
2. Магній 4,8 г спалили в атмосфері кисню. Яка маса магній оксиду утворилася ?
V. Висновок
Чи ми виконали завдання, що ставили перед собою ? ( слайд 14 )
VІ. Підсумок уроку. Оголошення домашнього завдання ( слайд 15)
- Прочитати параграф 5 .
- Завдання 46 , 47 , 49, 54 ( письмово )
- Творче завдання : скласти формули оксидів елементів ІII періоду з вищою
валентністю, дати назви, зазначити клас.


про публікацію авторської розробки
Додати розробку
