Урок-практикум "Окисно-відновні реакції"
nvk13kovel
![]() Комунальний заклад «Навчально-виховний комплекс
Комунальний заклад «Навчально-виховний комплекс
«Загальноосвітня школа І-ІІІ ст.. № 13 – колегіум» м. Ковеля»
Окисно-відновні реакції
Поняття про метод електронного балансу
(урок – практикум)
8 клас
Підготувала:
Палашевська Мирослава
Петрівна
вчитель хімії
Тема: Окисно-відновні реакції.
Поняття про метод електронного балансу.
Мета: Розповісти про метод електронного балансу.
Навчити виконувати рівняння реакцій за допомогою опорної схеми.
Виховувати інтерес до хімії.
Обладнання: картки із завданнями для експерименту, вугілля, залізний цвях, розчин CuSO4, HCl, мідна спіраль, Zn гранули, поршок KClO3
Хід уроку.
- Актуалізація опорних знань (робота з картками в групах).
|
Атом та йон елемента |
Символ атома та йона елемента |
Заряд ядра атома |
Загальна к-сть електронів в атомі та йоні |
К-сть електронів на зовнішньому шарі в атомі та йоні |
Ступінь окиснення |
|
Фосфор |
Р, Р+5, P+3, P-3 |
+15 |
15, 10, 12, 18 |
5, -, 2, 8 |
0, +3, +5, -3 |
- Хрестики-нулики.
Виграшний шлях складає однаковий ступінь окиснення
І варіант ІІ варіант
Нітрогену Сульфуру
|
KNO3 |
Mg3N2 |
NH3 |
|
|
|
|
|
N2 |
HNO3 |
NaNO3 |
|
|
H2SO3 |
Na2SO4 |
|
ZnSO4 |
|
S |
|
H2S |
SO2 |
|
- Дослід: Mg+H2SO4→MgSO4+H2
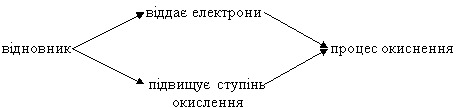 4. Використання опорної схеми:
4. Використання опорної схеми:
![]()
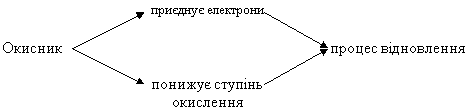
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
5. Закріплення матеріалу
Робота в групах
І група. Спалити вугілля
С+О2→СО2
ІІ група. Занурити Fe цвях у розчин CuSO4
Fe+CuSO4→FeSO4+Cu
ІІІ група. Cu cпіраль помістити у полум”я спиртівки
2Cu+O2→2CuO
IV група. Zn гранули помістити у розчин HCl
Zn+2HCl→ZnCl2+H2
V група. KCIO3 розкласти при нагріванні
KCIO3→KCI+O2
а) провести експеримент;
б) записати рівняння реакції;
в) скласти електронний баланс, вказати окисник, відновник.
6. Робота з картками.
Закінчити електронний процес
а) ![]()
б) ![]()
в) ![]()
г) ![]()
7. Підсумок уроку
а) питання для закріплення матеріалу по 6 пункті.
б) оцінювання учнів.
в) повідомлення домашнього завдання


про публікацію авторської розробки
Додати розробку
