Урок "Реакції сполучення, розкладу, обміну, заміщення".
Тема: Реакції сполучення, розкладу, обміну, заміщення.
Мета:
навчальна: узагальнити й систематизувати знання учнів про типи хімічних реакцій за складом вихідних та кінцевих речовин;
розвивальна: формувати навички розпізнавання типів реакцій теоретично - за рівняннями реакції, експериментально - за ознаками хімічних реакцій, розвивати навички і вміння складати рівняння хімічних реакцій, розвивати логічне мислення учнів, навички самостійної пізнавальної діяльності; продовжувати формувати здоров'язберігаючу компетентність, комунікативну й інформаційну компетентності.
виховна: сприяти формуванню наукового світогляду учнів; виховувати вміння спостерігати явища аналізувати їх, встановлювати причинно-наслідкові зв'язки й робити висновки. формувати здоров'язберігаючу компетентність.
Медіапрезентація додається.
Тип уроку: комбінований урок (узагальнення вивченого матеріалу й набуття нових знань); формування компетентностей. Методи: словесні ( бесіда, розповідь); наочні ( використання проектора,
або мультимедійної дошки); практичні ( проведення дослідів); інтерактивні
(«Хімічна розминка», «Вірю – не вірю», «Сортувальник», «Слідство ведуть хіміки», «Впізнай реакцію», «Так чи ні»).
Форми роботи: розповідь вчителя, фронтальне опитування, демонстраційний експеримент, складання схеми, індивідуальна робота з картками, мультимедійною дошкою, самостійна робота, проблемно-пошукова, робота в парах.
Обладнання: періодична система хімічних елементів, таблиця розчинності, ряд активності металів, мультимедійна презентація до уроку, картки зі схемою, картки із завданнями для самостійної роботи.
Реактиви: залізні пластини, купрум (ІІ) сульфат, натрій гідроксид.
Очікувані результати:
Знати: класифікацію хімічних реакцій за кількістю та складом реагентів і продуктів.
Вміти: розрізняти реакції сполучення, розкладу, заміщення,обміну.
Розуміти: відмінності між даними типами реакцій.
Епіграф уроку:
Те, що я чую, я забуваю.
Те, що я бачу, я пам’ятаю.
Те, що я роблю, я розумію.
Коли я чую, бачу,
Обговорюю і роблю –
Я набуваю знань і навичок.
Конфуцій
Хід уроку
І. Організаційний етап
Учитель. Для успіху на уроці нам потрібен ваш хороший настрій. Тому подивіться на сусіда по парті, усміхніться один одному та побажайте всього доброго.
ІI. Рефлексія
Перш ніж розпочати заняття , давайте з'ясуємо з яким настроєм ви сьогодні прийшли.
У кожного з вас на столі є картки різних кольорів. Подумайте і підніміть картку того кольору , який зараз найбільше імпонує вашому настрою:
- рожевий - добрий настрій;
- жовтий - поганий настрій;
- зелений – нейтральний.
Таким чином всі готові до активної взаємодії, тож нас чекає плідна робота.
ІІІ. Мотивація навчальної діяльності.
Стародавня легенда розповідає, що цариця Клеопатра , яка була відома не тільки своєю красою, а ще й освіченістю, виграла оригінальне парі, з'ївши дорогоцінний «сніданок», який коштував 100 000 сестерцій.
Ось як це описано в книзі Генрі Хаггарда «Клеопатра»: «…Вона вийняла з вуха одну з тих величезних перлин і опустила перлину в оцет. Запанувала тиша, вражені гості, завмерши спостерігали, як незрівнянна перлина повільно розчиняється у міцному оцті. Від неї не залишилось і сліду, і тоді Клеопатра підняла келих, покрутила його і випила весь до останньої краплі».
Що сталося з перлиною? До якого типу можна віднести цю хімічну реакцію?
Щоб відповісти на ці питання здійснимо класифікацію хімічних реакцій.
Відкрийте, будь ласка, зошити, запишіть число та тему над якою будемо працювати «Класифікація хімічних реакцій за кількістю і складом реагентів та продуктів реакцій: реакції сполучення, розкладу, заміщення, обміну»
Мета нашого уроку:
Ознайомитись з ознаками класифікації хімічних реакцій.
Навчитись розрізняти реакції сполучення, розкладу, заміщення, обміну.
Вміти наводити приклади вивчених типів хімічних реакцій.
ІV. Актуалізація опорних знань
- Хімічна розминка
1) Хімічні реакції – це
- явища, під час яких одні речовини перетворюються на інші.
2) Ознаки хімічних реакцій, це…
- зміна кольору;
- поява, зникнення чи зміна запаху;
- виділення газу;
- утворення або зникнення осаду;
- виділення чи поглинання теплоти;
- поява полум’я.
3) Реакція сполучення – це…
реакція, внаслідок якої з двох і більше речовин утворюється одна.
4) Реакція між простою і складною речовинами, під час якої атоми простої речовини заміщують атоми (йони) у складній речовині, називається…
реакцією заміщення.
5) Реакція розкладу – це…
реакція, внаслідок якої з однієї складної речовини утворюються дві та більше речовин.
6) Реакція між двома складними речовинами, під час якої вони обмінюються своїми складовими частинами, це…
реакція обміну.
- Бесіда
Які класифікації хімічних реакцій ви знаєте? Заповніть пусті місця у схемі (схема на мультимедійній дошці)
Класифікації хімічних реакцій
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()




Встановити, яке твердження правильне, а яке ні:
Вправа на інтерактивній дошці
- Схема А + В = АВ відповідає реакції сполучення.
- Схема АВ = А + В відповідає реакції розкладу.
- Схема А + ВС = АС + В відповідає реакції обміну.
- Схема А В + СД = АД + СВ відповідає реакції заміщення.
- У реакції розкладу бере участь одна складна речовина.
- У реакції сполучення можуть брати участь тільки прості речовини.
- У реакції обміну беруть участь дві речовини, з яких одна проста, а інша - складна.
- Реакція взаємодії металу з неметалом є реакцією сполучення.
- Реакція взаємодії металу з кислотою є реакцією заміщення.
- Вивчення нового матеріалу.
Ми пригадали вивчений матеріал. А зараз, дайте відповідь на запитання
Проблемне питання
За якою ознакою розрізняють реакції сполучення, розкладу, заміщення, обміну?
Щоб відповісти на це запитання виконаємо експериментальну частину.
Експериментальна частина
Перш ніж розпочати досліди, варто пригадати правила техніки безпеки:
1) Категорично заборонено брати речовини руками, пробувати їх на смак.
2) Заборонено нахилятися над посудом з реактивами, не вдихати парів речовин.
3) При попаданні на шкіру кислоти пошкоджене місце необхідно промити великою кількістю води, потім уражену ділянку шкіри обробити 5% розчином питної соди.
4) При попаданні на шкіру лугу необхідно промити уражену ділянку водою, потім 4% розчином оцтової кислоти, або 2% розчином борної кислоти.
5) Після виконання дослідів ретельно помийте руки з милом.
Зараз увага на екран:
- Реакції сполучення - хімічні реакції, в результаті яких із двох або кількох речовин утворюється одна нова складна речовина.
демонстрація відеофрагмента
Учень пише рівняння на дошці
4P + 5O2 → 2P2O5
Ознаки реакції: виділення густого білого диму.
- Реакції розкладу - хімічні реакції, в результаті яких із однієї складної речовини утворюється дві чи більше нових речовин.
Дослід. Хімічна загадка – що відбувається?
демонстрація відеофрагмента
Спостерігаємо розклад амоній дихромату:
(NH4)2Cr2O7 → Cr2O3 + N2↑ + 4H2O
Оранжевий зелений
Ознаки реакції: виділення тепла і світла
Питання класу:
- Про який вулкан - національну гордість і символ держави йде мова у японській ліричній мініатюрі – хоку Моцуо Басьо:
Туман і мряка заступають…
Та все одно: не одвести очей.
( Фудзіяма)
- Правда чи неправда, що на території України є вулкани?
( Правда, оскільки на Керченському півострові є 18 грязьових вулканів.)
Подивимося реакцію заміщення
- Реакції заміщення – хімічні реакції між простою і складною речовинами, під час яких атоми простої речовини заміщують атоми одного з елементів у складній речовині, утворюючи нову просту і нову складну речовини.
Проблемне питання класу:
А чи відомо вам, що розчин мідного купоросу успішно використовують у садівництві, але за умови, що розприскувач буде пластмасовий і не матиме залізних частин. Поясніть чому?(Щоб пояснити, давайте подивимось дослід)
Fe + CuSO4 → FeSO4 + Cu↓
Ознаки реакції: випадає осад міді.
Цікаве підґрунтя цієї реакції
Розповідь учня
Досить цікаве історичне підґрунтя цієї реакції. Один із семи чудес світу — Родоський колос. У III ст. до н. е. була споруджена статуя в честь бога Геліоса на острові Родос. Хоча творіння грандіозне й унікальне, проте через сім десятиліть після невеликого землетрусу завалилося. Причиною руйнування став не землетрус, а контактна корозія, адже в бронзову оболонку статуї вмонтували залізні каркаси, а ще сприяв окисно-відновному процесу вологий морський клімат. Залізо витіснило мідь з її сполуки як активний метал.
Тепер попрацюємо в парах
Зібратися разом – це початок, Триматися разом – це прогрес, Працювати разом – це успіх. Г. Форд
- Реакції обміну - хімічні реакції, під час яких дві речовини обмінюються своїми складовими частинками, утворюючи дві нові речовини.
CuSO4 + 2NaOH = Cu(OH)2↓+ Na2SO4; (виконують всі учні)
Ознаки реакції: випадає осад блакитного кольору.
Розповідь учня
Мідний купорос — речовина, що продається в господарських магазинах. ЇЇ використовують малярі для протравлювання стін перед білінням; садівники, городники для попередження хвороб сільськогосподарських рослин, для ветеринарної дезінфекції в акваріумах. Мідний купорос — це сині, красиві кристали, які хіміки називають «купрум сульфат пентагідрат».
VІ. Творче застосування знань, умінь, навичок
Саме зараз ми розширимо свої знання про типи хімічних реакцій в залежності від кількості реагентів і продуктів реакції.
Вправи на інтерактивній дошці
1) Вправа « Впізнай реакцію»
Установіть відповідність між рівнянням реакції та типом хімічної реакції:
Рівняння реакцій: Тип реакцій:
1. 2НCl + Mg = MgCl2 + H2↑; А.Сполучення ( 2, 5 )
2. 2Fe + 3Cl2 = 2FeCl3; Б. Розкладу ( 6 )
3. CuSO4 + 2NaOH = Cu(OH)2↓+ Na2SO4; В. Заміщення ( 1, 4 )
4. Zn + H2SO4 = ZnSO4 + H2↑; Г. Обміну ( 3 )
5. 4Al + 3O2 = 2Al2O3;
6. CaCO3 = CaO + CO2↑.
2) До якого типу реакцій можна віднести реакції, що подані схемами, послідовно з'єднуючи букви, що є відповідями ви отримаєте назву хімічного елемента.
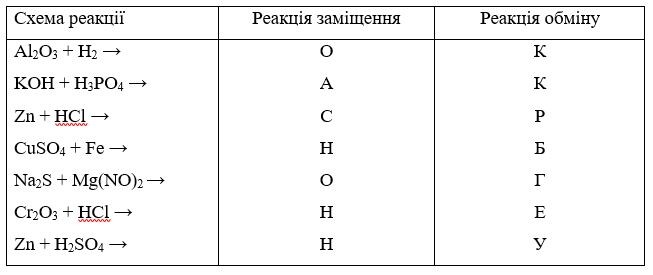
ОКСИГЕН
3) Художнику доручили ілюструвати підручник хімії для дев’ятикласників. Хімічні реакції розкладу, сполучення, заміщення, обміну він зобразив у такий спосіб, який ви можете спостерігати на слайді. Оцініть, чи правильно художник змоделював хімічні реакції різних типів.
- Учитель: На початку уроку було поставлено питання
Клеопатра розчинила в бокалі з оцтом свою коштовну перлину. До якого типу віднесемо дану реакцію?
Розповідь учня
Перли складаються переважно з кальцій карбонату СаСО3 і тому легко розчиняються в кислотах (оцет це розчин органічної оцтової кислоти). Напій, який коштував 100000 сестерцій, являв собою розчин кальцій ацетату.
СаСО3 + 2СН3СООН = (СН3СОО)2 Са + СО2↑ + H2O
Дві складні речовини в результаті реакції обмінюються своїми складовими. Це реакція обміну.
Висновок ( роблять діти)
Сьогодні на уроці ми:
- ознайомились з ознаками класифікації хімічних реакцій
- навчились розпізнавати реакції сполучення, розкладу, заміщення, обміну теоретично - за рівняннями реакцій, та експериментально – за ознаками хімічних реакцій.
VII. Самостійна робота
А зараз, щоб ви мене переконали, що тему уроку засвоїли, пропоную виконати декілька завдань. ( на виконання … хв.)
……………………………………………………………………………………
VIIІ. Підсумок уроку
Учитель.
IХ. Рефлексія
Наш урок добігає кінця, і зараз ми з вами з’ясуємо, чи змінився ваш настрій наприкінці уроку. Підніміть, будь ласка, картки, які відображають ваш настрій на цей момент:
- рожева - добрий настрій;
- жовта - поганий настрій;
- зелена– нейтральний.
Залишіть їх собі на згадку.
Х. Метод «Прес»
Закінчіть речення
На уроці я
- навчився
- дізнався
- зрозумів
ХI. Домашнє завдання
Опрацювати: §13
Вправи № 98, 100,103*
Творче завдання: скласти кросворд із словами, що зустрічаються в темі «Типи хімічних реакцій»
ХІІ. Виставлення оцінок
Вчитель
Стосунки між людьми можна порівняти з хімічними реакціями. Існують реакції сполучення, обміну, заміщення та розкладу. Найнебезпечніший вид стосунків – реакція розкладу. Тож, бажаю нам єдності і мирного неба над головою.
|
ВАРІАНТ № 1 1. (1,5 бала) Оборотня реакція – це:
а) утворення амоніаку 2. (1,5 бала) Рівняння реакції обміну:
а) CaO + SiO2 = CaSiO3 3. (1,5 бала) По данній лівій частині рівняння CuO + H2SO4 = … відновіть його праву частину.
а) CuSO4 + H2O 4. (1,5 бала) З кількох простих або складних речовин утворюється одна більш складніша речовина в реакції:
а) заміщення 5. (2 бала) Розставте коефіцієнти в схемах і вкажіть типи хімічних реакций:
а) Li + O2 6. (3 бала) Відновіть пропущений запис і вкажіть тип хімічної реакції:
а) ? + 2 HCl = FeCl2 + H2
|
ВАРІАНТ № 2 1. (1,5 бала) Необоротня реакція – це:
а) горіння свічки 2. (1,5 бала) Рівняння реакції розпаду:
а) CaO + SiO2 = CaSiO3 3.( 1,5 бала) По даній правій частині рівняння … = CuCl2 + 2 H2O відновіть його ліву частину.
а) Cu + 2 HCl 4. (1,5 бала) З однієї складної речовини утворюється дві або більше нових речовин в реакції:
а) заміщення 5. (2 бала) Розставте коефіцієнти в схемах і вкажіть типи хімічних реакций:
а) CuO + HCl 6. (3 бала) Відновіть пропущений запис і вкажіть тип хімічної реакції:
а) Fe2O3 + 3 H2 = ? + 3 H2O
|
|
ВАРІАНТ № 3 1. (1,5 бала) Оборотнє явище –це:
а) випаровування води 2. (1,5 бала) Вкажіть рівняння реакції заміщення:
а) BaO + H2O = Ba(OH)2 3. (1,5 бала) По данній лівій частині рівняння ZnO + 2 HCl =… відновіть його праву частину.
а) ZnCl2 + H2O 4. (1,5 бала) З однієї складної речовини утворюється дві або більше нових речовин в реакції:
а) заміщення 5. (2 бала) Розставте коефіцієнти в схемах і вкажіть типи хімічних реакций:
а) Fe2O3 + HCl 6. (3 бала) Відновіть пропущений запис і вкажіть тип хімічної реакції
а) ? + H2SO4 = ZnSO4 + H2
|
ВАРІАНТ № 4 1. (1,5 бала) Необоротнє явище – це:
а) плавлення олова 2. (1,5 бала) Вкажіть рівняння реакції сполучення:
а) N2 + O2 = 2 NO 3. . (1,5 бала) По лівій частині рівняння Zn(OH)2 + 2 HCl = … відновіть його праву частину рівняння:
а) ZnCl2 + H2
4. (1,5 бала) З двох складних речовин утворюється дві нових складних речовин в реакції: а) заміщення 5. (2 бала) Розставте коефіцієнти в схемах і вкажіть типи хімічних реакцій:
а) Al2O3 + H2SO4 6. (3 бала) Відновіть пропущений запис і вкажіть тип хімічної реакції:
а) Mg + 2 HCl = ? + H2
|
Перевірка (взаємоперевірка).
|
Вариант 1 |
|
Вариант 2 |
|
А 1. А |
|
А. 1. А |
|
2. Б |
|
2. В |
|
3. А |
|
3. Б |
|
4. Г |
|
4. В |
|
Б. 5. 4 Li + O2 = 2 Li2 O-сполучення |
|
Б. 5. CuO + 2 HCl = CuCl2 + H2O -обміну |
|
Fe2O3 + 2 Al = Al2O3 + 2 Fe –заміщення |
|
2 NH3 = N2 + 3 H2 – розпаду |
|
6. Fe + 2 HCl = FeCl2 + H2 заміщення |
|
6. Fe2O3 + 3 H2=2 Fe + 3 H2O заміщення |
|
2 Al + 3 Cl2 = 2 AlCl3 – сполучення |
|
Zn + 2 HCl = ZnCl2 + H2-заміщення |
|
Вариант 3 |
|
Вариант 4 |
|
А. 1. А |
|
А. 1. Б |
|
2. Б |
|
2. А |
|
3. А |
|
3. В |
|
4. В |
|
4. Б |
|
Б. 5. Fe2O3 + 6 HCl = 2 FeCl3 + 3 H2O обміну |
|
Б. 5. Al2O3 + 3 H2SO4 = Al2(SO4)2 + 3 H2O обміну |
|
2 NO + O2 = 2 NO2 - сполучення |
|
H2 + Cl2 = 2 HCl - сполучення |
|
6. Zn + H2SO4 = ZnSO4 + H2-заміщення |
|
6. Mg + 2 HCl = MgCl2 + H2-заміщення |
|
4 Al + 3 O2 = 2 Al2O3- сполучення |
|
2 Na + Cl2 = 2 NaCl - сполучення |
1


про публікацію авторської розробки
Додати розробку
