Урок з хімії 9 кл. "Використання якісних реакцій" за технологією " Перевернуте навчання"
Матеріал складається з трьох частин:
1. Презентація для дітей, що містить основний матеріал для самостійного вивчення з теми уроку.
2. Розробка уроку
3. Презентація до уроку.
Урок розроблений за технологією "Перевернуте навчання" із застосуванням групових форм роботи.
- для учнів Використання якісних реакцій.pptx pptx
- до уроку.pptx pptx
- .docx docx
Урок з хімії із застосування технології «Перевернуте навчання»
9 клас
Тема. Застосування якісних реакцій.
Мета. 1. На основі сформованої предметної компетентності щодо якісних реакцій у неорганічній хімії продовжити вдосконалювати й застосовувати набуті знання під час розв’язування практичних завдань, показати прийоми оптимального пошуку розв’язання поставленої задачі;
2. Розвивати логічне мислення, уважність, здатність аналізувати проблему та знаходити раціональний спосіб її вирішення;
3. Виховувати толерантність, вміння спілкуватися, працювати в групах.
Тип уроку: узагальнення та коригування знань.
Форма уроку: урок - експеримент
Предметна компетентність: на основі сформованої предметної компетентності щодо якісних раціональний спосіб її вирішення. Реакцій у неорганічній хімії продовжувати вдосконалювати і застосовувати набуті знання під час розв’язування практичних завдань, показати прийоми оптимального пошуку розв’язання поставленої проблеми, розвивати логічне мислення, уважність, здатність аналізувати проблему та знаходити раціональний спосіб її вирішення.
Ключові компетентності: спілкування державною мовою, математична компетентність, основні компетентності у природничих науках і технологіях, екологічна грамотність і здорове життя, інформаційно-цифрова компетентність, уміння вчитися впродовж життя, ініціативність .
Навчальне обладнання: реактиви, пробірки, штатив, блок завдань на розпізнавання неорганічних речовин за допомогою якісних реакцій.
ХІД УРОКУ
І. Організаційний етап
Хвилинка лакмусової перевірки настрою учасників уроку
ІІ. Мотиваційний етап.
Перегляд відеоролика про групову роботу
ІІІ. Повідомлення теми та мети уроку
ІV. Перевірка здобутих знань
Хімічний диктант із самоперевіркою
- Якісним реактивом на іон Н+ є:
а/ лакмус; б/ВаCl2; в/ фенолфталеїн; г/AgNO3.
- Якісним реактивом іон ОН-є:
а/ СаСl2; б/ВаCl2; в/ фенолфталеїн; г/AgNO3.
- Якісним реактивом на іон СО32-є:
а/ лакмус; б/НCl; в/ фенолфталеїн; г/AgNO3.
- Які з іонів не можуть одночасно існувати у розчині:
а/ Н+ і Cl- ; б/Ва2+ і Cl- ; в/ К+ і ОН-; г/Ag+ і Cl-.
- Ознакою хімічної реакції під час визначення сульфат-іону є
а/ поява білого осаду барій сульфату:
б/ поява жовтого осаду аргентум хлориду;
в/ поява блакитного осаду купрум(ІІ) сульфату;
в/ поява червоного розчину лакмусу.
-
Ознакою хімічної реакції під час визначення ортофосфат – іону буде:
а/ поява білого осаду барій сульфату:
б/ поява жовтого осаду аргентум ортофосфату;
в/ поява блакитного осаду купрум(ІІ) сульфату;
в/ поява малинового розчину фенолфталеїну .
ХВИЛИНА САМОПЕРЕВІРКИ.
Б. Відповіді:
- А; 2. В; 3. Б; 4. Г; 5. А; 6. Б
ІV. Узагальнення та коригування знань
ХВИЛИНКА БЖД
- Проблемне завдання Готуючись до уроку я хвилювалася і переплутала пробірки з речовинами. Як за допомогою одного реактиву розпізнати речовини?
В трьох пробірках містяться сполуки:
- NaOH + лакмус = синій колір
- HCl + лакмус = червоний колір
- NaCl + лакмус = колір не змінився.
- У пробірках під номерами 1, 2 та 3 містяться речовини: хлоридна кислота, натрій сульфат; натрій хлорид. Визначте кожну речовину дослідним шляхом. Складіть рівняння реакцій у молекулярному та йонному вигляді.
- Відеопитання.
- Сторінка дослідника:
І варіант: складіть план визначення якісного складу речовини, проведіть реакції та запишіть відповідні рівняння реакцій в молекулярному та йонному вигляді. Купрум (ІІ) хлорид
ІІ варіант: складіть план визначення речовин та проведіть відповідні рівняння реакцій. Складіть рівняння в молекулярному та йонному вигляді. Натрій карбонат; натрій гідроксид, натрій сульфат.
ІІІ варіант: складіть план визначення якісного складу речовини, проведіть реакції та запишіть відповідні рівняння реакцій в молекулярному та йонному вигляді. Барій хлорид.
ІVваріант. Проведіть реакцію, скорочене йонне рівняння якої:
2Н++ СО32--= СО2+ Н2О
Рефлесія.
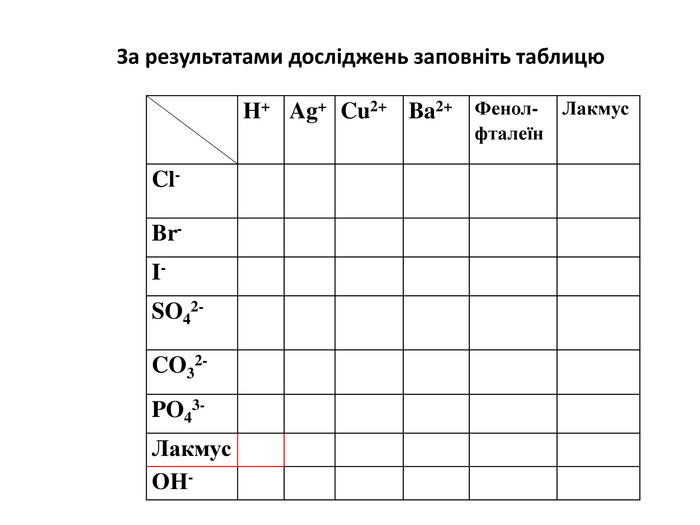
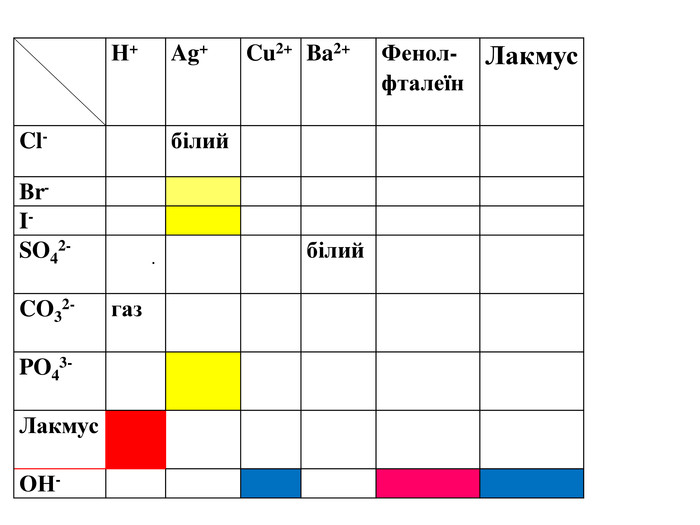
Вчитель. Отже, на сьогоднішньому уроці ми узагальнили знання з якісного визначення деяких йонів. Я пропоную вам заповнити кольорову таблицю, яка є у кожної групи.
|
|
Н+ |
Ag+ |
Cu2+ |
Ba2+ |
Фенол- фталеїн |
Лакмус |
|
Cl- |
|
білий |
|
|
|
|
|
Br- |
|
|
|
|
|
|
|
I- |
|
|
|
|
|
|
|
SO42- |
|
|
|
білий |
|
|
|
CO32- |
газ |
|
|
|
|
|
|
PO43- |
|
|
|
|
|
|
|
Лакмус |
|
|
|
|
|
|
|
ОН- |
|
|
|
|
|
|
Вчитель: отже, ми вже володіємо навичками проведення якісних реакцій, але де ж у побуті ми можемо застосувати свої знання?
Учні. 1. Якщо, наприклад, переплутали сіль, цукор та харчову соду, визначити її можливо дією оцту.
- Визначення кислотного чи лужного середовища у мийних засобів при алергічних реакціях шкіри;
- Визначення рН ґрунту під час вирощування квітів чи с/г культур
Заповнити таблицю та виставити зароблені бали:
|
№ завдання |
Тестування (0,5 бали за питання, всього 3 б.) |
Завдання 1. (проблемне) (макс. 2 б) |
Завдання 2 (макс. 2 б) |
Завдання 3 (відеопитання) (макс. 2 б) |
Завдання 4 (сторінка дослідника) (макс. 2 б) |
|
Бали |
|
|
|
|
|
|
Всього балів |
|
||||
Домашнє завдання:
- Для всіх : повторити п 13, виконати вправу 162 на стор.82.
- Для бажаючих: скласти 3 тестові питання з теми « Якісні реакції»


про публікацію авторської розробки
Додати розробку