Урок з розділу "Хімічний склад клітини" та біологічні молекули
розробки уроків біології для 9 класу з теми «Хімічний склад клітин та біологічні молекули.
Запропоновані уроки допоможуть систематизувати й узагальнити знання учнів та сприятимуть розвитку в них ключових предметних компетентностей.
Використання інтерактивних, інформаційно-комунікаційних технологій, ігрових моментів, різних способів перевірки знань (бесіди, розв'язування кросвордів, ребусів, анаграм, виконання тестових завдань), використання різноманітного дидактичного матеріалу (картки, таблиці, слайди) зроблять уроки цікавими і захопливими. Розроблено тестовий контроль знань у форматі ЗНО.
1
Урок 1.
Тема. Вода та її основні фізико-хімічні властивості
Мета: сприяти засвоєнню в учнів знань про особливості будови молекули води; розкрити роль води для життєдіяльності живих організмів; формувати комунікативну компетентність - вміння продуктивно працювати в групі, прислухатися до думки кожного, культуру спілкування, толерантність; інформаційну компетентність - розвивати вміння самостійно аналізувати та відбирати необхідну інформацію.
Обладнання й матеріали: таблиці, схеми.
Базові поняття й терміни: неорганічні сполуки, вода, гідрофільність, гідрофобність, амфіфільність.
Тип уроку: засвоєння нових знань.
Хід уроку
І. Організаційна частина
Привітання учнів, перевірка присутніх і стану готовності учнів до уроку
Створення робочих груп
Учні класу працюють у трьох групах: «Біологи», «Хіміки», «Географи».
ІІ. Актуалізація опорних знань
Біологічний диктант
- Назвіть імена вчених, які незалежно один від одного запропонували термін «біологія» … (Ж. Б. Ламарк і Г. Р. Тревіранус).
- У якому році з’явився термін біологія? (у 1802 році) .
3. Англійський учений, який уперше описав клітинну будову рослинних тканин … (Р. Гук) .
4. Голландський учений, який уперше побачив живі одноклітинні організми під мікроскопом … (Антоні ван Левен Гук).
5. Учений, який тривалий час працював в Україні, відкрив існування вірусів… (Д. Й. Івановський).
6. Український учений, засновник імунології та мікробіології, лауреат Нобелівської премії … (І. І. Мечников).
7. Учений, який створив учення про ноосферу, як новий стан біосфери … (В.І. Вернадський).
8.Учений, який у XVIII ст. уперше запропонував наукову систематику живих організмів … (К. Лінней).
9. Укажіть, на якому рівні організації живої матерії здійснюється кругообіг речовин між біотичною та абіотичною частинами природної системи … (біогеоценотичний).
10. Метод біологічних досліджень, що ґрунтується на спостереженні, широко використовували вчені давнини під час збирання фактичного матеріалу. У сучасних умовах за його допомогою відкривають нові види організмів … (порівняльно-описовий).
11. На якому рівні організації живого відбуваються хімічні реакції, збереження та зміни спадкової інформації … (молекулярному).
ІІІ. Мотивація навчальної діяльності
Проблемне запитання:
Про цю речовину А. де Сент-Екзюпері говорив: «Не можна сказати, що ти необхідна для життя, ти саме життя…Ти найбільше багатство у світі».
Яку речовину мав на увазі письменник?
Вода посідає особливе місце в історії нашої планети. Немає природного тіла – мінералу, гірської породи, живого організму, яке б не містило води. Нею просочена й охоплена вся земна речовина.
Проблемне запитання:
- Чому вода має першочергове значення у клітинах живих організмів?
- Чи залежить кількість води від вікових категорій людей?
Повідомлення теми та завдання уроку
Девіз уроку:
«Учітесь, читайте
І чужому навчайтесь
Й свого не цурайтесь»
Т. Г. Шевченко
ІV. Вивчення нового матеріалу
- Робота в групах
Завдання
Використовуючи текст підручника і додаткову літературу, охарактеризуйте воду.
- Презентація результатів роботи груп
Група «Географи» Вода – найпоширеніша речовина на Землі
Вода – найпоширеніша речовина на Землі. Вона покриває близько ¾ поверхні земної кулі: озера, річки, моря, океани. У великій кількості вода міститься в атмосфері повітря – пара, туман, хмари та в земній корі у вигляді підземних вод.
Вода на земній кулі існує у трьох агрегатних станах: твердому, рідкому та газоподібному.
Кожен живий організм у своєму складі містить воду. Вміст води в організмах тварин складає 60-70%, а у деяких (наприклад, медузи) – до 98%. Рослинні організми: огірок містить 90% води, картопля 77%. Тому впевнено можна сказати, що вода і життя на нашій планеті нероздільні.
Група «Біологи» Вода в людському організмі
Людський організм містить близько 65% води. Тобто, якщо маса тіла людини становить 65 кг, то з них 42 кг припадає на воду.
Між різними органами і тканинами людини вода розподілена нерівномірно: найбільше її в крові та нирках – 82 - 83%, клітини головного мозку та цитоплазма клітини містить 80% води, м’язи та печінка – близько 76%, жирова тканина – 30%, кістки – 20%, зубна емаль – 0,3%. Втрата понад 20% води – смертельно небезпечна для людини. Вода утворює основу внутрішнього середовища живих організмів ( цитоплазми одноклітинних тварин, крові, лімфи, соків рослин тощо).
Вміст води в тілі людини залежить від віку: у новонароджених він становить 75-80 %, у період завершення росту – 65-70 %, а в людей похилого віку – лише 55-60%.
Група «Хіміки» Джерела води в організмі людини
Протягом доби людині необхідно 2,5 л води. Приблизно 1 л входить до складу їжі, більше літра – у вигляді води, чаю, кави і близько 0,5 л утворюється в самому організмі.
- 100 г жиру – 107 мл води;
- 100 г вуглеводів – 55 мл води;
- 100 г білка – 41 мл води.
Виводиться із організму:
- з сечею – 1,4 л;
- з калом – 0,2 л;
- випаровування з поверхні легень – 0,4 л;
- з потом – 0,5 л.
У нормальних умовах в організмі підтримується динамічна рівновага водного балансу. Якщо води виділяється з організму більше, ніж надходить, виникає відчуття спраги.
- Будова молекули води
Розповідь учителя
Відповісти на запитання:
- Між якими атомами виникає ковалентний зв’язок?
- Що таке електронегативність і як ця властивість атома впливає на утворення диполя?
- За рахунок яких сил відбувається утворення водневих зв’язків між молекулами води?
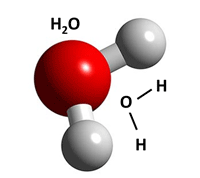 Молекула води складається з одного атома Оксигену і двох атомів Гідрогену. Кожен атом Гідрогену утримується біля атома Оксигену ковалентним зв’язком. Електричний заряд в середині молекули розподілений нерівномірно: в атомів Гідрогену переважає позитивний заряд, а в Оксигену – негативний. Завдяки цьому кожна молекула води – це диполь.
Молекула води складається з одного атома Оксигену і двох атомів Гідрогену. Кожен атом Гідрогену утримується біля атома Оксигену ковалентним зв’язком. Електричний заряд в середині молекули розподілений нерівномірно: в атомів Гідрогену переважає позитивний заряд, а в Оксигену – негативний. Завдяки цьому кожна молекула води – це диполь.
 Диполь – це молекула, що має однакові за величиною і протилежні за знаком заряди, які розташовані один від одного на відстані.
Диполь – це молекула, що має однакові за величиною і протилежні за знаком заряди, які розташовані один від одного на відстані.
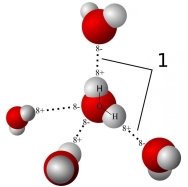 Тому молекула води може приєднуватися до різних молекул і ділянок молекул, що несуть заряд. В наслідок цього утворюються гідрати. За рахунок сил електростатичної взаємодії між негативним зарядом атома Оксигену однієї молекули та позитивним зарядом атома Гідрогену іншої виникає водневий зв’язок, який у 15-20 разів слабший за ковалентний. Коли вода перебуває у рідкому стані, її молекули безперервно рухаються і водневі зв’язки постійно то розриваються, то виникають знову. Тому вода має відносно високу температуру кипіння, плавлення й пароутворення.
Тому молекула води може приєднуватися до різних молекул і ділянок молекул, що несуть заряд. В наслідок цього утворюються гідрати. За рахунок сил електростатичної взаємодії між негативним зарядом атома Оксигену однієї молекули та позитивним зарядом атома Гідрогену іншої виникає водневий зв’язок, який у 15-20 разів слабший за ковалентний. Коли вода перебуває у рідкому стані, її молекули безперервно рухаються і водневі зв’язки постійно то розриваються, то виникають знову. Тому вода має відносно високу температуру кипіння, плавлення й пароутворення.
Молекулам води притаманна здатність до іонізації, коли вони розщеплюються на протон H+ і гідроксид-іон OH-. При цьому між молекулами води та йонами встановлюється динамічна рівновага:
![]() H2О → H+ +OH–
H2О → H+ +OH–
Від концентрації йонів Гідрогену, яку оцінюють за водневим показником рН, залежать структурні особливості та активність макромолекул.
Нейтральній реакції розчину відповідає рН 7,0. Якщо його значення нижче, реакція розчину кисла, вище – лужна. У різних частинах організму різні значення водневого показника. Наприклад, у людини та ссавців ферменти підшлункового соку активні у лужному середовищі, шлункового – в кислому середовищі.
2. Властивості води
Пояснення вчителя
Вода – найкращий розчинник із відомих речовин. Усі речовини поділяють на такі, що здатні добре розчинятися у воді – гідрофільні, або полярні, та нерозчинні у воді – гідрофобні, або неполярні.
Запитання до учнів.
Які сполуки належать до гідрофільних, а які – до гідрофобних?
(Гідрофільні або полярні – кухонна сіль, глюкоза, фруктоза, кислоти, луги, спирти, тростинний цукор).
(Гідрофобні – майже всі ліпіди, каучук, полісахариди вони розчиняються у неполярних органічних розчинниках – хлороформі, бензолі).
Існують й амфіфільні речовини – одна частина молекули цих сполук виявляє гідрофобні властивості, інша – гідрофільні. Наприклад, фосфоліпіди (сполуки ліпідів із залишками фосфорної кислоти), ліпопротеїди (сполуки ліпідів з білками).
3. Функції води
Самостійна робота з підручником
Завдання
За допомогою підручника з’ясувати основні функції води
1. Метаболічна функція:
- універсальний розчинник;
- середовище де відбуваються хімічні реакції;
- кінцевий продукт багатьох біохімічних реакцій.
2. Транспортна функція:
- вода головний компонент транспортної системи рослин і внутрішнього середовища людини і тварин.
3. Терморегуляторна:
- забезпечення рівномірного розподілу тепла організмі;
- під час транспірації у рослин та потовиділення у тварин охолоджує організм.
4. Вода як реагент:
- із води у світловий фазі фотосинтезу утворюється оксиген і гідроген.
5. Механічна функція води:
- створення пружності клітини (тургор).
6. Захисна:
- рідина, що заповнює порожнину суглобів, полегшує ковзання суглобових поверхонь, зменшуючи тертя між ними;
- вода живить хрящ, що вкриває суглобові поверхні.
Повідомлення учнів
Питна вода та вимоги до її якості. Методи очищення води
V. Узагальнення і систематизація навчального матеріалу
1. Бесіда за запитаннями
- Які особливості будови молекули води зумовили її специфічні властивості?
- Які властивості води є найважливішими для живих організмів?
2. Творче завдання
Складіть сенкан з теми «Вода»
Вода
Джерельна, ендогенна
Тече, замерзає, випаровується
Середовище життя
Рідина
3. Гра « Екологічне лото»
Учням роздають листочки із записами частин прислів’я. Під час гри вони повинні скласти повне прислів’я.
1 ряд 2 ряд
Де верба… - доброту віддячить.
Ліс і вода … - який поріг, така й господиня
Хліб – батько … - там і вода.
Криниця з водою … - вода – мати.
Хто в воді … - брат і сестра.
Яка криниця такий і господар … - той в добрі.
Вода за … - що людина з розумом.
- Робота з картками
Позначте знаком «+» правильні твердження про воду, знаком «-» – неправильні.
- А. H2О має низьку теплоємність і водночас низьку для рідин теплопровідність (-).
- Б. H2О безпосередньо не бере участі в хімічних реакціях, що протікають в організмах (-).
- В. H2О найкращий розчинник серед загальновідомих рідин ( +).
- Г. Вода є середовищем для життя багатьох організмів (+).
- Д. Є основним засобом пересування речовин по організму (-).
- Е. H2О практично не стискається, що дуже важливо для надання форми соковитим плодам (-).
- Є. H2О - основне середовище, де протікають хімічні реакції (+).
VІ. Домашнє завдання
- Вивчити відповідний параграф підручника.
- Дати відповідь на запитання:
Коли спека поєднується з високою вологістю повітря при дуже важкому фізичному навантаженні втрата води з потом може досягати близько 10 літрів на добу. При такому сильному потовиділенні організм зазнає лиха. Чому це відбувається і в чому виражається?
VIІ. Підсумок уроку
Вправа «Мікрофон»
- Що ви взяли для себе з уроку, чи потрібне це вам у майбутньому?
Урок 2.
Тема. Неорганічні сполуки
Мета: формувати в учнів знання про елементарний склад живих організмів; з’ясувати роль макро- мікро- та ультрамікроелементів; розвивати психічні процеси: мовлення, увагу, слухове зосередження інформації, креативне та логічне мислення, вміння порівнювати склад хімічних елементів у живій та неживій природі (інформаційна компетентність); виховувати бережливе ставлення до свого здоров’я і здоров’я оточуючих, як найвищої цінності (здоров’язберігаюча компетентність).
Обладнання й матеріали: таблиці, схеми.
Базові поняття й терміни: біохімія, організм, органогенні елементи, макроелементи, мікроелементи, ультрамікроелементи, органогенні елементи.
Тип уроку: засвоєння нових знань.
Хід уроку
І. Організаційна частина
Нумо, діти, підведіться!
Всі приємно посміхніться.
Продзвенів уже дзвінок,
 Починаємо урок!
Починаємо урок!
Прикріплюю на дошці смайлик «Радість» і бажаю всім учням гарного настрою, легкого засвоєння теми.
А зараз усміхніться один одному. Подумки побажайте успіхів на цілий день. Для того, щоб впоратися на уроці з завданнями, будьте старанними і слухняними.
Щоб не просто слухали, а чули.
Щоб не просто дивилися, а бачили.
Щоб не просто відповідали, а міркували.
Дружно і плідно працювали.
ІІ. Актуалізація опорних знань
Графічний диктант
1. Молекула води – диполь.
2. Вода забезпечує створення пружності клітин (тургор).
3. В основі будови молекули води лежить ковалентний полярний зв’язок.
4. Гідрофільні речовини не розчиняються у воді.
5. Структурована вода в клітині займає 4-5% від загальної кількості води в клітині.
6. Вода не здатна забезпечувати рівномірного розподілу тепла в організмі.
7. Гідрофобні речовини – розчинні у воді.
8. Віль вода займає в живій системі 94-95% вмісту.
9. Теплопровідність – здатність води поглинати тепло за незначних змін своєї температури.
10. Гідроліз – розщеплення органічних сполук з приєднанням до місця розриву йонів молекул води.
11. Молекулам води притаманна здатність до іонізації.
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
|
+ |
+ |
+ |
- |
+ |
- |
- |
+ |
- |
+ |
+ |
ІІІ. Мотивація навчальної діяльності
- Скільки хімічних елементів включають до складу періодичної системи?
- Які хімічні елементи частіше за все трапляються під час вивчення неорганічної хімії?
- Які хімічні елементи трапляються в навколишньому середовищі частіше за все?
Проблемні запитання
- На основі чого ґрунтується єдність живої та неживої природи?
- Чи існує єдність хімічного складу організмів?
Повідомлення теми та завдання уроку
ІV. Вивчення нового матеріалу
- Розповідь учителя
Запитання до учнів
Які науки вивчають елементний склад живих організмів?
(Відповідь. Біохімія – наука, що вивчає хімічний склад живих організмів, перетворення хімічних речовин, їхній перерозподіл в організмі та функції).
Хімічні елементи у живих організмах утворюють два класи сполук – неорганічні та органічні
У складі живих організмів близько 70 елементів, але лише 24 з них мають цілком встановлене значення і зустрічаються в живих організмах постійно.
У неживій природі більше 100 хімічних елементів. Разом з тим у живих організмах не виявлено жодного з хімічних елементів, якого б не було у неживій природі.
Деякі організми інтенсивно накопичують певні хімічні елементи:
|
Живі організми |
Хімічні елементи |
|
Бурі водорості |
Йод |
|
Хвощ польовий, злаки |
Силіцій, кремній |
|
Ряска |
Радій |
|
Хребетні тварини |
Ферум |
|
Молюски, ракоподібні |
Купрум |
|
Бактерії |
Манган |
- Пояснення вчителя
Якщо в неживих об’єктах на нашій планеті за кількістю атомів найбільш поширеними є О (63%), Si (21,2%), Al (6,5%), Na (2,4%), Fe (1,9%), Ca (1,9%), то в живих організмах перші місця за вмістом займають H (64%), О (25,6%), С (7,5%), N (1,25%), P (0,24%), S (0,06%).
Живі організми і нежива природа утворені одними й тими самими хімічними елементами.
- Про що це свідчить? (Відповідь. Про єдність живої і неживої природи).
За хімічним складом клітини різних організмів можуть суттєво відрізнятися одна від одної, але елементи, що входять до їхнього складу, однакові.
- Про що це свідчить? (Відповідь. Про єдність усіх живих організмів, про єдність елементарного складу органічного світу планети).
За вмістом у живих організмах хімічні елементи можна поділити на три групи: макроелементи, мікроелементи, ультрамікроелементи.
Заповнення таблиці разом з учнями
Хімічні елементи живих організмів
|
Хімічні елементи у складі живих організмів |
||
|
Макроелементи |
Мікроелементи |
Ультрамікроелементи |
|
Становлять від 10 до 0,001% маси тіла |
Становлять від 0,001 до 0,0000015 маси тіла |
Становлять менше 0,000001% маси тіла |
|
C, H, O, N, P, Na, K, Mg, Ca, Cl |
Fe, Cu, Zn, Co, I, Mo, V, Ni, Cr, Se, Si, Br, Sn, As |
U, Ra, Au, Hg, Se |
- Розповідь учителя
C, H, O, N – відносять до органогенних елементів, оскільки їхня частка становить майже 98% маси живих організмів.
Хімічні елементи беруть участь у побудові організму у вигляді йонів.
Йони – це заряджені частинки речовини, які утворюються з атомів чи груп атомів у наслідок віддачі чи приєднання електронів.
Катіони – позитовно заряджені йони (Na+, Н+).
Аніони – негативно заряджені йони (ОН–, Cl–).
Біологічне значення деяких хімічних елементів (перегляд слайдів).
Слайд 1

Слайд 2

Кальцій з вітаміном D3 рекомендують під час вагітності, у період годування немовлят, при підвищеній кислотності, для нормалізації серцевої діяльності, для зміцнення зубів та нігтів.
Слайд 3

Слайд 4

Йони магнію нормалізують стан нервової системи, має здатність розширювати судини, сприяє зниженню артеріального тиску. Сполуки магнію містять різні крупи, хліб грубо-змеленого борошна, банани, горіхи, рибні продукти.
За нестачі або відсутності магнію листки стають блідо-зеленими або взагалі втрачають зелений колір, як наслідок виникає – хлороз.
Слайд 5
Фосфор необхідний для функціонуванні центральної нервової системи. Входить до складу АТФ – головного акумулятора енергії в організмі. Добова потреба людини у фосфорі 1,6-2,0 г.

Слайд 6

Ферум входить до складу гемоглобіну, який здатний зв’язувати кисень та вуглекислий газ і транспортувати їх по організму. Міститься в печінці, м’ясі, нирках, яйцях, гречаній крупі, зелені, яблуках, петрушці.
Слайд 7
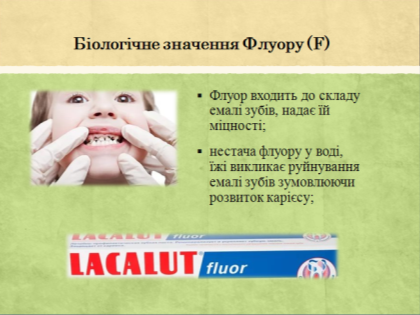
Недостатня кількість флуору у раціоні харчування викликає карієс зубів. Якщо в організм надходить збільшена кількість флуору, виникає флуороз. Захворювання супроводжується порушенням будови зубної, на якій з’являються цятки, зуби стають крихкими.
Слайд 8
- Прийом «Хвилинка - цікавинка» (короткі, цікаві, змістовні, інформативні повідомлення учнів про рослини-розвідники та індикатори).
V. Узагальнення і систематизація навчального матеріалу
1. Бесіда за запитаннями
- Що є доказом єдності живої та неживої природи?
- Які хімічні елементи трапляються в живих організмах найчастіше?
- Які елементи й чому називають органогенними?
- Які елементи й чому називають макроелементами та мікроелементами?
- Які елементи й чому називають ультрамікроелементами.
2. Прочитайте текст: «Лікар виявив у пацієнта руйнування емалі зубів. До таких наслідків могла призвести нестача (1). Лікар порадив вживати в їжу (2), які містять цей хімічний елемент. Замість цифр у тексті потрібно вибрати слова, наведені у рядку. Укажіть правильний варіант відповіді.
А 1 – калію, 2 – картоплю, сливи, абрикоси
Б 1 – флуору, 2 – шпинат, молоко, морепродукти
В 1 – феруму, 2 – печінку, яйця, яблука, петрушка
Г 1 – йоду, 2 – ламінарію
- Перегляд та аналіз фрагмента фільму про йододефіцит.
-
 Розгадати ребуси:
Розгадати ребуси:
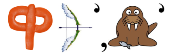 (Флуор) (Катіони)
(Флуор) (Катіони)
 (Аніони)
(Аніони)  (Вітаміни)
(Вітаміни)
VІ. Домашнє завдання
- Вивчити відповідний параграф підручника.
VIІ. Підсумок уроку
- Що нового ви дізнались на уроці?
- Чи будуть отримані знання корисними у вашому житті?
Урок 3.
Тема. Органічні молекули. Біологічні макромолекули – біополімери
Мета: сприяти засвоєнню в учнів знань про амінокислоти, як мономери білків та нуклеотиди, як мономери нуклеїнових кислот; розвивати уміння порівнювати органічні сполуки та їхнє значення у життєдіяльності організмів, уміння спостерігати, співставляти та робити відповідні висновки (інформаційна компетентність; розвивати вміння працювати в парах (комунікативна компетентність); виховувати бережливе ставлення до живих організмів планети.
Обладнання й матеріали: таблиці «Будова нуклеїнових кислот», «Будова білків»; моделі ДНК, білків; картки з формулами амінокислот, нітратних основ, нуклеотидів, нуклеозидів.
Базові поняття й терміни: амінокислоти, нуклеотди, нуклеозиди, пуринові основи, піримідинові основи.
Тип уроку: засвоєння нових знань.
Хід уроку
І. Організаційна частина
Привітання з учнями. Налаштування на роботу.
Давайте один одному посміхнемось,
Із усмішки натхнення зачерпнемо.
Із настроєм почнемо працювати
І перешкоди будь-які долати!
ІІ. Актуалізація опорних знань
Повторити знання учнів про неорганічні сполуки.
- Розминка
Цей хімічний елемент відкрили у 1811 році під час Наполеонівських війн і назвали за колір його парів «фіолетовий». Він входить до складу гормону тироксину і виробляється однією із залоз внутрішньої секреції у тілі еукаріотичних організмів. Назвіть хімічний елемент та залозу організму.
А) Фтор; Б) Хлор; В) Йод; Г) Тимус; Д) Щитоподібна.
- Установіть відповідності між групою організмів ї їхніми представниками
|
І) мікроелементи |
А) Калій |
|
ІІ) ультрамікроелементи |
Б) Нітроген |
|
ІІІ) мікроелементи |
В) Йод |
|
|
Г) Плюмбум |
3.Установіть відповідність між хімічними елементами та їхніми біологічним значенням
|
І) Ферум |
А) входить до складу молекули хлорофілу |
|
ІІ) Кальцій |
Б) забезпечує виникнення мембранного потенціалу |
|
ІІІ) Калій |
В) входить до складу дихальних пігментів |
|
|
Г) бере участь у зсіданні крові |
4. Письмове завдання
Із переліку хімічних елементів C, Cl, I, K, F, Mg, P, Ca, Fе, O, Na необхідно вибрати один відповідно до запитання:
1. Входить до складу молекул усіх органічних речовин – (С).
2. Основний позитивно заряджений іон в організмі тварин – (К).
3. Основний компонент кісток і черепашок – (Са).
4. Негативно заряджений іон в організмі тварин – (Cl).
5. Головний внутрішньоклітинний позитивно заряджений іон – (Na).
6. Входить до складу гормонів щитовидної залози – (I).
7. Входить до складу зубів – (F).
8. Структурний елемент білків, нуклеїнових кислот, АТФ – (Р).
9. Структурний компонент хлорофілу, активізує діяльність ферментів – (Mg).
10. Входить до складу молекули води – (О).
11. Входить до складу дихального пігменту гемоглобіну – (Fе).
ІІІ. Мотивація навчальної діяльності
Знання – велика сили. Володіючи знаннями, ми зможемо забезпечити собі здоров’я. Тож сьогодні ми відкриємо ще одну сторінку знань – дізнаємося про органічні молекули. Біологічні макромолекули – біополімери.
Проблемне запитання:
Чому в харчовому раціоні людини повинні бути продукти рослинного походження?
Повідомлення теми та завдання уроку
Девіз уроку:
«Єдиний шлях, веде до знань, – це діяльність»
Бернард Шоу
ІV. Вивчення нового матеріалу
1. Амінокислоти
Пояснення вчителя
Амінокислоти – це органічні кислоти, що містять аміногрупу (-NН2), якій притаманні лужні властивості, та карбоксильну групу (-СООН) з кислотними властивостями. У складі амінокислот є й специфічні для кожної з них частини, їх називають радикалами (R – групами).
![]() Загальна формула амінокислоти: N2 – СН – СООН
Загальна формула амінокислоти: N2 – СН – СООН
R
Таким чином, амінокислоти відрізняються одна від одної хімічною природою радикалу, який може бути у вигляді кільця чи ланцюга.
Відомо багато різних амінокислот – більше 300. Окремо виділяють групу із 20 найважливіших амінокислот, що постійно наявні у всіх білках.
Їх список подано в таблиці.
|
Назва амінокислоти |
Скорочена назва |
|
Аланін |
Ала |
|
Аргінін |
Арг |
|
Аспарагін |
Асн |
|
Аспарагінова кислота |
Асп |
|
Валін |
Вал |
|
Гістидин |
Гіс |
|
Гліцин |
Глі |
|
Глутамін |
Глн |
|
Глутамінова кислота |
Глу |
|
Ізолейцин |
Іле |
|
Лейцин |
Лей |
|
Лізин |
Ліз |
|
Метіонін |
Мет |
|
Пролін |
Про |
|
Серин |
Сер |
|
Тирозин |
Тир |
|
Треонін |
Тре |
|
Триптофан |
Три |
|
Фенілаланін |
Фен |
|
Цистеїн |
Цис |
2. Робота з підручником
Завдання
Користуючись текстом підручника, визначте, які амінокислоти є замінними, а які незамінними. Заповнити таблицю.
|
Амінокислоти |
|
|
замінні |
незамінні |
|
|
|
- Замінні амінокислоти – амінокислоти, які організм людини і тварини здатен синтезувати з продуктів обміну речовин (аланін, аспарагін, гістидин, гліцин, глутамін, пролін, серин, тирозин, цистеїн, аспаргінова кислота, глутамінова кислота).
- Незамінні – це ті амінокислоти, які повинні надходити з їжею, і в той же час, можуть і синтезуватися, але в недостатній кількості (аргінін, валін, ізолейцин, лейцин, лізин, метіонін, треонін, триптофан, фенілаланін).
Джерелом незамінних амінокислот повинна бути білкова їжа тваринного і рослинного походження.
Рослинні білки засвоюються гірше і містять не повний набір амінокислот, тому їх краще поєднувати з тваринними білками:
- крупи: гречана, рисова, перлова, вівсяна;
- горох, сочевиця;
- квасоля і соя;
- горіхи;
- гриби.
Незамінні амінокислоти містяться в м’ясо-молочних продуктах:
- молоко коров’яче і козяче, сир, сметана, кефір, ряжанка, вершки;
- баранина, яловичина, свинина, печінка;
- яйця.
-
Прийом «Хвилинка – цікавинка» (короткі, цікаві, змістовні, інформативні повідомлення учнів про значення амінокислот для організму людини).
- лізин і триптофан забезпечують ріст;
- метіонін – обмін жирів;
- лейцин і ізолейцин – для роботи щитовидної залози, ендокринної системи;
- фенілаланін – це амінокислота для роботи мозку, посилює пам’ять, активізує розумове сприйняття;
- аргінін – активізує імунну систему, оберігає від пухлин;
- аспарагін – виводить аміак, зменшує втому;
- гліцин – відповідає за вироблення гормонів, що регулюють імунну діяльність;
- аланін – зміцнює м’язову і нервову систему, бере участь у синтезі гормонів.
Класифікація амінокислот
|
Ароматичні |
Гетероциклічні |
Афалітичні |
Амінокислоти, що містять сірку |
Амінокислоти, що містять гідроксильну групу |
|
тирозин |
пролін |
валін |
метіонін |
треонін |
|
фенілаланін |
триптофан |
лейцин |
цистеїн |
серин |
|
|
гістидин |
гліцин |
|
|
|
|
|
аланін |
|
|
|
|
|
ізолейцин |
|
|
2. Нуклеотиди
Нуклеотиди – це мономери ДНК та РНК.
![]()
![]() Молекула нуклеотиду складається
Молекула нуклеотиду складається
![]() залишок залишок залишок
залишок залишок залишок
азотистої основи пентози ортофосфатної
кислоти
Нітратні основи ДНК:
аденін (А), гуанін (Г), цитозин (Ц), тимін (Т).
Нітратні основи РНК: аденін (А), гуанін (Г),
цитозин (Ц), урацил (У)
Пуринові основи: аденін, гуанін.
Піримідинові основи: цитозин, тимін, урацил.
V. Узагальнення і систематизація навчального матеріалу
1. Гра «Упізнай мене»
Учитель демонструє учням картки з назвами амінокислот, нітратних основ, нуклеотидів, нуклеозидів. Учням необхідно вибрати лише амінокислоти.
Аспарагін, аланін, гліцерин, тимін, гуанін, колаген, лізин, аспарагінова кислота, гістидин, олеїнова кислота, аденін, урацил, серин, міозин, цитозин.
2. Гра «Третій зайвий»
- треонін, аланін, аспарагін;
- серин, аргінін, пролін;
- триптофан, глутамін, валін,
- гліцин, лізин, гістидин.
3. Розшифрувати закодовані терміни:
- Окиманисоті – амінокислоти.
- Делукотини – нуклеотиди.
- Ропивуні восони – пуринові основи
4. Розгадати ребус
|
Нуклеотид
|
Амінокислота
|
|
Нуклеозид
|
Пурини
|
VІ. Домашнє завдання
- Вивчити відповідний параграф підручника, відповісти на запитання після параграфа.
- Дати відповідь на запитання: Чому раціон дітей і підлітків повинен містити достатню кількість білків?
VIІ. Підсумок уроку
- Рефлексія
Оцінка ефективності уроку за допомогою «кольорових» карток:
- зелений колір – мені все зрозуміло;
- жовтий колір – є труднощі, не все цікаво;
- червоний – потребую допомоги.
Урок 4.
Тема. Білки, їхня структурна організація та основні функції
Мета: сформувати в учнів знання про будову, властивості та функції білків, рівні структурної організації білків; розвивати уміння пов’язувати здобуті знання з життям та раніше вивченими темами; сприяти формуванню соціальної компетентності – вміння продуктивно співпрацювати з однокласниками, вчителем; компетентності саморозвитку – залучення учнів до написання доповідей, потребу у самостійній пошуковій діяльності; здоров’язберігаючої компетентності – бережливе ставлення до власного здоров’я та життєву необхідність здорового способу життя.
Обладнання: таблиці «Структурна будова білка», «Вміст білка в продуктах», відрізки дроту по 25 см; пробірка з білком курячого яйця, штатив, спиртівка, пробірко тримач.
Тип уроку: засвоєння нових знань
Хід уроку
І. Організаційна частина
Зібратися разом – це початок,
Триматися разом – це прогрес,
Працювати разом – це успіх.
Ми зібралися всі разом і починаємо працювати. Бажаю успіху!
ІІ. Актуалізація опорних знань
- Робота в парах
Розгадати ребуси
|
аденін |
|
гуанін |
|
|
тимін |
|
цитозин |
|
|
урацил |
|
|
|
- Розв’язати кросворд
|
|
3 |
|
|||||||||
|
|
2 |
|
|
|
|||||||
|
|
|
|
|
||||||||
|
|
1 |
|
|
||||||||
|
|
|
|
|||||||||
|
|
|
|
|||||||||
|
|
|
|
|||||||||
|
4 |
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
||||||
|
|
|
||||||||||
|
|
5 |
|
|
|
|
|
|||||
|
|
|
|
|||||||||
|
|
|||||||||||
|
6 |
|
|
|
|
|
|
|||||
|
|
|
|
|||||||||
|
7 |
|
|
|
|
8 |
|
|
|
|
||
|
|
|
|
|
|
|||||||
|
|
|
||||||||||
|
|
|
||||||||||
|
|
|
||||||||||
По горизонталі:
4. Амінокислоти, що синтезуються в організмі людини та тварин.
5. Головний внутрішньоклітинний позитивно заряджений іон.
6. Органогенний елемент що входить до складу біомолекул.
7. Нерозчинні у воді речовини.
По вертикалі:
1. Частка (4-5%) води від загальної кількості в організмі.
2. 20 амінокислот, які зустрічаються майже в усіх білках.
3. Властивість води поглинати тепло за незначних змін своєї температури.
5. Амінокислоти, які надходять в організм людини разом з продуктами харчування.
8. Хімічний елемент, що входить до складу гемоглобіну.
ІІІ. Мотивація навчальної діяльності
Життя на планеті Земля вирує в усіх проявах. Людей часто цікавлять питання: що таке життя?, звідки воно пішло?
На ці запитання наука намагалася дати відповідь протягом усієї історії. І вже досить давно вчені зрозуміли і пояснили всім, що найголовнішу роль у всіх життєвих процесах відіграють білки. Інакше кажучи, життя – це спосіб існування білкових тіл.
Символом життя завжди було яйце. Ось чому білок пташиних яєць дав назву всьому класові сполук білки. Коли вчені відкрили, що білки головні компоненти клітини, то всі прояви життя почали пов’язувати лише з ним.
Повідомлення теми та завдань уроку
ІV. Сприйняття та засвоєння нового матеріалу
- Будова білків
1. Розповідь учителя
Білки, або протеїни, становлять 50-80% усіх органічних речовин клітини. У клітинах тварин їхній вміст становить до 40-50%, у рослинних клітинах – 20-35%. До складу молекул білків входять атоми Карбону, Гідрогену, Оксисену, Нітрогену, а також Сульфуру, Фосфору, Феруму.
Білки – високомолекулярні нітрогеновмісні біополімери, мономерами яких є залишки амінокислот.
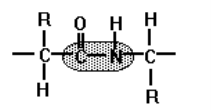 Молекули амінокислот у складі білків сполучені між собою міцним ковалентним зв’язком, який називають пептидним.
Молекули амінокислот у складі білків сполучені між собою міцним ковалентним зв’язком, який називають пептидним.
Ковалентний зв’язок виникає між карбоксильною групою однієї амінокислоти та аміногрупою іншої. Утворена сполука амінокислот називається пептидом. Пептид із двох амінокислот називається дипептидом, із трьох амінокислот – трипептидом, з багатьох амінокислот (від 6-10 до декількох десятків) – поліпептидом. Поліпептиди з високою молекулярною масою (від 6000 до кількох мільйонів) називають білками.
- Рівні структурної організації білка
Пояснення учителя
В ході вивчення, учні заповнюють таблицю.
Білки мають 4 рівні просторової організації (конформації) білка - первинна, вторинна, третинна і четвертинна структура білкових молекул.
Рівні структурної організації білка
|
Структура білка |
Який має вигляд |
Види зв’язків |
|
Первинна |
Певна послідовність амінокислотних залишків у поліпептидному ланцюзі
|
Пептидні |
|
Вторинна |
Розташування білкової молекули у вигляді спіралі та бета шару
|
Водневі |
|
Третинна |
Поліпептидна спіраль закручується в грудку або глобулу. |
Ковалентні дисульфідні, водневі; електростатичні, гідрофобні взаємодії
|
|
Четвертинна |
Спільне об’єднання кількох поліпептидних ланцюгів |
Водневі та йонні зв’язки; гідрофобні взаємодії
|
 Первинна структура білка – послідовність амінокислотних фрагментів, сполучених пептидними зв’язками. Первинна структура закодована в структурних генах.
Первинна структура білка – послідовність амінокислотних фрагментів, сполучених пептидними зв’язками. Первинна структура закодована в структурних генах.
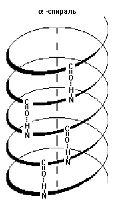
Вторинна структура – розташування білкової молекули у вигляді альфа спіралі та бета-шару. В основі утворення лежать водневі зв’язки.
Альфа-спіраль – виникає за допомогою водневих зв’язків між NH- групами одного витка спіралі і С=О групами сусіднього витка. Білок кератин утворює альфа-спіраль.
Бета – шар характерний для білків шовку.
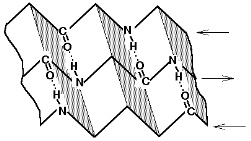
 Бета-складчаста структура білка
Бета-складчаста структура білка
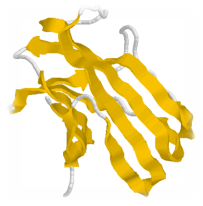
Третинна структура – здатність альфа-спіралі, закручуватись певним чином у вигляді глобули або кульки. В основі утворення лежать 4 типи зв’язків:
- ковалентні дисульфідні зв’язки між залишками цистеїну;
- водневі зв’язки (між С=О; –ОН, –NH2, –SH-групами);
- електростатична взаємодія заряджених груп в радикалах амінокислот (NН3+ і СОО-);
-
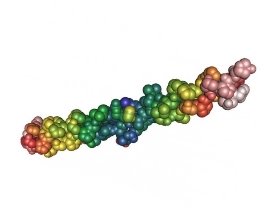 гідрофобні взаємодії виникають між негативно і позитивно зарядженими залишками амінокислот.
гідрофобні взаємодії виникають між негативно і позитивно зарядженими залишками амінокислот.
Виділяють два типи третинної структури:
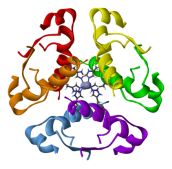 1). у фібрилярних білках третинна структура представлена або альфа-спіраллю (наприклад, в колагені), або бета-складчастими структурами.
1). у фібрилярних білках третинна структура представлена або альфа-спіраллю (наприклад, в колагені), або бета-складчастими структурами.
2). у глобулярних білках завжди є нерегулярні ділянки, є бета-складчасті структури і альфа-спіралі (наприклад, інсулін).
Четвертинна структура – це спільне об’єднання кількох поліпептидних ланцюгів, які утримуються завдяки водневим та йонним зв’язкам, а також завдяки гідрофобним взаємодіям. Наприклад, молекула гемоглобіну утворена 4 білковими молекулами, інсуліну - 2 .
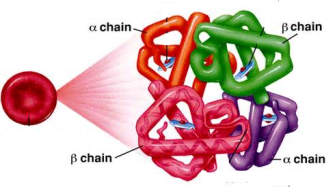
Молекула гемоглобіну
3. Класифікація білків
Складання схеми
За хімічним складом білки:
- Прості (протеїни) – складаються лише з залишків амінокислот (білок альбумін, кератин, колаген, еластин).
- Складні (протеїди) – у молекулах, крім амінокислотних залишків, мають такі небілкові компоненти: вуглеводів, ліпідів, залишки ортофосфатної та нуклеїнових кислот, атоми Купруму, Цинку, Феруму (глікопротеїди, ліпопротеїди, нуклеопротеїди).
За формою молекул:
- фібрилярні (ниткоподібні) білки нерозчинні у воді, виконують рухову (актин і міозин – білки м’язів) або будівельну (наприклад, кератин входить до складу шерсті тварин, волосся людини).
- глобулярні (кулясті) водорозчинні (наприклад пепсин забезпечує розщеплення білків їжі, імуноглобіліни – здійснюють захисну функцію, гемоглобін забезпечує транспорт газів).
- Властивості білків
Пояснення вчителя з демонструванням досліду
Запитання до учнів
Що відбудеться з білком під дією температури?
Одна з основних властивостей білків – їхня здатність під впливом чинників: дії концентрованих кислот і лугів, важких металів, високої температури, радіації, ультрафіолетового випромінювання змінювати свою структуру і властивості. Демонстрування пробірки з білком курячого яйця, який під дією температури легко змінює свою структуру.
У цьому випадку спочатку руйнується четвертинна структура, потім третинна, вторинна і, наостанок, первинна, коли розпадається поліпептидний ланцюг.
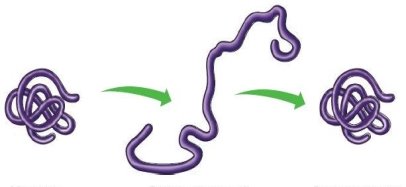 Денатурація – процес порушення природної структури білка без руйнування її первинної структури. Але якщо на початкових стадіях припинити дію чинника, то білок може відновити свій початковий стан. Це явище називається ренатурація.
Денатурація – процес порушення природної структури білка без руйнування її первинної структури. Але якщо на початкових стадіях припинити дію чинника, то білок може відновити свій початковий стан. Це явище називається ренатурація.
Денатурація і ренатурація білкової молекули
Необоротній процес руйнування первинної структури білка називається деструкцією.
- Прийом «Хвилинка – цікавинка»
Вчитель. Ми можемо трішки відпочити і послухати цікаві, змістовні, інформативні доповіді учнів.
Доповідь «Білкове живлення, хвороби, що пов’язані з ним»
Білки становлять основу структурних елементів клітин і тканин. Організму людини в середньому необхідно 1,1-1,3 г білка на 1 кг ваги тіла. Білкове голодування швидко призводить до важких розладів здоров’я. Особливо чутливий до нестачі білка зростаючий організм дітей.
Білкова недостатність викликає затримки фізичного розвитку, а потім і до повного припинення росту, до млявості, проносу, схуднення, недокрів’я, запалення шкірних покривів, порушення функцій печінки та підшлункової залози, сприйнятливості до інфекційних захворювань.
Доповідь «Амінокислоти замінні і незамінні. Роль амінокислот в профілактиці захворювань».
Харчова цінність білків залежить від їх амінокислотного складу. Замінні амінокислоти є будівельним матеріалом. Проте вісім незамінних амінокислот не синтезуються в організмі і обов’язково повинні поступати з їжею. Це такі амінокислоти, як лейцин, валін, ізолейцин, метіонін, треонін, лізин, фенілаланін, триптофан. Дослідження амінокислотного складу різних харчових продуктів показало, що білки тваринного походження більше відповідають структурі людського тіла. Амінокислотний склад білків яєць був прийнятий за ідеальний, оскільки їх засвоєння організмом людини наближається до 100%. Білки: молока засвоюються організмом на 96%, м’яса і риби – 93%, хліба і овочів на 80%, картоплі, бобових лише на 70%. У населення Земної кулі простежується певний дефіцит метіоніну, лізину, триптофану. Тому, сприятливими є поєднання рослинних і молочних продуктів, борошняних виробів з м’ясом.
Доповідь «Проблема штучного синтезу білка»
Це питання принципово розв’язане наукою. Внаслідок багаторічного роботи вдалося здійснити повний штучний синтез білків – інсуліну, рибонуклеази. Процес одержання існуліну складається з 228 окремих стадій, для кожної необхідно підібрати відповідні реактиви, каталізатори, оптимальні умови. Білок утворюється в клітині за лічені секунди. Цей процес в живих організмах навдивовижу досконалий.
- Функції білків
Самостійна робота учнів з підручником
Завдання: за допомогою тексту підручника заповнити таблицю
Класифікація білків за їх функціями
|
Класи білків |
Приклади |
Функції |
|
Структурні
|
колаген
|
Входить до складу хрящів, сухожилля, шкіри і надає відповідним органам міцності
|
|
кератин |
входить до складу нігтів, кігтів, ріг, копит, волосся, дзьобів, пір’я птаха
|
|
|
еластин
|
входить до складу шкіри, зв'язок, має здатність розтягуватись
|
|
|
фібрин |
головний компонент шовкових ниток та павутиння
|
|
|
Захисні |
імуноглобуліни (антитіла)
|
здатні впізнавати та знешкоджувати віруси, бактерії, чужорідні для організму білки
|
|
фібрин, тромбопластин, тромбін |
беруть участь у зсіданні крові, що запобігає великим крововтратам у разі пошкодження кровоносних судин
|
|
|
інтерферон |
пригнічує розмноження вірусів
|
|
|
лізоцим |
знешкоджує хвороботворні мікроорганізми |
|
|
Скоротливі |
актин і міозин |
забезпечують скорочення м’язової тканини, війок, джгутиків
|
|
Резервні або запасаючі |
яєчний білок – альбумін |
накопичується в білковій оболонці пташиних яєць; в ендоспермі насіння кукурудзи, пшениці, рису відкладаються білки, яким живиться зародок під час свого розвитку зародок
|
|
Транспортні |
гемоглобін |
забезпечує перенесення кисню у крові хребетних тварин
|
|
гемоціан
|
забезпечує перенесення кисню у крові безхребетних тварин |
|
|
міоглобін |
накопичує кисень у м’язах, який приносить білок гемоглобін; багато міоглобіну виявлено у тварин, здатних тривалий час перебувати під водою ( тюлень, кит, пінгвін) |
|
|
Каталітичні |
пепсин |
забезпечує розщеплення білків |
|
ліпаза |
розщеплює емульсовані жири |
|
|
каталаза |
розщеплює дисахариди до моносахаридів; розщеплює гідроген пероксид
|
V. Осмислення об’єктивних взаємозв’язків і взаємозалежностей у вивченому матеріалі
Проблемне завдання
Користуючись різнокольоровими частинками дроту, змоделюйте структуру білка, уявляючи, що кожний відрізок є поліпептидним ланцюгом.
VІ. Узагальнення і систематизація навчального матеріалу
- Вправа «Поміркуйте»
Вовняна тканина складається з білка кератину. Якщо випрати одяг із вовни в гарячій воді, одяг збігається. Чому? (Міцність молекули білка зумовлюється дисульфідними зв’язками. Якщо попрати тканину в гарячій воді, у молекулах білка кератину дисульфідні зв’язки розриваються і поліпептидні ланцюги згортаються у клубок).
- Поставити запитання до термінів: протеїни, пептидний, амінокислота, інтерферон, імуноглобуліни, каталаза, денатурація, ренатурація, гемоглобін, деструкція.
- Робота в парах
Закінчити сенкан з подальшим обговоренням
1. Білок
2. ……., нерозчинні
3. Руйнується,….. скорочується
4.................
5. Життя
- Гра – «Так-Ні»
- Незворотна денатурація – це руйнування білка до амінокислот із руйнуванням його первинної структури (Ні).
- Мономером білка є нуклеотид (Ні).
- Прості білки складаються лише з амінокислотних залишків (Так).
- Рухову функцію білків виконує актин і міозин (Так).
- Процес денатурації білків може бути тільки необоротнім (Ні).
- Амінокислоти можуть сполучатися одна з одною за допомогою пептидного зв’язку (Так).
- Поліпептиди з молекулярною масою понад 6000 називають білками (Так).
- До складу білків входять 10 амінокислот (Ні).
- Кератин виконує транспортну функцію (Ні).
- Лізоцим знешкоджує хвороботворні мікроорганізми ( Так).
- Пепсин забезпечує розщеплення вуглеводневої їжі ( Ні).
VI. Домашнє завдання
- Вивчити відповідний параграф підручника, відповісти на запитання після параграфа.
VII. Підсумок уроку
Вправа « Мікрофон»
- Що ви взяли для себе з уроку, чи потрібно це вам у майбутньому?
- Що найбільше запам’яталося?
Урок 5.
Тема. Ферменти, їхня роль в клітині
Мета: сприяти засвоєнню в учнів знань про будову і принцип дії ферментів, їх роль у життєдіяльності організмів; показати наочний приклад дії ферментів; розвивати вміння спостерігати за біологічними процесами та аналізувати їх (інформаційна компетентність); виховувати самостійність, культуру розумової праці, наполегливість у здобутті знань (комунікативна компетентність).
Обладнання: таблиці «Структурна будова білка», «Вміст білка у продуктах», відрізки дроту по 25 см; пробірка з шматочки сирої та вареної картоплі, штатив.
Тип уроку: засвоєння нових знань
Хід уроку
І. Організаційна частина
Учитель. Доброго дня, діти. На кожному уроці ми прагнемо досягти успіху. Сьогоднішній урок не є виключенням. Для початку, посміхніться один одному і побажайте успіху. До речі, а що таке успіх? Ви хотіли б бути успішними людьми? А що потрібно щоб досягти успіху в житті? Кожен день проведений в школі, кожен урок наближає вас до великого успіху. І сьогоднішній урок біології – це ще один крок до успіху.
ІІ. Актуалізація опорних знань
І. Виконання тестових завдань
- Які структури білків можуть порушуватися під час денатурації:
а) первинна; б) вторинна; в) третинна; г) четвертинна.
- Білки у травному тракті розщеплюються до:
а) жирних кислот; б) гліцерину;
в) амінокислот; г) глюкози.
ІІ. Вставте пропущені слова:
- Амінокислоти складаються з …, якій притаманні лужні властивості, та … з кислотними властивостями.
- Ці групи, як і атом гідрогену, зв’язані з атомом … .
- Групи атомів, за якими амінокислоти відрізняються між собою, називають … .
- Амінокислоти поділяють на … і … .
ІІІ. Установіть відповідність між білком та його біологічною функцією:
|
1) гемоглобін |
А) рухова |
|
2) пепсин |
Б) транспортна |
|
3) актин |
В) регуляторна |
|
4) фібрин |
Г) транспортна |
|
|
Д) захисна |
ІІІ. Мотивація навчальної діяльності
Демонстрація досліду
Якщо нанести краплину пероксиду водню на зріз свіжої картоплини, можна побачити виділення пухирців, а якщо на зріз вареної, то пухирці не з’являються. Що це за пухирці і чому вони не з’являються у другому випадку?
Повідомлення теми та завдань уроку
ІV. Сприйняття та засвоєння нового матеріалу
1.Будова ферментів
Розповідь учителя
Ферменти або ензими – це речовини білкового походження, які здатні вироблятися живою клітиною. Ензими виконують роль каталізаторів біохімічних процесів, що відбуваються у живих організмах. Відомо близько 1000 ферментів. Назва ферментів складається з назви речовини, на яку вони діють, і закінчення «аза». Наприклад, фермент, який розщеплює лактозу – лактазою, фермент, який розщеплює сахарозу, називають сахаразою.
Активність ферментів залежить від вологості та реакції середовища. Підвищення вологості призводить до прискорення ферментних процесів і, відповідно, до псування продуктів. Найбільша активність ферментів спостерігається у слабо-кислому або нейтральному середовищах.
Ферменти використовують у виробництві печива, хліба, для одержання патоки з крохмалю. При додаванні ферментів до пшеничного борошна скорочується процес випікання хліба, покращується його смак і аромат, збільшується об’ємний вихід, уповільнюється черствіння.
Ферменти, можуть здійснювати і негативний вплив. Наприклад, бродіння варення, руйнування вітаміну С, проростання зерна, викликати скисання молока, згіркнення жирів, перестигання плодів. З метою попередження цих процесів продукти, які швидко псуються, зберігають в холодильних камерах, для зниження активності ферментів .
Ферменти бувають простими та складними.
Прості ферменти – це білкові молекули, які складаються лише з амінокислотних залишків (пепсин, трипсин).
Складні ферменти – ферменти, які крім білкової частини апоферменту, містять ще й небілкову частину, яку називають кофактором.
Будь-яка клітина містить сотні різних видів ферментів, кожен з яких виконує певну реакцію, впливаючи на конкретну речовину – субстрат.
2. Механізм дії ферментів
Пояснення учителя
Каталітична активність ферменту зумовлена не всією його молекулою, а лише її невеликою ділянкою – активним центром, який відповідає за приєднання та перетворення сполук, що вступають в реакцію. Активний центр здатний швидко взаємодіяти лише з відповідною речовиною – субстратом. Субстрат є специфічним для певного ферменту і підходить як за структурою, так і за фізико-хімічними властивостями до активного центру «як ключ до замка». Перебіг реакції субстрату з активним центром здійснюються миттєво. Унаслідок реакції виникає фермент-субстратний комплекс, який легко розпадається утворюючи нові продукти.
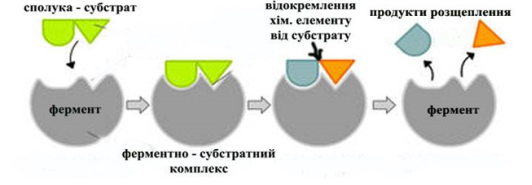
Механізм дії фермента
- Значення ферментів у господарській діяльності
Повідомлення учнів
Завдання: за розповіддю скласти схему «Використання ферментів у господарській діяльності людини».
VІ. Осмислення та конкретизація вивченого матеріалу
Обговорення демонстраційного досліду, оформлення результатів дослідження.
Фермент каталаза міститься в кожній рослинній і тваринній клітині. У першому досліді спостерігається активне виділення пухирців кисню, тому що клітини свіжої картоплі містять фермент каталазу, який розщеплює пероксид водню на воду та кисень:
![]() 2Н2 О2 → 2Н2 О +О2
2Н2 О2 → 2Н2 О +О2
Н2О2 утворюється в живих організмах у результаті окисно-відновних процесів, він токсичний, тому в клітинах відбувається процес розщеплення Н2О2, тобто знешкодження Н2О 2 ферментом каталазою.
У другому досліді пухирці газу не з’являються в результаті руйнування ферменту каталази під дією високої температури.
VІІ. Узагальнення і систематизація навчального матеріалу
Позначте знаком «+» правильні твердження про ферменти, знаком «-» – неправильні.
- Фермент – субстратний комплекс здатний підвищувати енергію активації реакції (+).
- Ферменти – глобулярні білки (+).
- Пришвидшують протікання реакції, але самі в цій реакції не витрачаються (+).
- Високоспецифічні: один фермент може каталізувати тільки одну реакцію (+).
- Їхня активність не залежить від рН середовища, тиску, температури й від концентрацій як субстрату, так і самого ферменту (-).
- Взаємодіють із субстратом за допомогою активного центру – спеціальної ділянки, що за формою відповідає субстрату (+).
VІІІ. Домашнє завдання
- Опрацювати відповідний параграф підручника.
ІХ. Підсумок уроку
Метод «Незакінчене речення»
- З цього уроку я собі взяв (взяла) ………….
- Це мені знадобиться …………….
Урок 6.
Тема. Вуглеводи та ліпіди
Мета: сформувати в учнів знання про будову, властивості та функції ліпідів та вуглеводів, (моносахаридів); розкрити значення цих органічних сполук у живій природі; розвивати уміння порівнювати будову та функції органічних молекул та сполук у клітинах живих організмів; уміння складати схеми аналізувати та робити відповідні висновки; з метою розвитку комунікативної компетентності заохочувати до активного спілкування, вміння працювати в колективі, прислухатися до чужої думки й чітко висловлювати свої судження.
Обладнання й матеріали: таблиці: «Будова молекул глюкози та крохмалю», «Ліпіди»; муляжі цукрового буряка, лабораторне обладнання, вода, цукор, рослинна олія, ацетон, крохмаль.
Базові поняття й терміни: жири, ліпіди, гліцерин, моносахариди, дисахариди, полісахариди.
Тип уроку: засвоєння нових знань
Хід уроку
І. Організаційна частина
Те, що я чую, я забуваю.
Те, що я бачу і чую, я трохи пам’ятаю.
Те, що я бачу, чую й обговорюю, я починаю розуміти.
Те, що я бачу, чую, обговорюю й роблю, я одержую знання і вміння.
Коли я передаю знання іншим, я стаю майстром.
ІІ. Актуалізація опорних знань
Вправа «Вільний мікрофон»
- Що таке ферменти?
- Які властивості ферментів?
- Які функції виконують ферменти?
- Завдяки чому ферменти здатні виконувати свої функції?
ІІІ. Мотивація навчальної діяльності
Коли у ІV ст. до н.е. воїни Олександра Македонського вступили на землю Індії, серед різних чудес краю їх вразила ця речовина. Єгиптяни назвали її індійською сіллю. Через високу цінність вона вважалася предметом розкоші й була так само дорога, як і срібло. Про яку речовину йдеться? Спробуймо знайти відповідь на це запитання під час уроку.
Повідомлення теми та завдання уроку
Девіз уроку:
«Щоб освоїти безконечне, треба роз’єднати, а потім сполучити».
Й.Гете
ІV. Вивчення нового матеріалу
(Учні об’єднуються в малі групи по 4 особи, визначають спікера. Учитель повідомляє завдання для груп).
Завдання для першої групи
- Прочитайте текст підручника «Органічні сполуки».
Визначте:
- поняття «органічні речовини»;
- які хімічні сполуки належать до органічних речовин;
- що таке вуглеводи і ліпіди?
2. Практичне завдання.
Дослід. З’ясуйте гідрофільні властивості вуглеводів на прикладі сахарид.
Завдання для другої групи
- Прочитайте текст підручника «Різноманітність ліпідів».
Визначте:
- поняття ліпіди;
- різноманітність ліпідів.
2. Практичне завдання.
Дослід. Визначити наявність жирів у насінині соняшника.
Завдання для третьої групи
- Прочитайте текст підручника «Вуглеводи, їх класифікація».
Визначте:
- поняття вуглеводи;
- на які класи поділяються вуглеводи, дайте характеристику кожному із них.
2. Практичне завдання.
Дослід. Доведіть гідрофобні властивості вуглеводів на прикладі крохмалю.
Завдання для четвертої групи
1. Прочитайте текст підручника та визначте основні функції ліпідів та вуглеводів.
- Практичне завдання.
Дослід. Доведіть гідрофобні властивості жирів.
Завдання для п’ятої групи
(Випереджувальне завдання)
З’ясувати значення вуглеводів та ліпідів у клітині, у природі та житті людини.
Презентація результатів роботи груп.
Спікери 2 - 4 груп креслять на дошці схеми та аналізують їх.
Члени першої групи звітують про виконання свого завдання
Звіт другої групи
Класифікація ліпідів
![]()
![]()
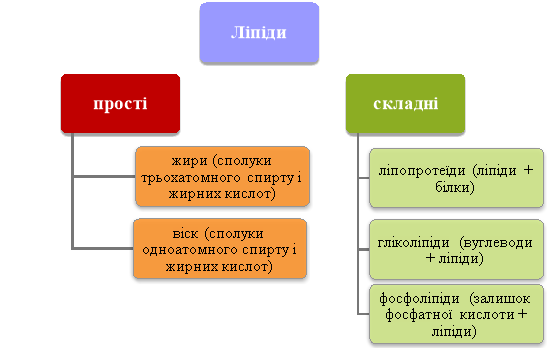
Різноманітність ліпідів
|
Жири |
Воски |
Стероїди |
|
Насіння та плоди, молоко ссавців, підшкірна жирова клітковина |
Утворюють водонепроникні шари на поверхні тіла. Використовуються бджолами для будівництва стільників. Вкривають поверхню листків та плодів. Входять до складу зовнішнього скелета комах. |
Стероїдну природу мають: статеві гормони: естрогени, андрогени, гормони надниркових залоз – кортикостероїди; холестерин, вітамін А та D |
Звіт третьої групи
Класифікація вуглеводів
|
Вуглеводи (елементи Н, С, О ) |
||
|
Моносахариди |
Дисахариди |
Полісахариди (складні) |
|
Моносахариди (складаються з однієї молекули): глюкоза, фруктоза, дезоксирибоза, рибоза, галактоза. |
Дисахариди ( складаються з двох молекул моносахаридів): сахароза, лактоза, мальтоза, трегалоза. |
Сполучення багатьох залишків молекул моносахаридів: крохмаль, хітин, целюлоза, клітковина, агар-агар, глікоген |
Звіт четвертої групи
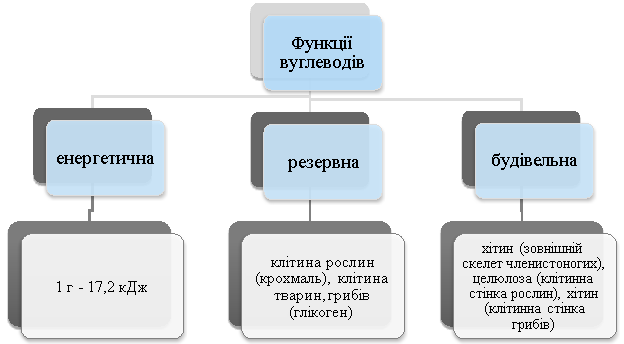
Функції ліпідів

Звіт п’ятої групи
Поширення вуглеводів у природі, біологічна роль, використання людиною.
|
Вуглеводи |
Поширення у природі |
Біологічна роль |
Використання людиною |
|
Фруктоза |
Фрукти, мед |
Енергетична, резервна |
Вживає в їжу |
|
Глюкоза |
Фрукти, мед |
Енергетична, резервна |
Вживає в їжу, використовує в медицині |
|
Рибоза |
РНК |
Структурна |
Моделювання біохімічних процесів |
|
Дезоксирибоза |
ДНК |
Структурна |
Штучний синтез генів |
|
Сахароза |
Цукровий буряк, цукрова тростина |
Резервна |
Вживає в їжу |
|
Лактоза |
Молоко ссавців |
Енергетична |
Вживає в їжу, виготовлення молочних сумішей |
|
Глікоген |
Печінка, клітини грибів |
Енергетична |
____ |
|
Целюлоза |
Стінки рослин |
Структурна |
Сировина для харчової промисловості |
|
Крохмаль |
Бульби картоплі, зернівки злаків, топінамбур |
Резервна |
Вживає в їжу |
|
Агар-агар |
Червоні водорості |
Резервна |
Поживне середовище для лабораторних досліджень |
|
Хітин |
Скелети членистоногих, стінки клітин грибів |
Структурна |
Виготовлення біологічних добавок |
Значення та практичне використання вуглеводів і ліпідів у житті людини:
- вуглеводи і ліпіди – основні джерела енергії, яку органи організму людини використовують для виконання своїх функцій;
- клітини головного мозку, працюють лише на глюкозі;
- м’язам для «запуску» потрібна лише глюкоза, а роботу виконують лише за рахунок енергії жирних кислот;
- серце використовує як «паливо» жирні кислоти – продукт розпаду жирів;
- полісахарид інулін, що міститься у топінамбурі здатний регулювати рівень цукру в крові. Вживання топінамбуру – найкраща профілактика діабету;
- вживання целюлози рослинних клітин створює оптимальні умови для розвитку корисної мікрофлори, впливає на моторику кишечника.
V. Узагальнення і систематизація навчального матеріалу
1. Вправа «Поміркуйте»
- Верблюди під час переходу через безводну пустелю можуть обійтися без води 10-12 днів. Ведмеді та бабаки під час сплячки не п’ють понад два місяці. Як на цей час вони забезпечують клітини водою?
- Чи можна налити в склянку ендогенну воду, що утворилася при окисненні жирів? Чому?
- Деякі водні ссавці мають прошарок жиру метрової товщини. Чи не тягнуть ці запаси жиру тварину на дно?
2. Гра « Так - ні»
1. У клітинах рослин переважають вуглеводи, а в клітинах тварин – білки та жири (Так).
2. Енергетична функція вуглеводів полягає в тому, що вони входять до складу опорних елементів клітини (Ні).
3.Хітин входить до складу кутикули членистоногих, стінок деяких грибів та зелених водоростей (Так).
4. Найпоширенішими серед полісахаридів є сахароза та мальтоза (Ні).
5. Підвищений вміст жирів характерний для молока ссавців та нервової тканини (Ні).
6. Рослинні жир, або олії, багаті ненасиченими жирними кислотами, тому в більшості випадків вони є легкоплавними – рідкими при кімнатній температурі (Так).
7. Тваринні жири при кімнатній температурі тверді, тому що вони містять насичені жирні кислоти (Так).
VІ. Домашнє завдання
- Вивчити відповідний параграф підручника.
- Скласти 6 запитань з теми, щоб розпочиналися словами Що?, Де?, Коли?, Як? Чому?, Навіщо?
VIІ. Підсумок уроку
Закінчити речення
- На уроці я:
дізнався ….,
зрозумів …,
навчився…
- Чи є бажання проводити дослідження надалі?
Урок 7.
Тема. Нуклеїнові кислоти. Роль нуклеїнових кислот, як носія спадкової інформації
Мета: сформувати в учнів знання про особливості будови та властивості нуклеїнових кислот; розвивати психічні процеси: мовлення, увагу, спостережливість, слухове зосередження на інформації, креативне та логічне мислення, вміння аналізувати та узагальнювати; розвивати вміння складати таблиці, порівнювати, робити висновки (інформаційна компетентність); з метою розвитку здоров’язберігаючої компетентності формувати позитивне ставлення до себе та оточуючих людей, уміння реально оцінювати свої здібності й можливості.
Обладнання й матеріали: таблиці: «Будова ДНК», «Репліація ДНК», модель «Подвійна спіраль ДНК».
Базові поняття й терміни: нуклеїнові кислоти, нуклеотиди, ДНК, РНК, і-РНК, т-РНК, р-РНК, аденін, гуанін, тимін, урацил.
Тип уроку: засвоєння знань, формування умінь і навичок і творчого застосування їх на практиці
Хід уроку
І. Організаційна частина
Психологічне налаштування на успіх
Учитель. Чим ви можете поділитися один із одним? (Знаннями з біології, здібностями, активністю).
Сьогодні на уроці ви зможете проявити ці якості, адже ми будемо працювати у парах. Я зможу поділитися із вами своїми знаннями предмета, який викладаю. Вам знадобляться розум, енергійність, знання, уміння, логіка, творчість, активність, талант. Лише тільки тоді ми зможемо отримати хороший результат. А результатом нашої роботи будуть міцні і глибокі знання з теми та високі оцінки.
ІІ. Актуалізація опорних знань
Робота в парах
- Розв’язати кросворд
|
5 |
|
9 |
|
||||||||||||||||||
|
|
4 |
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
7 |
|
|
10 |
|
|||||||||||||||
|
1 |
|
6 |
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
3 |
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
||||||||||||||||
|
2 |
|
|
|
|
|
|
|
8 |
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|||||||||||||||||||
|
11 |
|
|
|
|
|
12 |
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|||||||||||||||||
|
|
|||||||||||||||||||||
По горизонталі:
2. Мономери білків як полімерів.
3. Найпоширеніша з гексоз.
4. Резервний полісахарид рослин.
6. Білок, який виконує каталітичну функцію.
11. Вуглевод, який міститься в кутикулі членистоногих.
12. Прості молекули із залишків яких складаються біополімери.
По вертикалі:
1. Скоротливий білок м’язів.
5. В організмі ссавців слугує попередником під час синтезу статевих гормонів.
7. Міститься у великій кількості у волоссі, копитах, рогах.
8. Органічні сполуки, нерозчинні у воді.
9. Накопичується у м’язах та печінці.
10. Білок, який пригнічує розвиток вірусів.
- Визначте групу органічних речовин: сахароза, хітин, лактоза, рибоза, агар-агар, фруктоза, крохмаль, клітковина, глюкоза, глікоген, дезоксирибоза.
- а) Установіть відповідність між назвами тварин то особливостями їхньої фізіології:
|
1. комахи |
А) тварини, що тривалий час можуть жити без води, бо мають запаси жиру; |
|
2. бабаки |
Б) тварини, у яких запаси жиру містяться в жировому тілі; |
|
3. тюлені |
В) тварини, у яких жир виконує насамперед термоізоляційну функцію; |
|
4. верблюди |
Г) тварини, які завдяки запасам жиру впадають у тривалу зимову сплячку; |
|
|
Д) тварини, які не утворюють жирових запасів, оскільки мають постійне джерело живлення, а коливання параметрів середовища незначні. |
б) Установіть відповідність між назвами вуглеводів та їхніми властивостями:
|
1. целюлоза |
А) вуглевод, що зумовлює солодкий смак ягід, фруктів, меду; |
|
2. крохмаль |
Б) полімер, з якого складається деревина; |
|
3. фруктоза |
В) полісахариди, які не мають солодкого смаку й нерозчинні у воді, запасаються, наприклад у бульбах картоплі та зернах злакових; |
|
4. інсулін |
Г) полісахарид, що міститься в м язах і печінці людини; |
|
|
Д) полісахарид, що міститься в бульбах, коренебульбах і цибулинах деяких рослин, наприклад, топінамбуру, жоржини, нарцисів, лілії. |
ІІІ. Мотивація навчальної діяльності
Проблемне запитання:
У нашому організмі кожної секунди відбуваються безліч реакцій, витрачаються молекули білків, але їх не стає менше, синтезуються нові. Яким чином відтворюються саме ті білки, а не інші? Кожна дитина чимось схожа на батьків (наприклад, колір очей, форма носа). Чому?
Нуклеїнові кислоти – найважливіші органічні сполуки, які зумовлюють можливість існування й розвитку всіх живих організмів. Вперше нуклеїнові кислоти були описані у 1869 році швейцарським біохіміком І. Ф. Мішером. Виявлені в ядрі клітин лейкоцитів гною, звідки й походить назва. Багато нуклеїнових кислот в клітинах злоякісних пухлин, залозах, регенеруючи клітинах.
- Що таке нуклеїнові кислоти?
- Які існують типи нуклеїнових кислот?
- Які властивості та функції нуклеїнових кислот?
Повідомлення теми та завдання уроку
Девіз уроку:
«Не думкам потрібно навчати, а вмінню мислити».
Е. Кант
ІV. Вивчення нового матеріалу
- Будова нуклеїнових кислот
Нуклеїнові кислоти – складні біополімери, мономерами яких є нуклеотиди.
У складі однієї молекули нуклеїнових кислот може бути від 200 до 20 млн нуклеотидів. Нуклеїнові кислоти забезпечують зберігання, реалізацію та передавання спадкової інформації в живих організмах.
У живих організмах є два типи нуклеїновин кислот – дезоксирибонуклеїнова кислота (ДНК) та рибонуклеїнова кислота(РНК).
![]()
![]()
Будова дезоксирибонуклеїнової кислоти (ДНК)

Нуклеотид – ДНК



![]()
![]()
![]()
Азотиста основа Пентоза Фосфатна кислота
![]()


![]()
аденін (А) дезоксирибоза
гуанін (Г)
цитозин (Ц)
тимін (Т)
Азотисті основи у молекулі ДНК можуть повторюватися до кількох мільярдів раз.
У 1950 році американський вчений Ервін Чаргафф та його колеги виявили певні закономірності кількісного вмісту нітратних основ у молекулі ДНК.
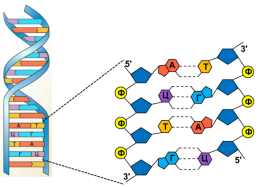 У молекулах ДНК:
У молекулах ДНК:
- кількість аденіну дорівнює кількості тиміну (А=Т), а кількість гуаніну – кількості цитозину (Г=Ц);
- кількість пуринів дорівнює кількості піримідинів: А+Г=Т+Ц або А+Г/Т+Ц=1;
- кількість основ із шістьма аміногрупами дорівнює кількості основ із шістьма кетогрупами: А+Ц=Г+Т(А+Ц/Г+Т =1).
Це відкриття стало ключем до з’ясування структури ДНК.
У 1953 р. англійські вчені Дж. Уотсон і Ф. Крик запропонували модель просторової структури ДНК. Вони показали, що молекула ДНК складається з двох поліпептидних ланцюгів, спірально закручених одна навколо іншої так, що проти аденіну завжди стоїть тимін, а проти гуаніну – цитозин. Багаторазове повторення цих зв’язків надає великої стійкості подвійній спіралі ДНК.
Чітку відповідність нуклеотидів у двох ланцюгах ДНК назвали комплементарністю.
Оскільки розміри Аденіну і Гуаніну де що більші ніж Тиміну і Цитозину, тому Аденін завжди сполучається із Тиміном двома водневими зв’язками, а Гуанін із Цитозином трьома водневими зв’язками.
Кожний виток спіралі складається з 10 пар нітратних основ. Відстань між парами нуклеотидів – 0,34 нм, крок спіралі дорівнює 3,4 нм, а її діаметр дорівнює 2 нм.
У ядерній зоні клітин прокаріотів молекула ДНК має кільцеву будову. У клітинах прокаріотів та еукаріотів молекули ДНК завжди складаються з двох ланцюгів.
Будова рибонуклеїнової кислоти (РНК)
Молекула рибонуклеїнової кислоти (РНК) є одноланцюговою ( лише в деяких вірусів РНК дволанцюгова).

Нуклеотид – РНК


![]()
![]()
![]()
![]() Азотиста основа Пентоза Фосфатна кислота
Азотиста основа Пентоза Фосфатна кислота
![]()
![]()

 аденін (А)
аденін (А)
гуанін (Г) рибоза
цитозин(Ц)
урацил (У)
Користуючись текстом підручника заповнити таблицю
|
Типи РНК |
Місце знаходження в клітині |
Будова |
Функції |
|
р-РНК |
рибосоми, мітохондрії, пластиди |
складає 85%усіх РНК клітини |
Входить до складу рибосом; разом з білками є основним їх компонентом |
|
т-РНК |
цитоплазма, рибосоми, мітохондрії, пластиди |
складає 10% усіх РНК клітини. Утворена із 70-90 нуклеотидів |
Приєднує амінокислоту і транспортує її до місця синтезу поліпептидного ланцюга в рибосомі |
|
і-РНК |
ядро, рибосоми, мітохондрії, пластиди |
складає 5% усіх РНК клітини. Має форму листка конюшини. Біля верхівки молекули міститься триплет нуклеотидів (антикодон), який є комплементарним кодону у складі і-РНК |
Передає інформацію про структуру білка з ядра клітини до рибосом |
|
іРНК |
тРНК |
рРНК |
|
|
|
|
- Властивості нуклеїнових кислот
Пояснення учителя
Молекули ДНК здатні до денатурації, ренатурації та деструкції. Молекула ДНК здатна до само подвоєння або реплікації. Воно ґрунтується на принципі компліментарності: послідовність нуклеотидів у новоствореному ланцюзі визначається їхнім розташуванням у ланцюзі материнської молекули ДНК. При цьому ланцюг материнської молекули ДНК слугує матрицею. Реплікація ДНК- напівконсервативний процес, тобто у кожній дочірній ДНК один ланцюг є материнським, а другий заново синтезований. Завдяки цьому дочірні молекули ДНК є точною копією материнської. Це явище забезпечує точну передачу спадкової інформації від материнської молекули ДНК до дочірньої.
- Функції ДНК
Функції ДНК- це кодування, збереження та реалізація спадкової інформації, передача її дочірнім клітинам при розмноженні. Окремі ланцюги молекули ДНК слугують матрицею для синтезу різних типів молекул ДНК. Цей процес називається – транскрипцією.
- Рівні організації ДНК у клітині
Молекули ДНК можуть досягати кількох сантиметрів у довжину. У ядрі їх багато. У людини 46 хромосом, кожна з яких складається з однієї молекули ДНК. Діаметр ядра близько 40 мкм.
- Як можна укласти ДНК у такому ядрі?
Первинна структура – це певна послідовність залишків нуклеотидів, розташованих у вигляді подвійного ланцюга. При цьому окремі нуклеотиди сполучаються між собою в ланцюжок за рахунок міцних ковалентних зв’язків, які виникають між залишком пентози одного нуклеотиду та залишком фосфатної кислоти іншого.
Вторинна структура молекули ДНК виникає, коли два ланцюги нуклеотидів обвивають один одного, створюючи закручену у право спіраль.
Третинна структура молекули ДНК – це суперспіраль, що виникає в результаті просторового ущільнення. Така будова характерна для ДНК хромосом еукаріотів і зумовлена взаємодією між ДНК та ядерними білками.
Наприклад, довжина ДНК найбільшої хромосоми людини становить 8 см, але вона скручена таким чином, що вміщується в хромосомі завдовжки 5 мкм.
V. Осмислення об’єктивних взаємозв’язків і взаємозалежностей у вивченому матеріалі
Практична робота № 1
Тема. Розв’язування елементарних вправ з реплікації та транскрипції.
Мета: навчитися розв’язувати задачі з молекулярної біології.
Обладнання та матеріали: таблиця генетичного коду, підручник.
Хід роботи
- Користуючись принципом комплементарності нітратних основ, напишіть послідовність нуклеотидів у ланцюзі ДНК, що буде синтезована на матриці – ланцюга ДНК із такою послідовністю нуклеотидів:
ААА-ГЦА-ЦЦГ-ЦАГ-ГГГ-АГГ-ААА-ЦТТ-ТЦА-ЦАТ
- Користуючись принципом компліментарності нітратних основ, напишіть послідовність нуклеотидів іРНК, що буде синтезована на такому фрагменті ДНК: ААА-ГЦА-ЦЦГ-ЦАГ-ГГГ-АГГ-ААГ-АЦТ-ТЦА
- Ділянка поліпептидного ланцюга має таку будову: серин – валін – аланін – лізин. Визначте послідовність нуклеотидів у ділянці ДНК. Що кодує цю частину ланцюга.
- Ділянка молекули ДНК має таку будову: АЦЦ-ГГА-АТА-ЦАА-ГТЦ
Визначте послідовність амінокислот у поліпептидному ланцюзі.
5. У молекулі ДНК тимідилові нуклеотиди складають 20% від загальної кількості. Визначте процентний вміст інших видів нуклеотидів.
6. Дослідження засвідчили: 24% загальної кількості нуклеотидів
молекули і-РНК припадає на гуанін, 38% - на аденін, 22% - на цитозин. Визначте й вкажіть назву й частку четвертого нуклеотиду в цій молекулі.
- Довжина фрагмента РНК складається з 42 нуклеотидів, яка його довжина?
VІ. Узагальнення і систематизація навчального матеріалу
- Творче завдання
Складіть сенкан з теми «ДНК»
ДНК
Дволанцюгові, високомолекулярні
Кодують, зберігають, передають
Мономерами ДНК є нуклеотиди
Біополімери
2. Визначте відповідність між молекулами та їхніми функціями:
1) АТФ А) є матрицею для синтезу іРНК
2) р-РНК Б) є матрицею для синтезу білка
3) і-РНК В) є універсальним переносником енергії
4) т-РНК Г) входить до складу рибосом
Д) транспортує до місця синтезу білка
Амінокислоти
VІІ. Домашнє завдання
- Вивчити відповідний параграф підручника.
- Порівняння ДНК і РНК, заповнити таблицю.
|
Ознаки |
ДНК |
РНК |
|
Місцезнаходження у клітині
|
Ядро, пластиди, мітохондрії |
Ядро, пластиди, мітохондрії, цитоплазма |
|
Типи нуклеотидів |
Аденіловий (А), тимідиловий (Т), гуаніловий (Г), цитидиновий (Ц).
|
Аденіловий (А), уридиловий(У), гуаніловий (Г), цитидиновий (Ц). |
|
Будова нуклеотиду |
Нітратні основа, дезоксирибоза, фосфатна кислота |
Нітрогеновмісна основа, рибоза, фосфатна кислота
|
- Розв’язати біологічну задачу ( творче завдання)
Білок складається з 9 амінокислот. Визначте й вкажіть кількість нуклеотидів в і-РНК, яка містить інформацію про цей білок.
VIІІ. Підсумок уроку
Вправа «Незакінчене речення»
- Сьогодні найцікавішим для мене було…
- Які навички виробили під час виконання практичної роботи?...
Урок 8.
Тема. АТФ. Поняття про перетворення енергії та реакції синтезу в біологічних системах
Мета: сприяти формуванню в учнів знань про особливості будови АТФ, перетворення енергії в біологічних системах; формувати комунікативну компетентність – розвивати творчу активність, пізнавальні інтереси, системність мислення; вміння правильно формулювати питання і правильно відповідати; компетентність саморозвитку - формування свідомого ставлення до навчання; виховувати інтерес до біології як до науки.
Обладнання й матеріали: таблиця: «Будова молекули АТФ».
Базові поняття й терміни: АТФ, АДФ, АМФ, макроергічний зв’язок.
Тип уроку: засвоєння нових знань.
Хід уроку
І. Організаційна частина
Привітання учнів, перевірка присутніх і стану готовності учнів до уроку.
ІІ. Актуалізація опорних знань
- Робота з картками
розшифрувати терміни та дати їм визначення
- Дезоксирибоза
|
|
е |
|
о |
|
с |
|
р |
|
б |
|
з |
|
- Аденін
|
а |
|
е |
|
і |
|
- Нуклеотид
|
н |
|
к |
|
е |
|
т |
|
д |
- Тимін
|
|
и |
|
і |
|
- Урацил
|
у |
|
а |
|
и |
|
- Запишіть послідовність нуклеотидів у молекулі і-РНК, утвореної на ділянці гена ААЦ – ЦАЦ – ЦАГ – ГАЦ
- Знайдіть помилку в ланцюзі ДНК: ТАГ- ЦАТ -ЦУА
- Метод «Мозковий штурм»
- Чому нуклеїнові кислоти мають таку назву?
- Порівняйте будову молекули ДНК і РНК.
- Що спільного і в чому відмінність ДНК і РНК?
- Що таке компліментарність у розташуванні нуклеотидів молекули ДНК і яке значення має це явище?
- Які види молекул РНК є в клітині та які їхні функції?
ІІІ. Мотивація навчальної діяльності
Ви коли-небудь замислювалися над тим, звідки у нас береться енергія для виконання різноманітних видів активності за різних умов.
Усі живі істоти потребують безперервного надходження енергії для підтримки синтезу білку і ДНК, обміну речовин, транспорту різних іонів і молекул, підтримання певної температури тіла. М’язові волокна в ході силових тренувань також вимагають легкодоступної енергії. Енергію для усіх цих процесів поставляє АТФ.
Проблемне запитання:
Що таке АТФ і яке її біологічне значення?
Повідомлення теми та завдання уроку
ІV. Вивчення нового матеріалу
- Будова АТФ, роль АТФ у перетворені енергії
Пояснення вчителя
Макроергічні сполуки – це біомолекули, що мають зв’язки, які називаються макроергічними і позначаються символом ~ (тильда).
Основною макроергічною сполукою живих організмів є молекула АТФ (аденозинтрифосфатна кислота), міститься в кожній клітині.
Вона забезпечує енергією більшість реакцій, що відбуваються в клітині. За допомогою АТФ клітина рухається, синтезує нові молекули білків, жирів, вуглеводів, позбавляється відходів, здійснює активний транспорт.
Молекула АТФ складається із азотистої основи (аденіну), п’ятивуглецевого цукру - рибози і трьох залишків ортофосфатної кислоти. Фосфатні групи у молекулі АТФ з’єднані між собою високоенергетичними (макроергічними) зв’язками в яких запасається велика кількість енергії.
 Азотиста основа
Азотиста основа
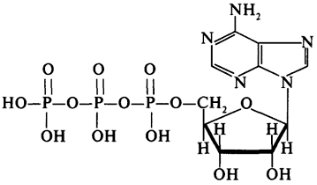
![]() Три залишки
Три залишки
ортофосфатної
кислоти

Рибоза
АТФ (аденозинтрифосфатна кислота)
АТФ – єдине і універсальне джерело енергії в клітині. За допомогою спеціального коензиму в результаті гідролітичного відщеплювання кінцевої фосфатної групи з АТФ утворюється аденозиндифосфорна кислота (АДФ) і вивільняється енергія.
АТФ + H2O → АДФ + Н3РО4 + енергія
Після відщеплювання другої фосфатної групи утворюється аденозинмонофосфат (АМФ) і вивільняється ще одна порція енергії.
АТФ + H2O → АМФ + Н3РО4 + енергія
АТФ утворюється з АДФ і неорганічного фосфату за рахунок енергії, яка вивільняється при окисненні органічних речовин.
Цей процес називається фосфорилюванням. При цьому має бути витрачено не менше 40кДж/моль АТФ. Приєднання фосфатних залишків до АМФ супроводжується акумулюванням енергії в її макроергічних зв’язках.
Фермент, 40 кДж Фермент, 40 кДж
![]()
![]()
![]()
![]() АТФ АДФ АМФ
АТФ АДФ АМФ
АТФ надзвичайно швидко відновлюється. У людини, наприклад, кожна молекула АТФ розщеплюється і знову відновлюється 2400 разів на добу, так що середня тривалість її життя менше 1 хвилини.
Синтезується АТФ головним чином у мітохондріях і хлоропластах. АТФ, що тут утворилася, по каналах ендоплазматичної сітки надходить у ті ділянки клітини, де виникає потреба в енергії.
АТФ відіграє головну роль в енергетичному обміні клітини і організму. Будь-які види клітинної активності відбуваються за рахунок енергії, що вивільняється при гідролізі АТФ. Решта енергії (близько 50%), яка вивільняється при розщепленні молекул білків, жирів і вуглеводів, розсіюється у вигляді тепла і практично не має істотного значення для життєдіяльності клітини.
V. Узагальнення і систематизація навчального матеріалу
- Вправа «Вільний мікрофон»
- Що таке АТФ і яке її біологічне значення?
- Гра «Ланцюжок»
- Мітохондрії називають «силовими станціями» клітини, тому що їхня основна функція … синтез АТФ.
- АТФ синтезується в мітохондріях клітин усіх організмів і являє собою …нуклеотид.
- Молекула АТФ може перетворюватися в ….. АДФ, при цьому виділяється енергія кількістю 40 кДж.
- Основним джерелом енергії в клітині є … глюкоза.
- Універсальним переносником енергії в клітині є молекула … аденозинтрифосфатної кислоти (АТФ).
- Встановити відповідність
|
А. Назвіть компоненти молекули АТФ |
1. Фосфорна кислота |
|
Б. Яка азотиста основа входить до складу молекули АТФ? |
2. Азотиста кислота |
|
В. Залишків якої кислоти в молекулі АТФ більше, ніж у молекулі АДФ? |
3. Рибоза |
|
Г. Що є неорганічними компонентами молекул АТФ і АДФ? |
4. Міозин |
|
Д. Який вуглевод входить до складу молекули АТФ? |
5. Лізин |
|
|
6. Аденін |
Відповіді
|
А) 1, 3, 6 |
Б) 6 |
В) 1 |
Г) 1 |
Д) 3 |
VІ. Домашнє завдання
- Вивчити відповідний параграф підручника, відповісти на запитання після параграфа.
VIІ. Підсумок уроку
- Метод «5 хвилинний відпочинок»
(Підкреслити одне із слів в кожній парі)
Яким був урок?
- Важкий – легкий
- Цікавий – нецікавий
- Зрозумілий – незрозумілий
- Потрібний – непотрібний
Урок 9.
Тема: Узагальнюючий урок з теми: «Хімічний склад клітини та біологічні молекули»
Мета: систематизувати знання учнів з теми: «Хімічний склад клітини та біологічні молекули»; перевірити рівень навчальних досягнень учнів; виявити прогалини у засвоєнні знань; формувати свідоме ставлення до навчання, розвивати навички пізнавальної діяльності; сприяти формуванню відповідальності в учнів за свою навчальну успішність – (комунікативна компетентність); уміння реально оцінювати здібності й можливості – (здоров’язберігаюча компетентність).
Тип уроку: урок узагальнення, корекції та контролю знань
Хід уроку
І. Організаційний момент
Друзі, сьогодні в нас незвичайний урок, бо ми маємо продемонструвати, що знаємо і вміємо. Цілком природно, якщо ви відчуваєте хвилювання. Нехай побороти його допоможе пам’ятка:
Я розумна, творча особистість.
Я вчуся, бо все хочу знати.
Я все знаю, я все можу, я все зможу!
Усім бажаю успішної роботи на уроці.
ІІ. Актуалізація опорних знань
1. Вправа «Шкереберть»
едазобизриско нипспе інорнефрет
иарулц гнараспаі сазохраа
2. Термінологічна розминка
Дайте визначення таким термінам і поняттям
- мікроелементи;
- макроелементи;
- диполь;
- амфіфільні речовини;
- нуклеїнові кислоти;
- білки;
- ліпіди;
- вуглеводи;
- АТФ;
- ферменти;
- денатурація;
- ренатурація.
3. Гра «Що зайве? Чому?»
- Урацил, аденін, гуанін, цитозин, тимін.
- Гуанін, цитозин, аденін, тимін, урацил.
- Лактоза, сахароза, дезоксирибоза, хітин.
- Агар-агар, рибоза, целюлоза, крохмаль.
ІІІ. Письмовий контроль знань учнів
Варіант 1
І. Виберіть із запропонованих відповідей одну правильну
1. Укажіть назву процесу відновлення природної структури білка після її порушення:
а) біосинтез; б) деструкція;
в) денатурація; г) ренатурація.
2. Як називають хімічні елементи, вміст яких у клітині менше ніж 0,1 %:
а) органогенні елементи; б) мікроелементи;
в) ультрамікроелементи; г) мікроелементи.
3. Яка структура має вигляд глобули:
а) первинна; б) вторинна;
в) третинна; г) четвертинна.
4. Укажіть білок, який виконує каталітичну функцію:
а) кератин; б) пепсин;
в) інсулін; г) тубулін
5. До якої групи ліпідів належать речовина, що утворює кутикулу на поверхні листків:
а) воски; б) жири;
в) фосфоліпіди; г) стероїди.
6. Укажіть, яку функцію виконують жири та глюкоза:
а) енергетичну; б) структурну;
в) регуляторну; г) теплоізоляційну.
7. Який полісахарид накопичується у клітинах тварин:
а) пектин; б) мурен;
в) глікоген; г) целюлоза.
8. Здатність клітин до виправлення пошкоджень у молекулах ДНК називається:
а) денатурація; б) реплікація;
в) репарація; г) ренатурація.
9. Необхідна умова зсідання крові – наявність у плазмі крові йонів:
а) магнію; б) калію;
в) кальцію; г) натрію.
10. До складу РНК, на відміну від ДНК, входять:
а) дезоксирибоза, аденін; б) рибоза, тимін;
в) дезоксирибоза, урацил; г) рибоза, урацил.
11. У ядрі відбувається синтез:
а) полісахаридів; б) ліпідів;
в) моносахаридів; г) нуклеїнових кислот.
12. Процес синтезу іРНК на одному з ланцюгів ДНК називається:
а) реплікацією; б) трансляцією;
в) транскрипцією; г) компліментарністю.
ІІ. Установіть відповідність між мономерами та макромолекулами, які вони утворюють:
|
1. нуклеотиду |
а) холестерин |
|
2. моносахариди |
б) целюлоза |
|
3. амінокислоти |
в) РНК |
|
|
г) інтерферон |
ІІІ. Установіть відповідність між назвами речовин і класами органічних речовин:
|
а) нуклеїнова кислота |
|
б) ліпіди |
|
в) вуглевод |
|
г) амінокислота |
|
|
д) білок |
ІV. Фрагмент одного ланцюга ДНК складається з нуклеотидів:
АТЦ-ТТГ-ГЦЦ-ААТ-ТЦА-ЦАТ. Вкажіть послідовність нуклеотидів в іРНК.
V. Інтенсивно працюючі клітини головного мозку мають потребу у великій кількості глюкози. З чим це пов’язано?
Варіант ІІ
І. Виберіть із запропонованих відповідей одну правильну
1. Як називають хімічні елементи, вміст яких у клітині від 0,1% до 0,01%:
а) органогенні елементи; б) мікроелементи;
в) ультрамікроелементи; г) мікроелементи.
2. Укажіть головну функцію ферментів:
а) захисна; б) сигнальна;
в) регуляторна; г) каталітична.
3. Укажіть речовини, які під дією ферментів розкладаються на амінокислоти:
а) поліпептиди; б) полісахариди;
в) ліпіди; г) полінуклеотиди.
4. У молекулі ДНК кількість нуклеотидів, що містять аденін, дорівнює кількості нуклеотидів, які містять:
а) тимін; б) гуанін;
в) урацил; г) цитозин.
5. Укажіть, яку функцію виконує білок інтерферон в організмі людини:
а) захисну; б) структурну;
в) сигнальну; г) транспортну.
6. Укажіть сполуку розчинну у воді:
а) кератин; б) крохмаль;
в) глюкоза; г) віск.
7. Укажіть речовину, що накопичується у м’язах та печінці:
а) глікоген; б) хітин;
в) крохмаль; г) целюлоза.
8. Укажіть, як називається процес синтезу нових молекул ДНК:
а) конформація; б) денатурація;
в) реплікація; г) ренатурація.
9. Укажіть з якої речовини побудована клітинна стінка рослин:
а) хітин; б) глікоген;
в) крохмаль; г) целюлоза.
10. Укажіть, який хімічний елемент входить до складу активного центру молекули хлорофілу:
а) магній; б) кальцій;
в) манган; г) ферум.
11. Зазначте, за рахунок яких зв’язків стабілізується вторинна структура білка:
а) йонних; б) водневих;
в) дисульфідних; г) пептидних.
12. Зазначте, яка частина молекули амінокислоти надає їй лужних властивостей:
а) карбоксильна група; б) аміногрупа;
в) гідроксильна група; г) сульфогрупа.
ІІ. Установіть відповідність між білками та їхніми функціями:
|
а) захисна |
|
б) каталітична |
|
в) сигнальна |
ІІІ. Установіть відповідність між біополімерами та їхніми мономерами:
|
а) моносахариди |
|
б) нуклеотиди з урацилом |
|
в) жирні кислоти |
|
г) амінокислоти |
|
|
д) нуклеотиди з тиміном |
ІV. Користуючись принципом компліментарності нітратних основ, напишіть послідовність нуклеотидів іРНК, що буде синтезована на такому фрагменті ДНК: ААА-ГЦА-ЦЦГ-ГГГ-АГГ-ААА
V. З якими білками пов’язаний процес зсідання крові? Що таке гемофілія?
V. Домашнє завдання
- Підготувати (за бажанням) інформацію про методи дослідження клітини.
VІ. Підсумок уроку
Література
- Барна І. Біологія. Збірник тестових завдань для підготовки до зовнішнього незалежного оцінювання. Тернопіль: підручники і посібники, 2017. – 304 с.
- Біологія: навч. метод. посіб./ О.А. Біда, С.І. Дерій, Л.М. Ілюха та ін.- К.: Літера ЛТД, 2006. – 656 с.
- Біологія: навч. посіб. / М.Є. Кучеренко, П.Г. Балан, Ю.Г. Верес та ін. – 4-є вид., перероблене і доповнене. – К.: Фітоцентр, 2001. – 372 с.
- Біологія: навч. посіб. / А.О. Слюсарєв, О.В. Самсонов, В.М. Мухін та ін; за ред.. та пер. з російської В. О. Мотузного. – 2-ге вид., виправлене. – К.: Вища шк., 1995. – 607 с.
- Загальна біологія: Підруч. для загальноосвіт. навч. закл. : рівень стандарту, академічний рівень / П. Г. Балан, Ю. Г. Верес, В. П. Поліщук. – К. : Генеза, 2010. – 288 с. : іл.
- Бугай О. В., Микитюк О. М., Вовк О. Г. Біологія у визначеннях, таблицях і схемах: 3-тє видання, доповнене. – Х.: Ранок, 2001 – 128 с.
- Загальна біологія: навч. посіб. / Т. О. Сало – Х.: Гімназія; Країна мрій, 2002. – 196 с.
- Зуй В. Д. Біологія: Тестові завдання для учнів 10-11 класів середніх загальноосвітніх шкіл. – К.: Вирій, 1999. - 224 с.
- Яковлєва Е. В. Уроки біології. 10 кл.: Метод. посіб. для вчителів біології. – Запоріжжя: Просвіта, 1999.


про публікацію авторської розробки
Додати розробку