Урок "Значення періодичного закону. Життя і діяльність Д. І. Менделєєва."
ТЕМА: Значення періодичного закону. Життя та діяльність Д.І. Менделєєва.
Мета:ознайомити учнів з науковим подвигом Д.І.Менделєєва; систематизувати знання
про періодичний закон і періодичну систему хімічних елементів; розкрити
узагальнююче та прогностичне значення періодичного закону і періодичної
системи елементів Д.І Менделєєва для розвитку науки та виробництва,
продовжити формувати матеріалістичний світогляд учнів; забезпечити розвиток
розумових здібностей учнів і їх уміння користуватися логічними прийомами
мислення; розвивати творчі здібності учнів; викликати у них інтерес до вивчення
хімії; показати зв’язок навчання з життям; самостійно добувати і застосовувати
знання.
Тип уроку: комбінований
Обладнання:портрет Д.І. Менделєєва; періодична система хімічних елементів; презентації; картки із завданням.
ХІД УРОКУ
І. Організаційний момент
Кожного дня шукайте позитивний момент, який би підняв вам настрій і налаштував вас на роботу, це запорука УСПІХУ.
Періодичний закон був відкритий унаслідок повсякденної напруженої роботи, коли Менделєєву казали,що він геній, учений відповідав: «Працював усе життя – тому і геній»
Працюючи від душі, ви зробите все
І для близьких, і для себе, а якщо успіху
не буде, працюйте ще.
Д.І.Менделєєв.
Постановка проблеми
Подивіться на годинник .Якби ми його розібрали, а потім зібрали, він запрацював би?Що треба для цього зробити?(Учні відповідають, щоб зборка повинна проходити в певному порядку, щоб система працювала).Ось і таблиця Менделєєва – це також система з певними закономірностями. Вони складаються з деталей,що пов’язані між собою. Ці взаємозв’язки ми з вами і пригадаємо.
ІІ. Актуалізація пізнавальної діяльності
Бліц - турнір
(використовуємо Періодичну систему хімічних елементів Д.І.Менделєєва)
- Ким і коли був відкритий періодичний закон?
- Яку властивість елементів було взято за основу їх класифікації Д.І.Менделєєвим?
- Яку будову має періодична система хімічних елементів?
- Що таке період?
- Скільки періодів у періодичній системі хімічних елементів?
- Що показує номер періоду?
- Що таке група?
- Скільки груп містить періодична система хімічних елементів?
- Що показує номер групи?
- На що вказує порядковий номер хімічного елемента?
Періодичний закон зумів поєднати всі хімічні елементи живої та неживої природи. Цей закон витримав випробування часом.
ІІІ. Мотивація навчальної діяльності
Отже, ми закінчили вивчення періодичного закону та періодичної системи.
Пройшов 151 рік, але періодичний закон та періодична система з успіхом застосовується і донині. Як ви думаєте, чому? Чому періодична таблиця Д.І.Менделєєва прикрашає кожен хімічний кабінет у школі чи ВНЗ, кожен підручник з хімії?
Сьогодні ми з’ясуємо значення періодичного закону і тим самим відповімо на питання:
- Світове визнання Д.І. Менделєєва – це заслуга його геніальності чи кропіткої праці?
ІV.Повідомлення теми і мети та плану уроку.
Тема уроку «Значення періодичного закону. Життя та діяльність Д.І.
Менделєєва.»
Мета:ознайомитись з науковим подвигом Д.І.Менделєєва; узагальнити знання про періодичний закон і періодичну систему хімічних елементів; розкрити узагальнююче та прогностичне значення періодичного закону і періодичної системи елементів Д.І Менделєєва для розвитку науки та виробництва; а також ознайомитись з життєвим і творчим шляхом Д.І. Менделєєва.
V. Вивчення нового матеріалу
Значення періодичного закону.
1.Періодичний закон – один із найфундаментальніших законів природи. Йому підпорядковані всі хімічні елементи всесвіту. А оскільки з хімічних елементів складається жива і нежива природа, то періодичний закон – це не тільки основний закон хімії, але й основний закон природи.
Графічним відображенням періодичного закону є періодична система хімічних елементів.
Наукове значення Періодичного закону.
1) Періодичний закон Д.І. Менделєєва – один із основних і найзагальніших законів природи, закон, який пов’язує властивості елементів з будовою їх атомів.
Науковий подвиг Д.І. Менделєєва полягає в тому, що він зумів поєднати всі хімічні елементи живої та неживої природи.
2) Дав можливість пояснювати явища, в яких беруть участь хімічні елементи, та передбачати нові явища і факти.
3) Дав можливість передбачити існування на той час ще невідомих хімічних елементів;
- Створюючи періодичну систему, вчений залишив багато клітинок порожніми, бо дійшов висновку, що там мають бути хімічні елементи, які існують в природі, але поки що не відкриті. Їхні властивості мають бути проміжними між властивостями сусідніх елементів. Д. І. Менделєєв дуже докладно описав властивості трьох ще не відкритих елементів і назвав їх екабором, екаалюмінієм і екасиліцієм. Протягом 15 років ці елементи були відкриті.
- Першим був відкритий екаалюміній (Лекок-де-Буабодран , француз, 1875). Цей елемент був названий галієм (Галлія - старовинна назва Франції). Другим був відкритий екабор (скандій) (Л. Ф. Нільсон , швед, 1880), потім екасиліцій, названий германієм (К. А. Вінклер, німець,1886). Ці відкриття явилися яскравим доказом справедливості вчення про періодичність властивостей елементів.
|
Властивості, які передбачив для екасиліцію Д. І. Менделєєв |
Властивості Германію, знайдені дослідним способом |
|
Відносна атомна маса 72 |
Відносна атомна маса 72,6 |
|
Сірий тугоплавкий метал |
Сірий тугоплавкий метал |
|
Густина 5,5 г/см3 |
Густина 5,35 г/см3 |
|
Повинен утворюватися при відновленні воднем з оксиду |
Утворюється при відновленні оксиду воднем |
|
Формула оксиду EsO2 |
Формула оксиду GeO2 |
|
Густина оксиду 4,7 г/см3 |
Густина оксиду 4,7 г/см3 |
|
Хлорид EsCl4 має бути рідиною з густиною 1,9 г/см3 і температурою кипіння близько 90 °С |
Хлорид GeCl4 – рідина з густиною 1,887 г/см3 і температурою кипіння 86°С |
- Цікавий факт: Лекок де Буабодран помилково визначив густину галію 4,7. Ґрунтуючись на своєму законі, Д. Менделєєв попередив винахідника, що густина галію повинна бути 6. Повторні досліди підтвердили, що вона становить 5,96.
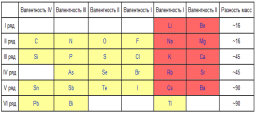
4) На основі періодичного закону і періодичної системи було виправлено відносні атомні маси багатьох елементів ( берилію, титану, ітрію, лантану, церію, талію , урану)
Наприклад, в той час відносна атомна маса Берилію мала значення 13,5. в такому випадку Берилій мав би знаходитися між Карбоном і Нітрогеном. А це, в свою чергу, порушило би періодичність у зміні властивостей елементів, оскільки метал Берилій розмістився би між двома неметалами. Звідси Менделєєв зробив висновок, що Берилій повинен мати відносну атомну масу проміжну між 7 (Літій) і 11 (Бор). Подальші дослідження це підтвердили.
5) Дав поштовх розвитку новим науковим пошукам і дослідженням, зокрема, у галузі теорії будови атома; став поштовхом для розвитку ядерної фізики.
Періодичний закон і періодична система становлять основу вивчення хімії елементів. Не варто запам’ятовувати склад і хімічні властивості великої кількості речовин. Це й неможливо зробити. Логіка вивчення хімії в університетах грунтується на порівнянні складу і властивостей простих речовин та сполук елементів кожної групи періодичної системи, а також кожної підгрупи. Вам потрібно навчитися виділяти, розуміти і передбачати головне про хімічні елементи та речовини, спираючись на періодичний закон і використовуючи періодичну систему.
У 1905 році Менделєєв написав: "Очевидно, періодичному законові майбутнє не грозить руйнуванням, а тільки надбудови і розвиток обіцяє.
Оцінюючи велич діянь Д.І. Менделєєва, видатні вчені недарма називали періодичний закон «компасом» (Рамсей В.), «яскравим маяком» (Бор Н.), «чарівною призмою» (Щукарьов С.) для виконання досліджень в галузі природничих наук.
─ А який життєвий та науково-дослідницький шлях був у Дмитра Івановича, професора Петербурзького університету, що зробив такий величезний внесок у розвиток хімії?
Про це ви повинні були підготувати повідомлення.
ДОПОВІДАЧ 1. «Життєвий і творчий шлях Д.І. Менделєєва».
ДОПОВІДАЧ 2. «Менделєєв і мистецтво».
Проблемне питання
Світове визнання Менделєєва – це заслуга його геніальності чи кропіткої праці?
Немає без явної посиленої працьовитості ні талантів, ні геніїв! – говорив Д.І.Менделєєв.
VI. Закріплення набутих знань
Природа має лише один секрет:
чи тут, чи там, у космосу глибинах.
Все: від малих піщинок до планет –
із елементів складене єдиних.
С. Щипачов “Читаючи Менделєєва”
- Як ви розумієте значення цих слів ? Що нам дає знання періодичного закону? Як практично його можна використовувати? (учні відповідають)
Дійсно, таблиця Менделєєва - це наш путівник по країні хімії, наш рятівник у "хімічно складних" ситуаціях. Тільки потрібно зуміти побачити все, що в ній написано і не написано, треба вміти читати між рядків.
Тому наступні хвилини ми з вами проведемо разом біля таблиці Менделєєва.
- Давайте пригадаємо деякі важливі числа, що повʼязані з Д.І. Менделєєвим і його відкриттям.
Завдання 1. Числові заморочки. Число – подія. Прокоментувати числа, які зображені на аркушах.
1. 1869 (відкриття періодичного закону і створення періодичної системи хімічних елементівМенделєєвим)
2. 63 (хімічні елементи було відомо на момент відкриття періодичного закону)
3. 11 (хімічних елементів передбачав Менделєєв)
4. 7 (періодів у періодичній системі).
5. 15 (років працював Менделєєв над періодичним законом)
6. 17 (дітей у родині Менделєєвих)
7. 151 (років з часу відкриття періодичного закону і створення ПСХЕМ)
8. 1834 (народився Дмитро Іванович)
9. 1907 (рік смерті Менделєєва)
10. 8 (груп елементів у короткій формі ПСХЕМ)
11. 18 (груп елементів у розгорнутій формі ПСХЕМ)
12. 14 (лантаноїдів і актиноїдів)
Звичайно, вклад Д.І. Менделєєва в розвиток хімії величезний, але він працював над проблемою класифікації елементів не один. І до нього, і після нього були зроблені відкриття, що дозволили розкрити сутність закону і підтвердити ті дані, які Менделєєв міг лише передбачати.
Завдання 2. Кросенс. Виконують 2 групи. Розмістити на магнітній дошці.
-Зрозуміло, що з тими вченими, які далі працювали над створеною системою ми поговорити не зможемо, але маємо про них листи.



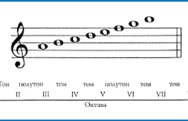




Кросенс 1. Періодична система хімічних елементів.
- Здійснена класифікація хімічних елементів
- Використані знання про поділ на метали і неметали запропонований Антуаном – Лораном Лавуазʼє
- Розподіл елементів на тріади В. Деберейнера
- Використано правило октав Дж. Ньюлендса
- У таблиці Меєра хімічні елементи складені в порядку, за атомними масами.
- Менделєєв у таблиці залишив порожні клітинки для ще не відкритих хімічних елементів.
- Таблиця приснилася вченому уві сні






 Кросенс 2. Періодична система хімічних елементів.
Кросенс 2. Періодична система хімічних елементів.
- Для складання таблиці Менделєєв вивчив властивості елементів
- Вчений врахував значення атомних мас
- Врахував періодичність зміни цих властивостей
- Менделєєв відкрив періодичний закон
- В періодичній таблиці систематизував хімічні елементи.
- Розташовані в певному порядку
- Автор періодичної системи мав улюблену справу – ремонтувати старі валізи.
Завдання 3. Лікувальні джерела. Робота в парах. Завдання на картках.
Води лікувальних мінеральних джерел містять практично всі хімічні елементи періодичної таблиці Д. І. Менделєєва. Кількість деяких із них є незначною, це мікроелементи. Установіть відповідність між назвами мікроелементів та електронними формулами їхніх атомів.
|
Назви мікроелементів 1 Літій 2 Купрум 3 Ферум 4 Флуор |
Електронні формули атомів А 1s22s22p63s23p63d64s2 Б 1s22s1 В 1s22s22p2 Г 1s22s22p5 Д 1s22s22p63s23p63d104s1 |
Завдання 4.Підпиши листа адресату. Індивідуальна робота. Користуючись періодичною системою напишіть листа.
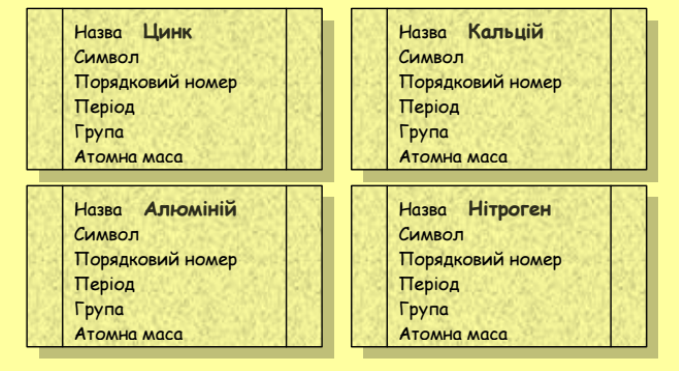
Завдання 5. Що? Де? Чому? Коли? Заповніть таблицю.
|
Назва елемента |
Електронна формула |
Порядковий номер |
Номер періоду |
Номер групи |
|
Берилій |
1s²2s² |
4 |
2 |
2 |
|
Нітроген |
1s²2s²2p³ |
7 |
2 |
5 |
|
Силіцій |
1s²2s²2p63s23p2 |
14 |
3 |
4 |
|
Магній |
1s²2s²2p6 3s2 |
12 |
3 |
2 |
Завдання 6. Засели «жителів» будинку. Розмістити хімічні елементи по родинах до яких вони належать. (Cl, Ca, Na, Ar, Ba, Mg, K,Br, Sr, Xe, Be, I, F, He, Rb, Li).
VІІ. Підбиття підсумків уроку
Періодичний закон — провідна зірка для нових відкриттів і в хімії, і в фізиці, для пошуку і добування нових хімічних елементів, для створення речовин і матеріалів із наперед заданими властивостями. Він є тією науковою основою, яка зумовлює подальший розвиток сучасної хімії, теорії будови атома, ядерної фізики та багатьох інших наук. Ось чому добутий групою американських учених під керівництвом Глена Сіборга у 1955 р. хімічний елемент № 101 був названий ними Менделевієм на честь великого російського вченого.
Крім наукового, періодичний закон і періодична система елементів мають суттєве світоглядне значення. Вони показують, що всі елементи як подібні, так і відмінні за властивостями, містяться в єдиній системі, де їх властивості змінюються закономірно, шляхом переходу кількісних змін (заряд ядра) у якісні (властивості елементів). Властивості будь-якого елемента в періодичній системі виявляються у зв'язку з іншими елементами. Отже, періодична система елементів переконливо доводить, що природа не є скупченням речовин, ізольованих одна від одної і не зв'язаних між собою. Вона ясно показує, що існує спорідненість між усіма хімічними елементами, що розвиток має місце не лише у світі тварин і рослин, а і в неорганічній природі.
Наш урок я хочу закінчити словами Д. І. Менделєєва: «Періодичному закону в майбутньому не загрожує руйнування, а тільки надбудова і розвиток суспільства». Як бачимо, ці слова пророчі.
Я вам дякую за співпрацю та гарні відповіді і маю сюрприз. Хочете дізнатися, який хімічний елемент відповідає даті вашого народження ? Я приготувала для вас
Хімічний гороскоп
За допомогою цієї формули можна обчислити номер хімічного елемента, який пов’язаний з датою народження:


VІІІ. Домашнє завдання
- Прочитати параграф 12.
- А ще дайте характеристику та дізнайтеся цікавий матеріал про свій елемент (той, що відповідає вашій даті народження).
ІХ. Оцінювання, аргументування оцінок
Я дякую вам за урок! Успіхів вам!


про публікацію авторської розробки
Додати розробку
