Уроку "Екзотермічні та ендотермічні реакції. Термохімічні рівняння"
Тема. Екзотермічні та ендотермічні реакції. Термохімічні рівняння.
Мета: сформувати поняття про тепловий ефект реакції та термохімічні рівняння, навчити розрізняти екзо- та ендотермічні реакції, характеризувати реакції за тепловим ефектом; розвинути знання про класифікацію хімічних реакцій; сформувати навички сцінювання практичного значення та ролі термохімічних реакцій у природі й житті людини.
Обладнання: негашене вапно, вода, фарфорова чашка, свічка, свіжоприготовлений купруму гідроксид; спиртівка; сірники
Хід уроку
І. Актуалізація опорних знань
«Мозковий штурм»
Пригадайте, якими зовнішніми ефектами характеризується перебіг хімічної реакції.
ІІ. Мотивація навчальної діяльності
Сьогодні панує тренд – дбати про своє здоров’я. Чи знаєте ви, як обчислюється енергетична цінність харчових продуктів?
Чи уявляєте ви життя сучасної людини без холодильника? Не думали, як в ньому підтримується низька температура? (холодоагент)
Чи можна уявити еволюцію людства без вогню, без можливості приготувати їжу, обігріти житло?
Що об’єднує холодильник і піч? Як досягається в обох випадках зміна температури?
В їх основі – хімічні реакції, під час яких відбувається виділення або поглинання тепла.
Тема уроку…
ІІІ. Формування новихзань і вмінь
- Тепловий ефект реакції.
Атоми або йони в сполуках реагуючих речовин і утворених із них продуктів реакції мають між собою хімічні зв’язки.
Які зв’язки зруйнуються, а які мають утворитись?
Чи погодитесь, що для того, щоб щось зруйнувати, треба докласти зусиль? Отже, на це витрачається енергія?
![]() Розрив зв’язків Утворення зв'язків
Розрив зв’язків Утворення зв'язків
Поглинається Е Виділяється Е
(Поглинаєтьс тепло) (Виділяється тепло)
Знайдіть у підручнику визначення теплового ефекту реакції (ст 104). Запишіть в зошит.
Що, на вашу думку, треба знати для визначення енергетичної цінності харчових продуктів?
(Щоб обчислити енергетичну цінність харчових продуктів, треба знати тепловий ефект реакції їх згоряння)
- Екзо- та ендотермічні реакції.
Пригадайте з фізики - кожна речовина характеризується певним запасом енергії, що утворюється внаслідок хаотичного руху структурних частинок цієї речовини (молекул, атомів, йонів тощо). Як називається така енергія?.
![]() Реагенти Продукти
Реагенти Продукти
Внутрішня Е Внутрішня Е
Що відбудеться, якщо внутрішня енергія реагентів більша , ніж внутрішня енергія продуктів? ( Енергія у вигляді тепла виділяється)
Що відбудеться, якщо внутрішня енергія реагентів менша , ніж внутрішня енергія продуктів? ( Енергія у вигляді тепла поглинається)
Дослід 1. Взаємодія кальцій оксиду з водою - «гасіння вапна».
На дно фарфорової чашки покладемо кілька шматочків кальцій оксиду й обережно доллємо воду. Спостерігаємо бурхливу реакцію, «закипання» суміші з виділенням великої кількості тепла
![]()
Тепло виділяєтьс я, чи поглинається? Позначення теплового ефекту
Знайдіть на ст 102 , як називається така реакція. Запишіть в зошит
Наведіть ще приклади реакцій, під час яки виділяється тепло
Дослід 2. Розклад купрум(ІІ) гідроксиду.
Нагріємо в полум'ї спиртівки синій осад купрум(ІІ) гідроксиду, добутий реакцією обміну. За кілька хвилин спостерігаємо утворення чорного осаду — порошку купрум(ІІ) оксиду. Реакція відбувається тільки за нагрівання, тобто з поглинанням тепла.
На ст 103 підручника знайдіть, як називають такі реакції. Запишіть в зошит
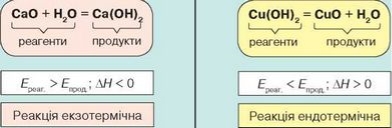
- Термохімічні рівняння
Зверніть увагу на запис реакції реакції «гасіння вапна». Що в ній незвичне? ![]()
Знайдіть на ст 104, як називають такі реакції. Запишіть в зошит
IV.Систематизація набутих знань і вмінь
- Вправа 2 (ст 106 підручника Березан)
Перетворіть наведені схеми на рівняння реакцій та вкажіть, які з них є екзотермічними (відповідь обґрунтуйте):
1) СН4 → С + Н2 ↑;
2) CS2 + O2 → CO2 + SO2 ;
3) K + H2 O → KOH + H2 ↑;
4) HgO → Hg + O2 ↑;
5) KNO3 → KNO2 + O2 ↑;
6) Cu(OH)2 → CuO + H2 O;
7) AgNO3 →Ag + NO2 ↑ + O2 ↑;
8) Ca + O2 → CaO;
9) H3 PO4 + KOH → K3 PO4 + H2 O;
10)CuSO4 · 5H2 O → CuO + SO3 + H2 O
- Вправа 6 (ст 1007 підр Березан)
Укажіть, які з наведених рівнянь описують екзотермічні реакції, а які — ендотермічні:
SO3 (г) + H2 O(г) = H2 SO4 (р); ∆H = –89 кДж;
2SO3 (р) = 2SO2 (г) + O2 (г); ∆H = +284 кДж;
H2 (г) + Br2 (г) = 2HBr(г); ∆H = –68 кДж;
CaO(т) + CO2 (г) = CaCO3 (т); ∆H = –1770 кДж;
N2 (г) + 3H2 (г) = 2NH3 (г); ∆H = –92 кДж
Прокоментуйте реакції
V. Домашнє завдання:
вивчити §20, виконати вправу 1 (знизу сторінки 106 підручника Березан)


про публікацію авторської розробки
Додати розробку
