Відносна молекулярна маса речовини. Її обчислення за хімічною формулою.
Конспект відкритого уроку
з хімії
на тему:
«Відносна молекулярна маса речовини. Її обчислення за хімічною формулою»
Підготувала
Вчитель хімії
Колаковська Л.О.
Тема. Відносна молекулярна маса речовини. Її обчислення за хімічною формулою.
Знаннєвий компонент:поглибити поняття про хімічну формулу, її використання для розрахунків; дати поняття про відносну молекулярну масу; Діяльнісний компонент:формувати вміння й навички обчислювання за хімічними формулами; навчити визначати відносну молекулярну масу простих і складних речовин за їх формулами;
Ціннісний компонент: виховувати бережливе ставлення до навколишнього середовища та себе самого; робить висновки на основі спостережень.
Тип уроку: комбінований
Наскрізні змістові лінії:
Спілкування державною мовою
Здоровя і безпека ( безпечне поводження із речовинами)
Підприємливість і фінансова грамотність ( розв’язування задач на визначення молекулярної маси речовин).
Обладнання: періодична система хімічних елементів, роздатковий матеріал, проектор, презентація, пробірки, сода, оцтова кисота.
Методи та методичні прийоми: словесні: бесіда, розповідь; практичні: самостійна робота; частково-пошукові; проблемне запитання, вправа «Шпаргалка», вправа «Мікрофон», вправа «Сортувальник», мотиваційний прийом «Відгадай і обчисли», самостійна робота з навчальною таблицею, вправа « Піраміда», стратегія «Кошик», прийом «Закінчи речення..».
Базові поняття та терміни: атом, молекула, відносна атомна маса, ядро, протон, електрон, молекулярна маса, відносна молекулярна маса.
«Той, хто прагне якомога краще знати хімію, має бути знавцем і в математиці…»
М. В. Ломоносов
Структура уроку:
- Організаційний момент.
- Перевірка домашнього завдання.
- Мотивація навчально-пізнавальної діяльності.
- Актуалізація опорних знань, вмінь та навичок.
- Вивчення нового матеріалу.
- Закріплення вивченого матеріалу.
- Підбиття підсумків уроку.
- Домашнє завдання .
ХІД УРОКУ
І. Організаційний момент.
Вчитель: Нумо, діти, підведіться!
Всі приємно посміхніться.
Продзвенів уже дзвінок,
Починаємо урок!
- Прикріпляю на дошці смайл "Радість" і бажаю всім учням гарного настрою, легкого засвоєння теми.
Для того, щоб впоратися на уроці з завданнями,
будьте старанними і слухняними.
Щоб не просто слухали, а чули.
Щоб не просто дивилися, а бачили.
Щоб не просто відповідали, а міркували.
Дружно і плідно працювали.
- А зараз усміхніться один одному, подумки побажайте успіхів на цілий день.
ІІ. Перевірка домашнього завдання .
На ваших столах є картки для самоконтролю знань із зображенням колбочки. Запишіть своє прізвище. Користуйтеся цією карткою протягом уроку.
«Шпаргалка». Вчитель роздає два види карток: на одних записує термін,а на інших – його визначення. Один учень називає термін, а інший – правильне його визначення.
|
Термін |
Визначення |
|
Хімічна формула |
Умовний запис складу речовини за допомогою хімічних символів та індексів |
|
Молекула |
Найменша частинка речовини, що зберігає властивості речовини |
|
Атом |
Найменша частинка хімічного елемента, яка складається із позитивно зарядженого ядра і негативно заряджених електронів, які рухаються навколо ядра. |
|
Хімічний елемент |
Вид атома із певним зарядом ядра |
|
Індекс |
Цифра, яка стоїть біля хімічного елемента у правому нижньому кутку і вказує на кількість атомів у молекулі |
III. Актуалізація і поглиблення знань.
Вправа «Мікрофон»
• Прочитайте формули записаних речовин і розшифруйте якісний і кількісний склад цієї речовини. (Працюють по черзі)
Вправа «Сортувальник»
• Розділіть запропоновані речовини на прості та складні.
СО2, О2, Н2О, NaCl, C12H22O12, NaHCO3, СаCO3, Zn, CaF
Тема нашого уроку записано на дошці. Для того, щоб її прочитати зясуємо відносні атомні маси хімічних елементів у таблиці. Відкриваємо слова так, щоб значення відносних атоних мас були розміщенні у порядку зростання. Ми отримали тему нашого уроку.
|
Хімічний елемент |
Відносна атомна маса |
Тема уроку |
|
Оксиген |
|
маса |
|
Карбон |
|
відносна |
|
Ca |
|
її обчислення |
|
Ферум |
|
за хімічною |
|
N |
|
молекулярна |
|
Цинк |
|
формулою |
|
Mg |
|
речовини |
Отже, тема нашого уроку «Відносна молекулярна маса речовини, іі обчислення за хімічною формулою.»
ІV. Мотивація навчально-пізнавальної діяльності.
Щоб хімію добряче знати,
Треба вміти рахувати.
Спочатку маси речовин,
Але це тільки на почин.
Проте почин – один з початків,
Формування вмінь й задатків.
Не навчишся, маси рахувати
Надалі важко буде хімію вивчати.
Постановка проблемного запитання
П’ятачок та Вінні-Пух йшли на День народження до ослика Іа та несли йому три кульки. Кульки були заповненні різними газами: киснем, воднем та вуглекислим газом. Одна з них весь час чомусь хотіла злетіти, інша намагалася впасти на землю. П’ятачок та Вінні-Пух вирішили дізнатися про причину цього явища у Мудрої Сови.
Як ви вважаєте, якою була її відповідь у?
А як обчислити масу всієї молекули?(Як суму атомних мас усіх атомів, що входять до складу молекули)
V. Вивчення нового матеріалу
Молекулярна маса — це маса однієї молекули певної речовини.
• А якщо для визначення молекулярної маси використовувати наведені в таблиці відносні атомні маси?
Відносна молекулярна маса— це фізична величина, що показує, у скільки разів маса певної молекули більша за 1/12 маси атома Карбону — 12.
Одиниця вимірювання: [Мr] = а.о.м.
Алгоритм обчислення Мr:
1) За періодичною системою знайди значення відносних атомних мас елементів Аr, що входять до складу молекули речовини.
2) Ці значення помнож на число атомів елемента (на індекс).
3) Додай одержані числа. Це і є відносна молекулярна маса Мr. Наприклад: Аr(S) = 32; Аr(О) = 16; Аr(Ba) = 137.
Готові округлені відносні атомні маси елементів можна також знайти в підручнику на ст.191-195.
4. Щоб обчислити відносну молекулярну масу, треба додати відносні атомні маси елементів, які входять до складу молекули, з урахуванням їх кількості.
5. Відносна молекулярна маса Мr величина безрозмірна (не має одиниць вимірювання).
Величини відносних молекулярних мас широко використовують у різних хімічних, фізичних і хіміко-технічних розрахунках. Тому важливо вміти її обчислювати.
- Закріплення вивченого матеріалу.
Мотиваційний прийом «Відгадай і обчисли»
Перед вами завдання: обчислити відносні молекулярні маси речовин, які є відгадками до загадок від Мудрої Сови.
❖ Ти рідка, тверда, ще й пара.
Знають всі тебе сповна.
Не звариш без тебе страви,
Хоч сама ти несмачна. (Вода)
Мr (Н2О)=1·2+16=18
Загадки:
❖ Я – газ без кольору, без смаку.
Я непомітний в вишині.
Та жити, друзі, неможливо
Без мене людям на Землі.
Я вам будинок обігрію,
В лікарні вилікую вас.
А, реагуючи із воднем,
Я воду утворю для вас.
Якщо колись (не дай-то Боже),
Я зникну раптом на Землі,
Життя зупиниться назавжди. Я – найцінніший на Землі. (Кисень)
Мr (О2)=16·2=32
Учні роблять записи на дошці і в зошиті
Цей елемент є складовою частиною космосу, а газ, що утворений цим елементом – найлегший на Землі. (Водень)
Це газ, без якого не проходив би процес фотосинтезу у природі (вуглекислий газ)
Демонстрація досліду. А зараз давайте поспостерігаємо цікаве явище, яке має назву «Шипучка». Учні спостерігають та обчислюють відносну молекулярну масу натрій гідроген карбонату, що утворився під час реакцій:
Мr (NаНСО3)=23+1+16·3=72,
Мотиваційний елемент (бесіда): Чи зустрічали ви таке явище в побуті? Яке його значення? Чи правильно роблять дорослі? Чи має ця рочовина інше використання?
Отже, хімічна формула речовини дозволяє обчислити відносну молекулярну масу речовини.
Завдання 1. До складу пластмаси конструктора «Лего» входить речовина барій сульфат, яка не розчиняється у воді і не токсична для організму. А ще її добре видно на рентгенівських знімках. Якщо дитина проковтне таку деталь, то її легко буде видалити. Формула цієї речовини BaSO4. Обчисліть відносну молекулярну масу цієї сполуки.
Завдання 2. Визначаємо відносні молекулярні маси речовин (обирають пелюстку квітки )
Звертаю увагу учнів на те, що слід враховувати кількість атомів кожного елемента в молекулі!
Завдання 3. Розташуйте речовини в порядку зростання відносних молекулярних мас.
CH4 SO2 O3 NO
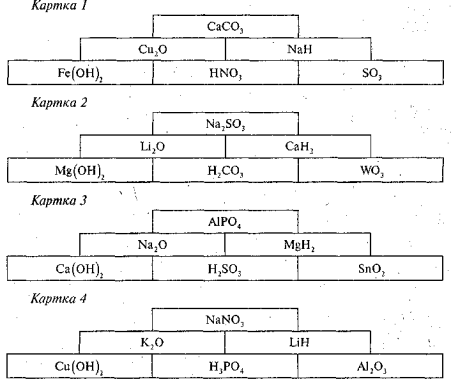
Піраміда
Кожна учень одержує картку-завдання і повинні обчислити суму відносних молекулярних мас. Завдання повторюються для можливості перехресної перевірки.
VІІ. Підбиття підсумків уроку.
Стратегія «Кошик». Вирушаючи в дорогу. Ви завжди берете із собою певні необхідні речі. Ось і сьогодні, закінчуючи урок, давайте зберемо наш кошик знань. Закінчити речення очікувань:
1. Я знаю, що відносна молекулярна маса речовини – це __________________________.
2. Я знаю, що відносна молекулярна маса позначається ___________________________ .
3. Я знаю, що для того, щоб розрахувати відносну атомну масу речовини необхідно ________________________________________ .
4. Я знаю, що відносну атомну масу кожного елемента можна знайти в _____________ .
5. Я знаю, що мені потрібно вміти обчислювати відносну атомну масу речовини, для того, щоб __________________________________ .
Виставлення оцінок та їх мотивація
VІI.Домашнє завдання . Прочитати параграф 16 с.78-79; завдання 4,5 с.82 (письмово).


про публікацію авторської розробки
Додати розробку

