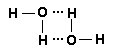
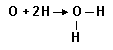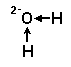Вода, її фізико-хімічні властивості.
1
Дата ___/____/____ Клас _________
Урок № 5
Роль води в життєдіяльності організмів
Мета уроку: сформувати в учнів знання про роль води в життєдіяльності організмів, стандарти якості питної води; продовжити розвивати логічне мислення, увагу, вміння аналізувати й робити висновки; формувати навички практичної діяльності; здійснювати екологічне виховання, сприяти формуванню здорового способу життя.
Очікувані результати: учні характеризують роль води в існуванні живих систем різного рівня, вікові зміни кількості води в клітинах, поняття «гідрофільність», «гідрофобність»; пояснюють необхідність контролю хімічного складу води; норми вживання води людиною в різних умовах навколишнього середовища.
Обладнання: ____________________________________________________________________
Тип уроку: урок формування вмінь та навичок.
- 1. Організаційний етап
Привітання учнів, перевірка їхньої готовності до уроку
- 2. Перевірка домашнього завдання й актуалізація опорних знань учнів
2.1. «Розумний куб».
(«Розумний куб» — це метод, для застосування якого виготовляється куб для індивідуального чи фронтального опитування. На кожній із граней написане одне із запитань, за яким можна дати характеристику чого-небудь, провести аналіз тощо. Учень кидає куб і відповідає на запитання, яке йому випало на верхній грані. Така робота дає можливість створювати на уроках ігрові моменти і дуже позитивно сприймається учнями.)
Зразок запитань на гранях куба:
1. Яка роль кисню в життєдіяльності організмів?
2. Яка роль оксидів у життєдіяльності організмів?
3. Яка роль неорганічних кислот у життєдіяльності організмів?
4. Яка роль мінеральних солей у життєдіяльності організмів?
5. Навіщо організму потрібні нерозчинні мінеральні солі?
6. У якому вигляді в організмі присутні мінеральні солі?
2.2. Розгадування кросвордів, які учні підготували вдома (учні обмінюються кросвордами і розгадують їх).
- 3. Мотивація навчальної діяльності
Слово вчителя
Відомий факт описаний французьким письменником Антуаном де Сент-Екзюпері в повісті «Планета людей», герой якої, зазнавши катастрофи під час перельоту над пустелею, пере-живши передсмертну агонію від зневоднення організму і відчувши радість спасіння, вигукнув: «Вода! У тебе немає ні смаку, ні кольору, ні запаху, тебе неможливо описати, тобою насолоджуєшся, не знаючи, що ти таке. Не можна сказати, що ти потрібна для життя: ти саме життя. Ти наповнюєш нас радістю, яку не пояснити нашими почуттями, з тобою повертаються до нас сили, з якими ми вже розпрощалися… Ти найбільше багатство на світі…»
Що ж таке вода? Таке запитання може здатися дивним, але ми спробуємо відповісти на нього. З водою добре знайомий кожен, хто звик умиватися, п’є чай, уміє плавати, катається на ковзанах, санчатах або лижах. Вода виліпила «обличчя» нашої планети. Усе зелене життя народжене водою, і ми — діти води. Вода — це найважливіша речовина на Землі, без якої не може існувати жоден живий організм і не можуть протікати жодні біологічні, хімічні реакції й технологічні процеси. Чому ж така важлива ця рідина, ми з’ясуємо сьогодні на уроці.
Повідомлення теми уроку. Визначення разом з учнями мети і завдань уроку.
- 4. Засвоєння нового матеріалу
План пояснення нового матеріалу
1. Будова молекули води. (Розповідь учителя, бесіда.)
2. Властивості та функції води. (Бесіда, самостійна робота учнів з підручником, складання
опорної схеми, заповнення таблиці, повідомлення учнів.)
- 5. Самостійне застосування учнями знань у стандартних ситуаціях
Практична робота № 1. Визначення вмісту води у власному організмі*
5.1. Виконання практичної частини роботи.
1. Інструктаж учителя щодо виконання практичної роботи.
2. Виконання практичної роботи (згідно з інструкційною карткою).
5.2. Звіт про виконання роботи.
- 6. Узагальнення і закріплення знань
Учитель просить учнів визначити результати уроку, назвати найбільш цікаві факти, що розглядалися на уроці.
- 7. Домашнє завдання
7.1. Завдання для всього класу.
Підручник _____________________________________________
Зошит _________________________________________________
7.2. Індивідуальні та творчі завдання.
Підготуватися до узагальнюючого уроку з теми «Вступ. Неорганічні речовини».
Урок
Роль води у життєдіяльності організмів
- 2. Перевірка домашнього завдання й актуалізація опорних знань учнів
2.3. «Так — ні».
Учитель зачитує твердження, а учні погоджуються або не погоджуються з ними.
1. Молекули мінеральних солей у водному розчині розпадаються на йони.
2. Сталий вміст натрій хлориду (0,9 %) у плазмі крові — необхідна складова підтримання гомеостазу нашого організму.
3. Збільшення секреції хлоридної кислоти позитивно впливає на організм людини.
4. До неорганічних сполук належить тільки вода.
5. Різна концентрація йонів Na+ і K+ поза клітинами та всередині них призводить до виникнення різниці електричних потенціалів на мембранах, які оточують клітини.
6. До складу багатьох ферментів входять йони Fe2+ і Zn2+, які забезпечують їхню активність.
7. Нітроген(ІІ) оксид є одним з найважливіших імунотропних медіаторів.
8. Сульфатна кислота необхідна для синтезу АТФ (є універсальним накопичувачем енергії в клітині) та різних типів нуклеїнових кислот.
9. Кисень може бути шкідливим для живого організму.
10. Вуглекислий газ є антиоксидантом.
11. Хлор-аніони входять до складу гормона тироксину.
12. Наявність у плазмі крові йонів Ca2+ — необхідна умова для зсідання крові.
Відповідь:
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
12 |
|
так |
так |
ні |
ні |
так |
ні |
так |
ні |
так |
так |
ні |
так |
- 4. Засвоєння нового матеріалу
1. Будова молекули води
- Розповідь учителя
Протягом усього свого життя людина щодня має справу з водою. Вона використовує її для пиття та їжі, для вмивання, улітку — для відпочинку, узимку — для опалення. Для людини вода є значно ціннішим природним багатством, ніж вугілля, нафта, газ, залізо, тому що вона незамінна. Без їжі людина може прожити близько 50-ти днів, якщо під час голодування вона буде пити прісну воду. Без води вона не проживе й тижня — смерть настане через 5 днів. За даними медичних експериментів, при втраті вологи в розмірі 6–8 % від ваги тіла людина впадає в напівнепритомний стан, при втраті 10 % — починаються галюцинації, при втраті 12 % людина не може відновитися без спеціальної медичної допомоги, а при втраті 20 % наступає неминуча смерть.
Вміст води в клітинах різних організмів відрізняється, наприклад вміст води в огірках дорівнює 95 %, у моркві — 90 %, у яблуках — 85 %. Не відстаємо від рослин і ми. Води мало лише в жировій тканині і кістках — 33 %, у м’язах — 77 %, у легенях і нирках — 80 %, у нервовій тканині — 84 %, а в сірій речовині мозку — 85 %.
Не випадково в давньоіндійському філософському трактаті «Упанішада» сказано: «води міркували: “Нехай ми станемо багато чим, нехай ми розмножимося”».
Справді, вода — найбільш дивовижна речовина в природі. Усі тіла при охолодженні стискаються, а вода — розширюється; на її поверхні можуть плавати тіла, важчі за воду; вона ніколи не буває в природі абсолютно чистою; вода навіть може подолати гравітацію! У хімічному відношенні вода досить стійка, але ця сполука має деякі дуже цікаві властивості. Порівняно з більшістю інших рідин у води незвично високі температури плавлення і кипіння, а також теплота випаровування.
Запитання до учнів:
— Чим можна пояснити ці дивовижні властивості води?
Очікувана відповідь учнів:
Хімічною будовою та фізико-хімічними властивостями води.
— Пригадайте з уроків хімії, які особливості будови характерні для молекули води.
Очікувані відповіді учнів:
До складу молекули води входять два атоми Гідрогену й один атом Оксигену. Оскільки електронегативність Оксигену значно більша за електронегативність Гідрогену, утворені за рахунок спільних електронних пар зв’язки О–Н у молекулі води ковалентні полярні. Вони розміщені під кутом 104,5°, і це спричинює асиметричність структури і виникнення диполя.
— Що таке диполь і за яких умов молекула є диполем?
Очікувані відповіді учнів:
Незважаючи на те, що молекула води загалом електронейтральна, у неї має місце дипольний момент. Її атом Оксигену несе на собі частковий від’ємний заряд, а атом Гідрогену — частковий додатний заряд. Перерозподіл додатного і від’ємного зарядів у межах однієї електронейтральної молекули створює дипольний момент.
- Розповідь учителя
Завдяки такому перерозподілу зарядів дві сусідні молекули води взаємодіють між собою за допомогою водневих зв’язків.
Запитання до учнів:
— Пригадайте, який зв’язок називається водневим. (Водневий зв’язок — це приклад міжмолекулярного хімічного зв’язку. Він виникає між атомами Гідрогену однієї молекули й атомом дуже електронегативного елемента іншої молекули.)
- Проектування зображення на екран
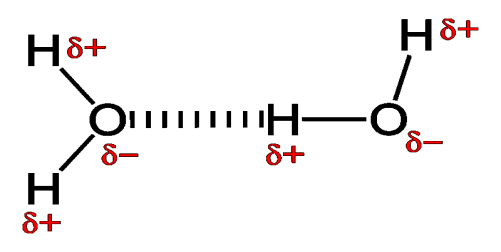
Отже, кожна молекула води може сполучатися із сусідніми молекулами.
- Формулювання висновку:
Завдяки дипольним властивостям воду можна вважати, у певному розумінні, полярною, або біполярною, рідиною. Саме біполярність води забезпечує високу розчинність у ній хімічних сполук. А розчинність сприяє проникненню цих сполук у клітини.
- Розповідь учителя
Розрізняють дві форми води — вільну та зв’язану (структуровану). Зв’язана вода здатна формувати водну оболонку навколо певних сполук (наприклад, білків), що запобігає їхній взаємодії між собою. Вона характеризується низкою специфічних властивостей: нижчою точкою замерзання, меншим об’ємом, відсутністю здатності розчиняти речовини, які містяться в невеликих концентраціях (цукри, гліцерин, деякі солі). Зв’язана вода становить 4–5 % від загальної кількості води в організмі. Решту води (95–96 %), не зв’язану з іншими сполуками, називають вільною. Саме вільна вода є універсальним розчинником.
2. Властивості та функції води
- Розповідь учителя
За властивістю розчинятися у воді хімічні речовини поділяються на гідрофільні та гідрофобні.
- Самостійна робота учнів з підручником
Завдання за варіантами:
І варіант: Які речовини називаються гідрофобними? Навести приклади.
ІІ варіант: Які речовини називаються гідрофільними? Навести приклади.
(Обговорення відповідей учнів.)
- Доповнення вчителя
Окрім цього, існує дуже поширений у живих клітинах клас хімічних сполук, які мають подвійну природу. У них є гідрофільна «голівка» і гідрофобний «хвіст». Такі сполуки мають назву амфіфільних (наприклад, фосфоліпіди і т. п.). Саме завдяки амфіфільності сполук, що створюють клітинну оболонку, клітина забезпечує собі певну ізольованість від зовнішнього середовища.
- Складання опорної схеми
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
- Повідомлення учня
Властивості та функції води
Вода — універсальний розчинник. У ній розчиняються всі необхідні для живого організму сполуки (органічні й мінеральні речовини, гази); вона має високу теплоємність і водночас високу для рідин теплопровідність. Ці властивості роблять воду ідеальною для підтримання теплової рівноваги організму.
Завдяки полярності своїх молекул вода виступає в ролі стабілізатора структури, визначає функціональну активність макромолекул залежно від товщини гідратної оболонки, що розташована навколо них. Вода — джерело кисню, що виділяється при фотосинтезі, і водню, який використовується для відновлення вуглекислого газу. Вода є основним середовищем, де відбуваються біохімічні й хімічні реакції.
Вода практично не стискається, що дуже важливо для надання форми органам і підтримання їх, створення тургору і забезпечення відповідного положення органів і частин організму. Завдяки воді стають можливі осмотичні явища в живих клітинах.
Вода — основний засіб пересування речовин в організмі (кровообіг, висхідний і низхідний рух розчинів у тілі рослин тощо). Тому вода — дійсно дивовижна речовина в природі.
- Заповнення таблиці
Властивості та функції води
|
Хімічна будова |
Фізичні властивості |
Біологічні функції |
|
H 1S’ O 1S22S22P4 |
1. За звичайних умов рідина, велика густина речовини |
1. Визначає об’єм клітини, основне середовище, транспорт речовин |
|
|
2. Висока діелектрична проникність |
2. Розчинник |
|
|
3. Високий поверхневий натяг |
3. Здатність до антигравітаційного руху |
|
|
4. Висока теплоємність |
4. Участь у терморегуляції |
- Формулювання висновку
Отже, виходячи з наведеної таблиці, ми ще раз можемо зазначити, що значення води у життєдіяльності організмів дуже велике і вона виконує такі функції:
• метаболічну;
• транспортну;
• терморегуляторну;
• механічну;
• є хімічним реагентом.
Запитання до учнів:
— Пригадайте з курсу 9-го класу, що таке водний баланс. (Водний баланс — це відношення кількості спожитої води до кількості виведеної. Для нормальної діяльності організму важливо, щоб надходження води повністю покривало витрати.)
- Повідомлення учня
Норми споживання води
Учені підрахували, що частину води (до 1,5 л) ми споживаємо з їжею і напоями, а близько 300 мл утворюється в самому організмі в результаті біохімічних процесів. Організму людини завдають шкоди як нестача води, так і її надлишок. Надмірне вживання води призводить до розрідження крові, що збільшує рівень навантаження на серцево-судинну систему, а зменшення концентрації шлункового соку спричиняє порушення травлення, посилене сечовиділення, що у свою чергу призводить до навантаження на нирки, тобто збільшується потовиділення і послаблюється весь організм. З виведенням поту і сечі відбувається інтенсивна втрата мікроелементів, яка порушує сольовий баланс організму. Цей механізм небезпечний тим, що нетривалі перевантаження водою можуть призвести до загальної стомлюваності організму, ослаблення м’язів і виникнення судом. Саме із цієї причини спортсменам на тренуваннях бажано не пити воду, а тільки полоскати ротову порожнину.
З організму вода виводиться такими шляхами (добова норма):
• через нирки — 1,5 л (48 %);
• із потом — 0,85 л (34 %);
• при диханні — 0,32 л (13 %);
• через кишечник — 0,13 л (5 %).
У нашому організмі є прекрасний індикатор нестачі води — відчуття спраги. Але треба розрізняти спрагу дійсну і помилкову. Перша зумовлена зменшенням вмісту води в крові через недостатнє надходження рідини або значну її втрату. Через рецептори судин сигнал про це передається в гіпоталамус, збудження якого викликає бажання пити. При псевдоспразі пересихає слизова оболонка ротової порожнини. Такий ефект виникає під час довгого читання вголос, при високій зовнішній температурі або в будь-яких стресових ситуаціях. Фізіологічної потреби у вживанні рідини в такі моменти немає. Достатньо прополоскати рот або просто зробити кілька ковточків води. У спеку ми втрачаємо багато рідини, а поповнювати запаси не встигаємо, що може призвести до зневоднення організму. Індикатором рівня зневоднення може бути колір і кількість сечі. Якщо сечі небагато і вона темно-жовтого кольору, це означає, що в організмі не вистачає запасів рідини і необхідно їх поповнити.
Навчитися правильно пити в спеку — не означає заливати в себе рідину «цистернами» або, навпаки, рахувати кожен ковток, дотримуючись яких-небудь йогівських практик. Ось кілька простих правил, дотримуючись яких, кожен зможе пережити спекотний літній день без шкоди для здоров’я. Для підтримки нормального водного балансу людині середнього зросту потрібно випивати як мінімум:
• 1,5 л — при середній температурі повітря 21 °С;
• 1,9 л — при температурі 26 °С;
• 3 л — при температурі 32 °С.
Корисного вам утамування спраги!
- Розповідь учителя
Вода, що використовується населенням для пиття і господарсько-побутових цілей, повинна відповідати певним гігієнічним вимогам, викладеним у Державних санітарних правилах і нормах (ДСанПіН) України № 383 1996 року «Вода питна. Гігієнічні вимоги до якості води централізованого господарсько-питного водопостачання».
Запитання до учнів:
— Як ви вважаєте, якою повинна бути питна вода згідно із санітарними вимогами?
Очікувані відповіді учнів:
Згідно з вимогами, доброякісна питна вода повинна:
1. Бути безпечною в епідемічному відношенні. Вода не повинна містити патогенних мікробів, вірусів та інших біологічних включень, небезпечних для здоров’я споживачів.
2. Бути нешкідливою за хімічним складом (хімічні речовини не повинні завдавати шкоди споживачеві або обмежувати використання води в побуті).
3. Мати хороші органолептичні властивості (бути прозорою, без кольору, не мати будь-якого присмаку або запаху).
4. Бути безпечною в радіаційному відношенні.
- Повідомлення учня
Органолептичні властивості води
Органолептичні властивості води зумовлені фізичними, хімічними і біологічними факторами.
Температура питної води повинна становити 8–12 °С. Така вода приємна на смак, освіжає, добре втамовує спрагу, швидко всмоктується і стимулює секреторну та моторну діяльність шлунково-кишкового тракту. Тепла вода п’ється неохоче, всмоктується повільніше, погано втамовує спрагу. Приймання її у великій кількості викликає неприємні відчуття і навіть нудоту. Краще спрагу втамовує прохолодна або гаряча вода, яка сприяє секреції слини і швидше всмоктується, ніж холодна або тепла. При будь-якій температурі найкраще задовольняє спрагу, посилюючи слиновиділення, міцний настій чаю. Пиття води, температура якої менша за 5 °С, викликає неприємні відчуття в порожнині рота, у тому числі зубний біль і може бути причиною переохолодження горла і рота. Близькою до оптимальної є температура води підземних джерел, що залягають на глибині 15–20 м і річні коливання температури якої не перевищують 2 °С. Це свідчить про добру захищеність води з поверхні ґрунту.
Людина віддає перевагу прозорій, без кольору, без неприємного запаху і присмаку питній воді. Вода не повинна містити водяних організмів, завислі частки або плаваючі плівки, які можна розрізнити неозброєним оком. Добра вода повинна бути прозорою на вигляд. Прозорість води характеризується її здатністю пропускати видиме світло і залежить від наявності в ній суспендованих частинок мінерального або органічного походження. Воду вважають достатньо прозорою, якщо через 30-сантиметровий шар води можна прочитати звичайний друкарський шрифт. Якість, протилежну прозорості, називають каламутністю. Каламутність води свідчить про забруднення її домішками ґрунту, стічними водами або про наявність недоліків в обладнанні криниць, свердловин. Дуже каламутна вода може призвести до подразнення слизової оболонки шлунка і кишок.
- Самостійне застосування учнями знань у стандартних ситуаціях
Практична робота № 1
Тема. Визначення вмісту води у власному організмі*.
Мета: навчитися обчислювати орієнтовний вміст води у власному організмі.
Обладнання: медичні ваги.
Хід роботи
1. Вимірювання маси тіла.
Виміряйте масу тіла за допомогою медичних ваг. Дані запишіть у зошиті.
2. Розрахуйте масу води у власному організмі, якщо відомо, що вона становить близько 70 % від маси тіла.
Маса води = маса тіла × 70 %.
3. Розрахуйте масу води у своєму організмі, поділивши свою масу тіла на 3 і помноживши результат на 2.
Маса води = Маса тіла / 3 × 2.
4. Порівняйте дані обох розрахунків.
5. Сформулюйте і запишіть висновок про значення води в організмі.
Дайте відповіді на запитання.
1. Від чого залежить вміст води в організмі?
2. Як залежить інтенсивність життєдіяльності клітини від кількості в ній води?


про публікацію авторської розробки
Додати розробку