Вступна контрольна робота з хімії 10 клас
Представлені 4 варіанти вступної контрольної роботи для учнів 10 класу у форматі ЗНО. Дозволяє оцінити залишковий рівень знань учнів після літніх канікул.
Вхідний тест
Варіант 1
П.І.Б. ___________________________________________________________
Клас 10-___ Дата__________________
- Обчисліть та вкажіть ступень окиснення Мангану у формулі калій перманганату. Наведіть розв’язок.
а) +2;
б) +4;
в) +7 ;
г) +5.
-
В якому напрямку відбудеться зсув хімічної рівноваги у системі при збільшені тиску Сl2 (г) + H2O (р)
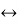
а) в бік утворення продуктів;
б) в бік утворення реагентів;
в) хімічна рівновага не зміститься.
3. Кисень у лабораторії можна добути реакцією розкладу:
а) CaCO3
б) KClO3
в) SiO2
г) H2SO4
Вкажіть рівняння даної реакції
- Газ, що одержали в процесі випалювання (взаємодії з киснем) халькопіриту CuFeS2 масою 14,72 г, перетворили на сульфатну кислоту. Обчисліть масу одержаної кислоти.
- Розв’яжіть окисно-відновну реакцію. Вкажіть окисник та відновник:
HIO3 + H2O2 = I2 + O2 ![]()
Розв’язок :
Відповідь:_______
Вхідний тест
Варіант 2
П.І.Б. ___________________________________________________________
Клас 10-___ Дата__________________
- Вкажіть ступені окиснення, які може виявляти атом Нітрогену в своїх сполуках:
а) -5; -3; +3; +5; +6; +7
б) -3; +2; +3; +4; +6; +7
в) -3; +1; +2; +3; +4 ; +5
г) -6; -3; +1; +4; +5; +7
-
В якому напрямку відбудеться зсув хімічної рівноваги у системі при зменшені тиску I2 (г) + 5CO2 (г)
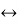
а) в бік утворення продуктів;
б) в бік утворення реагентів;
в) хімічна рівновага не зміститься.
- Вкажіть спосіб, яким можна розділити суміш метанолу та етанолу:
а) декантація
б) дистиляція
в) фільтрування
г) кристалізція
- До 200 г розчину калій гідроксиду з масовою часткою лугу 10,0 % додали калій оксид масою 4,7 г. Обчисліть масову частку речовини в одержаному розчині.
- Розв’яжіть окисно-відновну реакцію. Вкажіть окисник та відновник:
MnO2 + HCl = Cl2 ![]()
Розв’язок :
Відповідь:_______
Вхідний тест
Варіант 3
П.І.Б. ___________________________________________________________
Клас 10-___ Дата__________________
- Унаслідок електролітичної дисоціації кислотні залишки мають заряд:.
а) не мають заряду;
б) завжди негативний, що чисельно дорівнює їх валентності;
в)завжди позитивний, що чисельно дорівнює їх валентності ;
г) залежно від концентрації розчину – позитивний або негативний.
- Вкажіть рівняння реакції, на рівновагу якої не вплине підвищення тиску:
а) CO(г) + H2O (г) ![]()
б) 2NO2(г) ![]()
в) N2(г) + 3H2(г) ![]()
г) 4HCl(г) + O2(г) ![]()
- Виберіть речовини Х1 та Х2 для здійснення перетворень за схемою:
CaCO3 ![]() X1
X1 ![]() Х2
Х2 ![]()
а) CaSO4 , CaF2
б) CaO, CaSO4
в) CaCl2, Ca(OH)2
г) CaO, Ca(OH)2
- Залізну пластинку масою 5,2 г протягом тривалого часу витримували в розчині, що містив 1,6 г купрум сульфату (II). Після закінчення реакції пластинку вийняли з розчину й висушили. Яка її маса?
- Розв’яжіть окисно-відновну реакцію. Вкажіть окисник та відновник:
CuCl2 + SO2 + H2O = CuCl + H2SO4 + HCl
Розв’язок :
Відповідь:_______
Вхідний тест
Варіант 4
П.І.Б. ___________________________________________________________
Клас 10-___ Дата__________________
- Вкажіть формулу сахарози:
а) C6H12O6
б) C12H22O11
в) (C6H10O5)n
г) C2H5OH
-
В якому напрямку відбудеться зсув хімічної рівноваги у системі при збільшені тиску С (тв) + 2N2O (г)
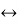
а) в бік утворення продуктів;
б) в бік утворення реагентів;
в) хімічна рівновага не зміститься.
- Вкажіть назву речовини:
а) склянка
б) магній
в) залізний цвях
г) магніт
Вкажіть рівняння даної реакції
- Обчисліть масові частки речовин у розчині, що утворився в результаті дії 25 мл розчину, в якому масова частка хлороводню 20% (густина 1,1 г/мл), на ферум (II) сульфід масою 4,0 г.
- Розв’яжіть окисно-відновну реакцію. Вкажіть окисник та відновник:
KMnO4 + PH3 + H2SO4 = H3PO4+ K2SO4+ MnSO4+ H2O
Розв’язок :
Відповідь:_______


про публікацію авторської розробки
Додати розробку
