Історичні відомості про спроби класифікації хімічних елементів
Розробка уроку висвітлює питання спроб класифікації хімічних елементів. Під час розробки уроку використані різні методи та прийоми, зокрема "Мікрофон" та "Переказ по колу". Також використана презентація.
Тема. Історичні відомості про спроби класифікації хімічних елементів
Недостатньо тільки хотіти – потрібно діяти.
В.О.Сухомлинський.
Мета: сформувати поняття “системи”, повторити першу класифікацію елементів, ознайомити учнів із іншими способами класифікації, підготувати учнів до свідомого сприйняття періодичного закону; продовжувати формувати науковий світогляд на основі знань про класифікації хімічних елементів; розвивати хімічну мову, мислення, увагу, уміння аналізувати, пізнавальну діяльність.
Методи: розповідь, бесіда, демонстрація слайдів, гра.
Обладнання: комп’ютер, проектор.
Тип уроку: засвоєння нових знань.
Хід уроку
І. Організаційний момент.
ІІ. Актуалізація опорних знань і чуттєвого досвіду учнів.
* Бесіда за слайдами.
1. (див. слайд 1) Де було створено такі символи хімічних елементів? (Стародавній Єгипет)
 (слайд 1)
(слайд 1)
2. (див. слайд 2) Хто запропонував ці символи елементів (1-ша колонка – алхіміки, 2-га колонка – Дальтон, 3-тя – Берцеліус)?
 (слайд 2)
(слайд 2)
3. (див. слайд 3) Кому належить дана класифікація хімічних елементів? (Лавуазьє)
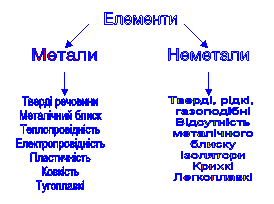 (слайд 3)
(слайд 3)
ІІІ. Мотивація навчальної діяльності учнів.
* Прийом “Мікрофон”
Учні за допомогою “мікрофона” та навідних питань формують позитивну мотивацію для вивчення цієї теми.
1. Що таке класифікація? (Класифікація – це створення чіткої системи явищ, рослин, тварин і т.д., яка передбачає їх групування за певними ознаками).
2. Чи необхідна вона? Якщо так, то для чого її необхідно знати? (Так, вона необхідна, оскільки дає змогу розподілити об’єкти класифікації за певними ознаками та полегшує процес їх вивчення).
3. Назвіть одну із найважливіших класифікацій в хімії. Для чого її необхідно знати? (Періодична система хімічних елементів. Вона дає змогу зрозуміти та передбачити властивості хімічних елементів та їх сполук).
Після цього учні самостійно формулюють мету і завдання уроку.
IV. Вивчення нового матеріалу
* Гра “Переказ по колу”
Учні читають текст параграфа. Потім стають у коло. Обирають першого, хто почне переказ, і починають переказувати: кожен учень має право висловити лише одне речення (одну фразу). По черзі всі додають свої речення, розкриваючи зміст прочитаного тексту. Коли учні розповідають про класифікації Деберейнера, Ньюлендса і Мейєра – учитель демонструє слайди із їх класифікацією, що дає змогу учням наочно побачити творіння цих вчених (див. слайди 4 – 7)
![]()
![]()
(слайд 4)
 (слайд 5)
(слайд 5)
![]()

(слайд 6)
Як ви гадаєте:
Чому Мейєр не зумів завершити створення періодичної системи? (Мабуть тому, що не зміг правильно пояснити таке розташування елементів).
Ось, що з цього приводу говорив сам вчений.
“ Я склав свою таблицю з 28 хімічних елементів, але чесно зізнаюся, що в мене не вистачило сміливості для таких припущень, які впевнено висловив Дмитро Іванович Менделєєв”. (Лотар Мейєр)
 (слайд 7)
(слайд 7)
Потім вчитель доповнює новими фактами сказане учнями.
* Розповідь учителя.
У 1858 р. англійський хімік У. Одлінг опублікував таблицю елементів, у горизонтальних рядках якої елементи здебільшого розміщені за принципом хімічної подібності (аналогії). Для однієї частини елементів визначена їх атомна маса, для іншої – значення хімічного еквівалента. Така двоїстість кількісної характеристики елементів не давала змоги виявити зв'язок хімічних властивостей елементів з їх атомною масою.
У 1862 р. французький учений Б. Шанкуртуа, щоб виявити зв'язок між атомною масою і властивостями елементів, запропонував розташувати елементи по спіральній лінії, намотаній на поверхню циліндра під кутом 45°. Узявши число 16 як таке, що визначає різницю між атомними масами аналогічних елементів, він поділив бічну поверхню циліндра на 16 рівних частин. На спіралі він проставив символи елементів на відстані один від одного в масштабі, що відповідав їх атомній масі. Подібні елементи, на думку Шанкуртуа, повинні були розміститися один над одним і повторюватись через кожні 16 поділок. Це була спроба показати за допомогою атомної маси зв'язок між елементами. На основі цього можна було припустити наявність періодичної залежності між властивостями елементів.
Крім названих вище вчених, спробами класифікації елементів займалися, наприклад, такі хіміки, як М. М. Соколов (Росія), Ж. Дюма (Франція), Д. Кук (США), М. Петтенкофер (Німеччина), Д. Гладстон (Англія) та ін. Причиною обмеженості спроб систематизації хімічних елементів до Д. І. Менделєєва було те, що всім цим ученим бракувало найголовнішого ‒ широкого теоретичного мислення природознавців, бо саме з його допомогою можна було піднестися від одиничного (елемента) через особливе (група подібних елементів) до загального (періодичної системи).
Незважаючи на це, спроби систематизації елементів до Менделєєва також мали певне значення для створення науково обґрунтованої системи елементів, для відкриття періодичного закону.
V. Узагальнення і систематизація знань.
* Прийом “Мікрофон”.
Учні по черзі дають відповіді, доповнюючи один одного.
Давайте пригадаємо:
1. Про які класифікації хімічних елементів ви дізналися сьогодні? (Деберейнера, Одлінга, Шанкуртуа, Ньюлендса, Мейєра).
2. Що хорошого було в цих системах, а що неправильного? (Деберейнер розташував у групи елементи подібні за своїми властивостями, але елементи були розміщені по групам не всі, і не було пояснено причини такого розташування.
Одлінг розмістив у групах елементи теж подібні за своїми властивостями, але для однієї частини елементів визначив атомні маси, а для іншої – хімічні еквіваленти.
Шанкуртуа створив занадто важку для сприйняття таблицю, хоча і на одній лінії опинилися подібні елементи.
Ньюлендс не зумів знайти підтвердження своєму “правилу октав”, хоча початок був правильним, але довести його до логічного завершення він не зумів.
Мейєр побоявся зробити такі припущення, які зробив Менделєєв у своїй класифікації).
VI. Домашнє завдання § 26 вивчити, вправа 3-4 ст. 121. Повторити основні класи неорганічних сполук та їх властивості. Декілька учнів отримують завдання створити презентацію на тему “Історія відкриття періодичного закону”.


про публікацію авторської розробки
Додати розробку
