Вступ до органічної хімії
Про матеріал
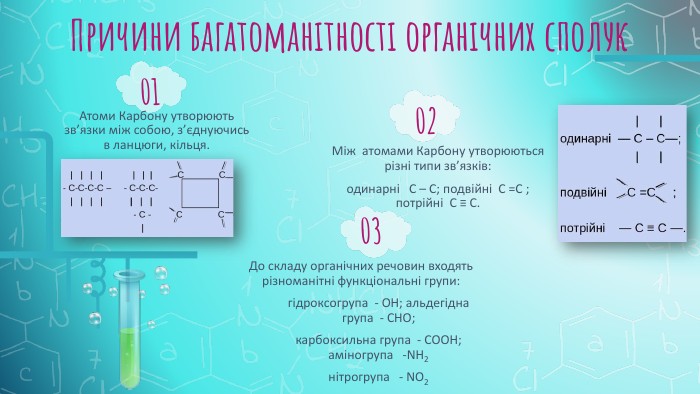
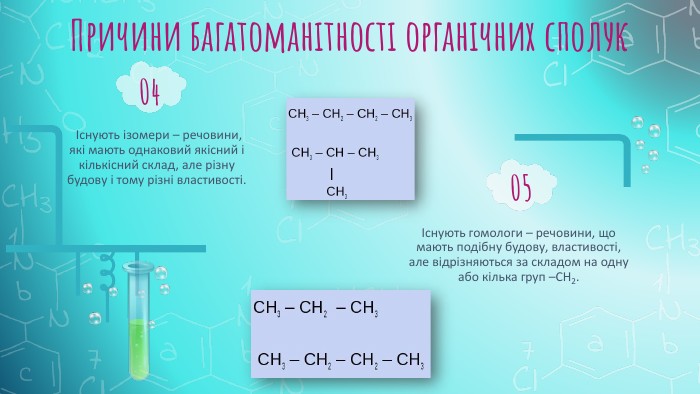
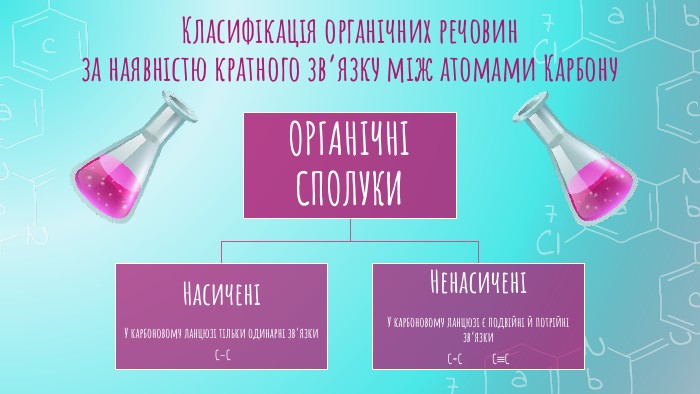
Ознайомити учнів з предметом вивчення органічної хімії, розмаїттям органічних сполук; розглянути подібні і відмінні ознаки органічних і неорганічних сполук, поняття «елементи - органогени»; розкрити особливості органічних сполук порівняно з неорганічними; ознайомити учнів з короткою історією розвитку органічної хімії. Розвивати вміння зіставляти і порівнювати, робити виновки. Виховувати інтерес до вивчення хімії. Перегляд файлу
Зміст слайдів
Середня оцінка розробки
Оцінки та відгуки
pptx
До підручника
Хімія 9 клас (Григорович О.В.)
Оцінка розробки

Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку