Методичні вказівки та інструкція до теми «Титриметричний аналіз»
Методичні вказівки та інструкція до виконання лабораторних робіт з дисципліни «Аналітична хімія та інструментальні методи» розроблені для студентів спеціальності 161 «Хімічні технології та інженерія» . Даний посібник рекомендований для виконання лабораторних робіт з теми «Титриметричний аналіз». Посібник містить наглядні схеми, що допоможуть студенам зрозуміти методику титрування при розгляді теми «Титриметричний аналіз».
МІНІСТЕРСТВО ОСВІТИ І НАУКИ УКРАЇНИ
ІНДУСТРІАЛЬНИЙ КОЛЕДЖ
Державного вищого навчального закладу
«Український державний хіміко-технологічний університет»
Методичні вказівки та інструкція
до теми «Титриметричний аналіз»
з дисципліни: «Аналітична хімія та інструментальні методи»
спеціальності 5.05130109 «Виробництво тугоплавких неметалевих і силікатних матеріалів і виробів»
Розробив
викладач першої категорії Г.С. Карпова
м. Кам’янське- 2018р.
Анотація
Методичні вказівки та інструкція для виконання лабораторних робіт з дисципліни «Аналітична хімія та інструментальні методи» розроблені для студентів спеціальності 5.05130109 «Виробництво тугоплавких неметалевих і силікатних матеріалів і виробів».
Даний посібник рекомендований для виконання лабораторних робіт з теми «Титриметричний аналіз». Посібник містить наглядні схеми, що допоможуть студенам зрозуміти методику титрування при розгляді теми «Титриметричний аналіз», а також в подальшому при виконанні лабораторних робіт.
Титриметричний аналіз —
сукупність методів кількісного аналізу в аналітичній хімії, засновані на вимірі
об'єму розчину реактиву відомої концентрації, що витрачається для реакції з визначуваною речовиною.
Титрування — процес визначення титру досліджуваної речовини.
Титр — це концентрація розчину, яка виражається відношенням маси розчиненої речовини до об'єму розчину, розмірність г/мл, розраховується за формулою:
T = Се · Em/1000, де Се — концентрація еквіваленту (нормальність розчину), Em — мольна маса еквіваленту розчиненої речовини.
Титрування проводять в бюретках, заповнених титрантом до нульової відмітки. Титрувати, починаючи від інших відміток, не рекомендується, оскільки шкала бюретки може бути нерівномірною. Заповнення бюреток робочим розчином здійснюють через лійку або за допомогою спеціальних пристосувань, якщо бюретка напівавтоматична. Кінцеву точку титрування (точка еквівалентності) зазвичай знаходять за допомогою відповідного індикатора або інструментально.
Розрізняють типи титрування: пряме, зворотне титрування і титрування замісника (замісникове).
При прямому титруванні до розчину визначуваної речовини (аліквоти або навіски, титрованого розчину) додають невеликими порціям розчин титрант (робочий розчин).
При зворотному титруванні до розчину визначуваної речовини додають спочатку явний надлишок спеціального реагенту і потім титрують його залишок, що не вступив в реакцію.
При титруванні замісника до розчину визначуваної речовини додають спочатку явний надлишок спеціального реагенту і потім титрують один з продуктів реакції між аналізованою речовиною і доданим реагентом.
Титрант (Т) — розчин реагенту, молярна концентрація еквіваленту якого встановлена з великою точністю, називають робочим розчином (стандартним розчином). Аналіт (А) (проба) — розчин в якому визначають концентрацію речовини.
Як титрувати
КРОКИ
ЩО ВАМ ЗНАДОБИТЬСЯ
- Титрант в надлишковій кількості.
- Точно відведені кількість аналіта.
- Колірний індикатор (наприклад фенолфталеїн)
- Відкалібрована бюретка (розмір залежатиме від того, скільки використовується титранту)
- Штатив для бюретки.
- Лабораторний стакан або колба Ерленмейера
- Паперові серветки
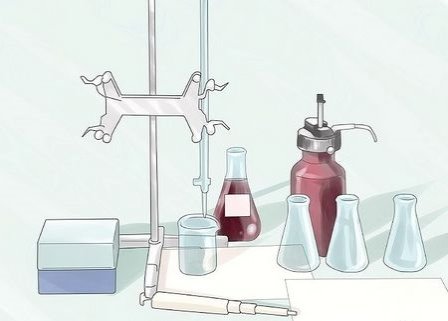
1
Візьміть предмети і реактиви, перелічені в розділі "Що вам знадобиться".
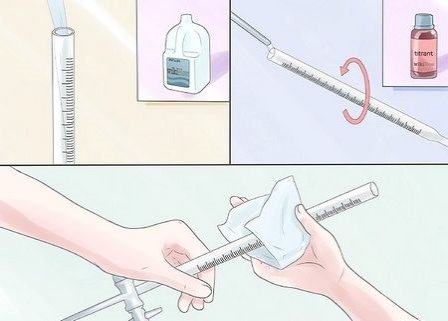
2
Промийте бюретку і вилийте воду.
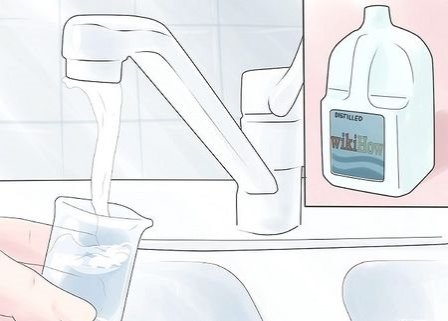
3
Промийте і сполосніть весь скляний посуд водопровідною водою (краще використовувати деіонізовану H2O, якщо вона є). З бюретками будьте дуже обережні - вони дуже крихкі. Завжди утримуйте їх обома руками.
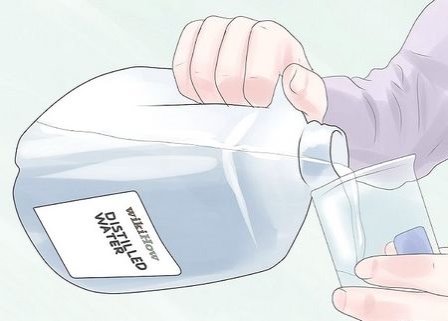
4
Сполосніть весь скляний посуд дистильованою водою, щоб знизити ймовірність забруднення.

5
Відміряйте точну кількість аналіту (реагент, змішаний з визначуваною речовиною).
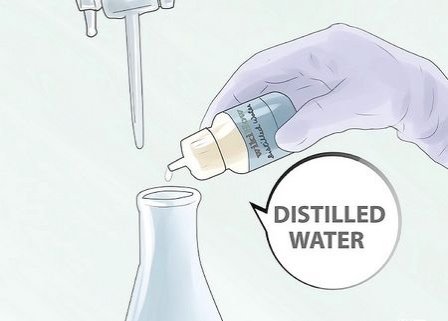
6
Налийте в склянку або колбу Ерленмейера невелику кількість дистильованої води.

7
Змийте аналіт в лабораторний стакан або колбу Ерленмейера, щоб весь він потрапив в стакан.
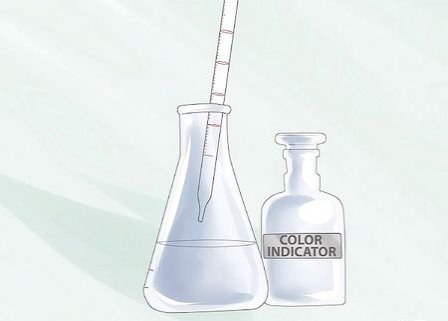
8
Помістіть в лабораторний стакан невелика кількість (4-5 крапель) відповідного кольорового індикатора.
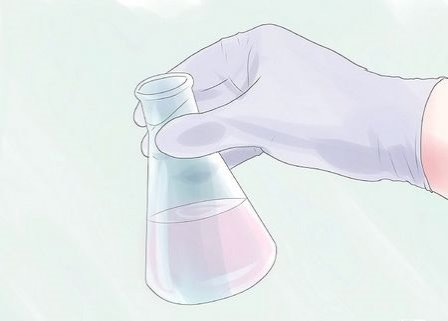
9
Перемішайте вміст склянки за допомогою збовтування.

10
Налийте в бюретку титрант в надмірній кількості (речовини, які реагують з аналітом). Титрант повинен бути у формі розчину.
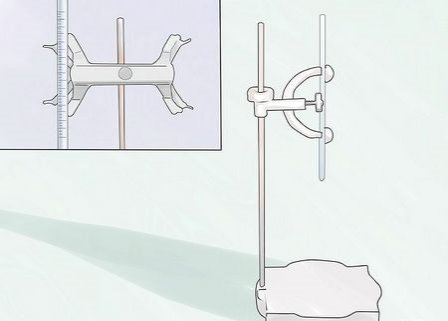
11
Обережно зафіксуйте бюретку на штативі. Кінчик бюретки не повинен торкатися ніякої поверхні.
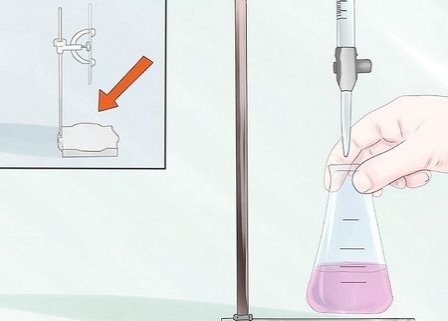
12
Поставте під бюретку лабораторний стакан.

13
Зафіксуйте початковий об`єм розчину в бюретці на рівні меніска (сама нижня частина поглиблення у верхній частині рідини).
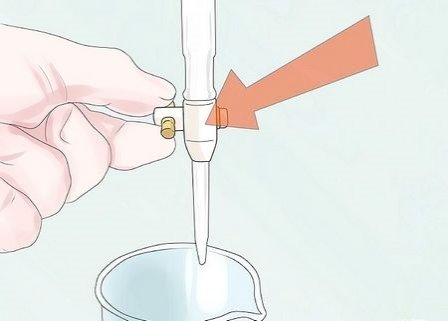
14
Поверніть краник бюретки (розташований біля кінчика) у вертикальне положення, щоб титрант полився в стакан. Дозвольте витекти лише невеликій кількості титранту. Повинна відбутися зміна кольору. Перемішайте вміст склянки, поки колір не зникне.
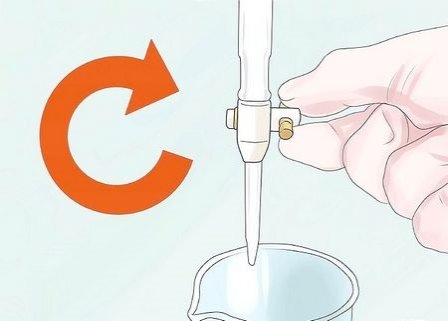
15
Повторіть попередній крок, поки злегка змінений колір не буде зберігатися (ця зміна буде ледь помітною, тому будьте дуже уважні і дійте повільно).

16
Запишіть об`єм розчину в бюретці.
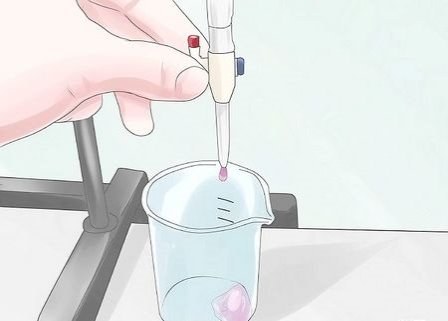
17
Наближаючись до точки еквівалентності, додавайте титрант по краплях.

18
Після кожної краплі перемішуйте вміст склянки.
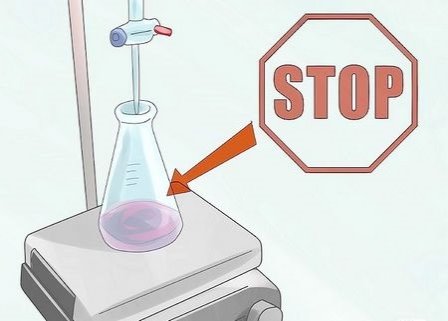
19
Коли ви досягнете точки еквівалентності, яка є точкою, в якій реагент в аналізі повністю нейтралізований, припиняйте додавати титрант. Ви зможете визначити момент досягнення точки еквівалентності по зміні кольору, яка буде залежати від використовуваного вами індикатора.

20
Запишіть кінцевий об`єм.
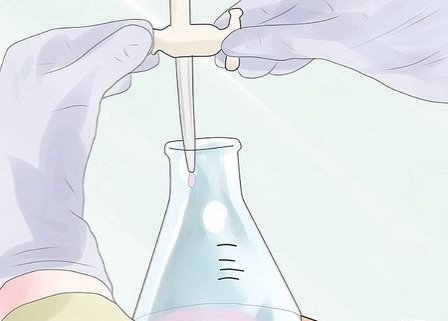
21
Додавайте краплі титранту, поки не пройдете точку еквівалентності. При цьому вміст лабораторної склянки буде того ж кольору, що і колір індикатора при додаванні титранту.
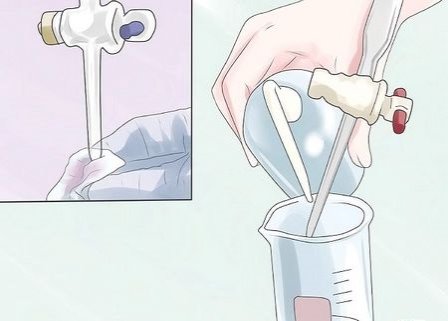
22
Витріть воду, що залишилася на посуді.

23
Вилийте всі використані реактиви в марковану тару для зливу.

24
Обчисліть концентрацію реагенту в аналіті за допомогою отриманих даних.
ПОРАДИ
- Точку еквівалентності можна з легкістю проморгати, тому будьте обережні і спостережливі. Коли у вас з`явиться найменша відчуття, що ви наближаєтеся до точки еквівалентності, почніть відлік крапель і дійте якомога повільніше.
- Розташуйте очі на тому ж рівні, що і рівень розчину в бюретці, - якщо ваші очі кожного разу будуть вище або нижче рівня рідини, то отримані дані будуть неточними.
- Розрахунок концентрації слід проводити до потрібної кількості значущих розрядів.
- Визначити, чи досягнута точка еквівалентності, буде легше, якщо ви помістите під конічну колбу білий папір, щоб зміна кольору індикатора була більш помітною.
- Не забудьте витягнути фільтр-воронку після того, як ви заповните бюретку титрантом, інакше результати титрування НЕ будуть ідеально точними.
- Користуйтеся бюреткою обережно, - вона легко може розбитися.
- На колбу з водою і розчином визначаємої речовини покладіть предметне скло за час, протягом якого ви будете виконувати титрування, їх молярность може помінятися.
- Записуйте об`єм розчину в бюретці за один розряд до зазначеного (наприклад, якщо на бюретці відзначені десятий, то вам потрібно записувати результати до найближчих сотих).
- Покладіть на верхівку бюретки перевернутий стакан, особливо якщо ви тітруете з NaOH- якщо його залишити контактувати з повітрям, деяка частина OH утворює зв`язок з молекулами води і порушить молярность розчину NaOH.
ПОПЕРЕДЖЕННЯ
- Не вживайте реагенти в їжу.
- Обов`язково промийте весь аналіт в стакан. Будь-яка його кількість, яка залишиться в чаші ваг або тарі призведе, до погрішностей.
- Не виливайте будь-які реактиви в раковину - лише у відповідну промарковану тару для зливу.
Список використаних джерел
1.А. Барсукова Аналитическая химия М.: «Высшая школа», 1990 г.
2. М.Є. Полесс И.М. Душечкина Аналитическая химия М.: «Медицина», 1987 г.
3. С.А. Шапиро, Я.А. Гурвич Аналитическая химия М.: «Высшая школа», 1973 г.
4.
http://ru.wikihow.com/%D1%82%D0%B8%D1%82%D1%80%D0%BE%D0%B2%D0%B0%D1%82%D1%8C.
5. https://uk.wikipedia.org/wiki/%D0%A2%D0%B8%D1%82%D1%80%D0%B8%D0%BC%D0%B5%D1%82%D1%80%D0%B8%D1%87%D0%BD%D0%B8%D0%B9_%D0%B0%D0%BD%D0%B0%D0%BB%D1%96%D0%B7


про публікацію авторської розробки
Додати розробку
