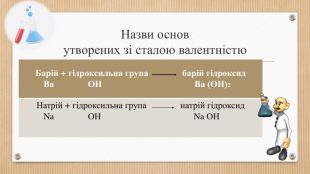
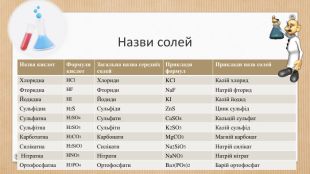
Основні класи неорганічних сполук. Класифікація сполук, їхні склад і номенклатура.
Про матеріал
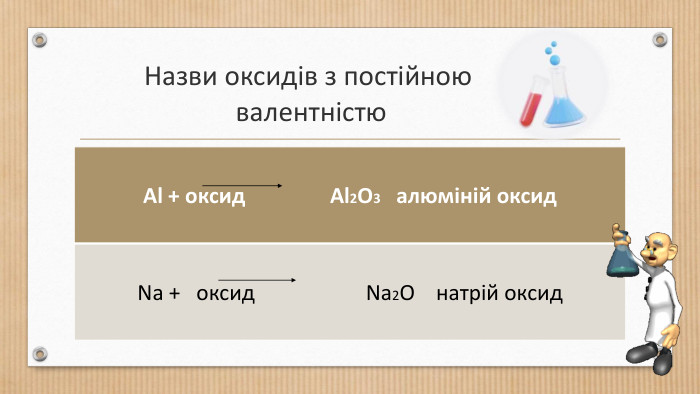
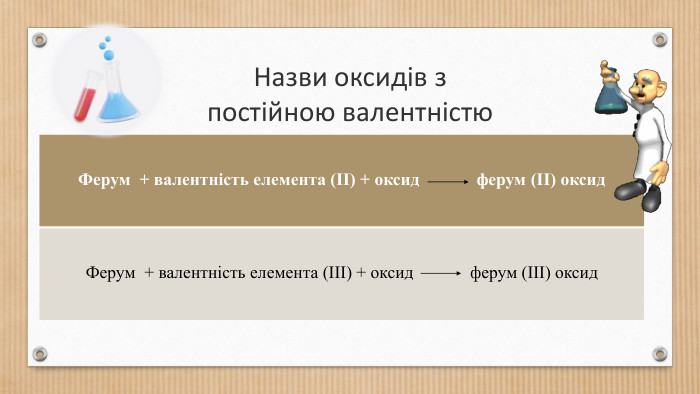
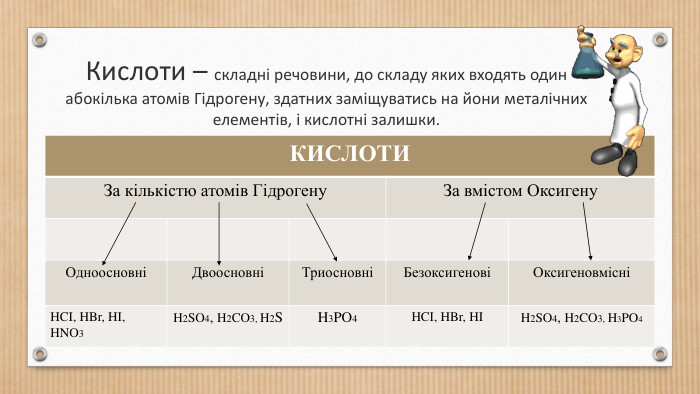
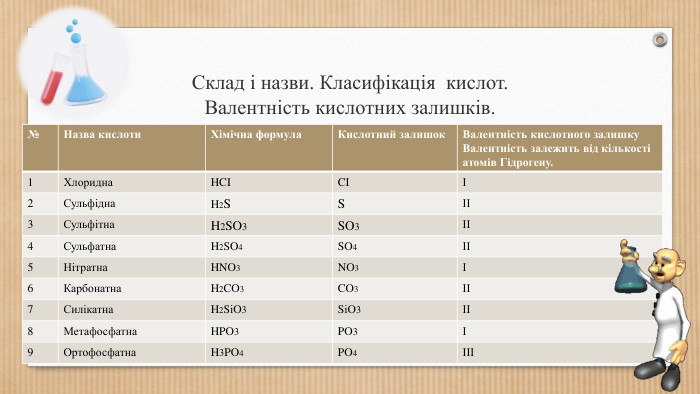
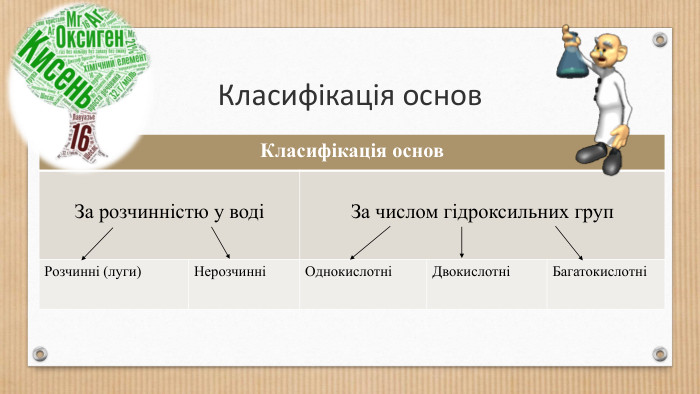
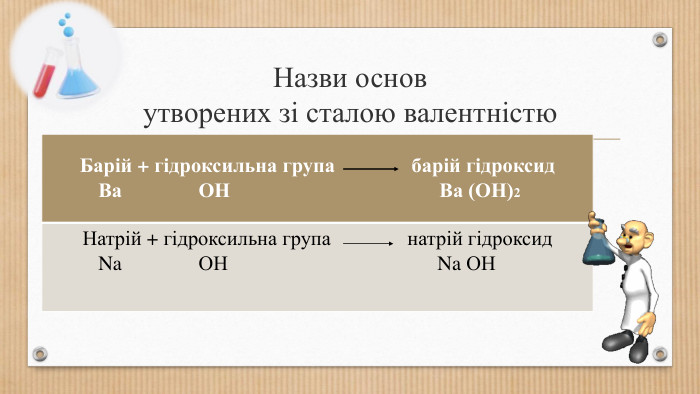
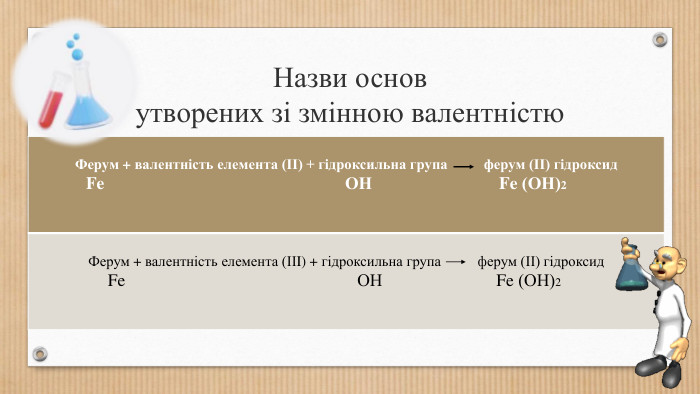
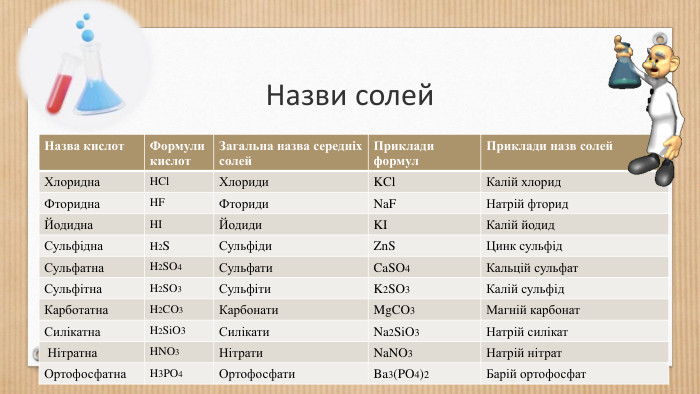
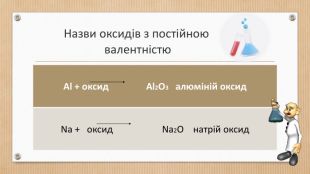
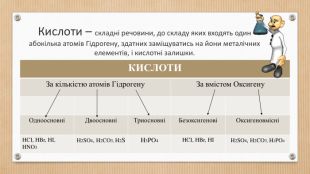
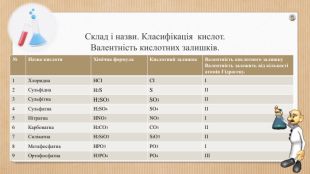
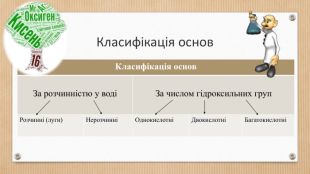
Основні класи неорганічних сполук. Класифікація сполук, їхні склад і номенклатура.
Класифікація оксидів, кислот, основ,Ю солей. Перегляд файлу
Зміст слайдів


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку