Правило "коромисло Івашини" - новий спосіб розв'язування задач при змішуванні розчинів.
В наш час, час швидких технологічних змін дуже поважають та цінують людей, які можуть вирішити проблему, використовуючи різні способи, які здатні в складній ситуації оцінити широко, масштабно задачу та розв’язати її.
В своїй роботі, як вчитель, я завжди націлюю дітей на те, що кожну справу треба доводити до кінця; кожне завдання треба виконувати вірно; із усіх варіантів вирішення проблеми використовувати найкоротший та найпростіший спосіб.
Хімія – це цікава, але не проста наука, з нею можуть потоваришувати не всі люди. Та в мене є мета – зробити так, щоб хімія була зрозумілою більшій кількості людей, ніж зараз.
При розв’язуванні задач завжди є декілька варіантів, щоб знайти рішення. Способи ров’язку не завжди є простими і зрозумілими.
В цій роботі я хочу всім запропонувати спосіб розв’язування задач пов’язанних з приготуванням розчинів з певною відсотковою концентрацією, використовуючи правило, яке назвав «коромисло Івашини». Для цього розв’яжемо декілька задач, використовуючи відомі раніше (стандартні) способи та правило, що було вказано вище. Але спочатку вкажемо величини, що будуть використовуватись при розв’язанні.
m1 – маса розчину, що буде змішуватись у якого концентрація менша або це може бути маса води, якщо її використовують для приготування нового розчину.
w1% – масова частка розчиненої речовини у першому розчині (якщо m1 – це маса води, то w1%(р.р.) = 0%).
m2 – маса розчину, що буде змішуватись у якого концентрація більша, або це може бути маса розчиненої речовини, якщо її використовують для приготування нового розчину.
w2% – масова частка розчиненої речовини у другому розчині (якщо m2 – це маса розчиненої речовини, що добавляють для підвищення концентрації, то w2%(р.р.) = 100%).
m3 – маса розчину, що утворюється при змішуванні першого та другого.
w3% – масова частка розчиненої речовини в утвореному розчині.
Задача №1
За одним з рецептів для приготування смачної страви з м’яса необхідно до 1 кг м’яса добавити 150 г розчину оцтової кислоти з відсотковою концентрацією 18%. Приготуйте необхідну кількість потрібного розчину для замочування 5 кг м’яса. Для цього можна використовувати 9%-вий та 60%-вий розчини оцтової кислоти.
Розв’язання
Спосіб №1 (стандартний)
Як зрозуміло з умови задачі необхідно приготувати 5×150 г = 750 г 18%-вого розчину. Позначемо масу цього розчину - m3.
Наше завдання визначити маси 9%-вого та 60%-вого розчинів, що необхідно взяти для приготування розчину m3. Позначимо відповідно їх маси m1 та m2. Надамо значення розчинам m1 та m2: m1=x, m2=y.
Враховуючи це запишемо:
m1 + m2 = m3, або x + y = 750.
Знаходимо масу оцтової кислоти, що міститься в третьому розчині:
m3(CH3COOH) = w3(CH3COOH)×m3 = 0,18×750 = 135 (г)
Відповідно знайдемо маси оцтової кислоти, що містяться в першому та другому розчині:
m1(CH3COOH) = w1(CH3COOH)×m1 = 0,09x
m2(CH3COOH) = w2(CH3COOH)×m2 = 0,6y
Оскільки
m1(CH3COOH) + m2(CH3COOH) = m3(CH3COOH), то
0,09x + 0,6y = 135
Таким чином можна скласти систему рівнянь з двома невідомими:
![]() x + y = 750
x + y = 750
0,09x + 0,6y = 135;
Розв’яжемо її:
![]() x = 750 - y
x = 750 - y
0,09 (750 - y)+ 0,6y = 135;
0,09 (750 - y)+ 0,6y = 135
67,5 – 0,09y + 0,6y = 135
0,51y = 67,5
y = 132,35
x = 750 – y = 750 – 132,35 = 617,65
Отже m1 = 617,65 г, m2 = 132,35 г.
Спосіб №2
Скористаємось правилом «коромисло Івашини». Для цього зобразимо відрізок в якому початковим значенням буде відсоткова концентрація першого розчину, а кінцевим – відсоткова концентрація другого розчину:
![]()
Між цими значеннями зобразимо і відсоткову концентрацію третього розчину:
![]()
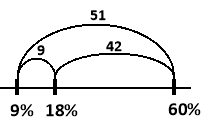 Вкажемо довжину утворенних відрізків:
Вкажемо довжину утворенних відрізків:
Таким чином вклад першого розчину в утворення третього складає ![]() частин, а вклад другого розчину -
частин, а вклад другого розчину - ![]() частин, тому
частин, тому
![]()
![]()
Перевага способу №2 полягає в тому, що для розв’язання задачі не треба вводити ніяких змінних, не треба розв’язувати рівняння при розрахунках яких діти часто роблять помилки.
Задача №2
Яку масу води та 30%-вого розчину натрій хлориду (NaCl) необхідно взяти для приготування 400 г 12%-вого розчину натрій хлориду?
Розв’язання
Задачу розв’язуємо використовуючи правило «коромисло Івашини».
m1 – маса води
m2 – маса 30%-вого розчину
m3 – маса розчину, що необхідно приготувати
Врахуємо, що у чистій воді масова частка розчиненої речовини становить 0%.
Складаємо відрізки та знаходимо їх довжини:
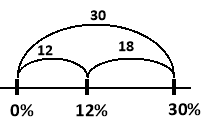
![]()
![]()
Відповідь: m1 = 240 г, m2 = 160 г.
Задача №3
Яку масу 25%-вого розчину калій нітрату та сухої солі калій нітрату необхідно взяти для приготування 500г розчину з масовою часткою калій нітрату – 42%.
Розв’язання
![]() – маса 25%-вого розчину, що необхідно взяти
– маса 25%-вого розчину, що необхідно взяти
![]() – маса сухого KNO3,що необхідно додатково розчинити
– маса сухого KNO3,що необхідно додатково розчинити
![]() – маса 42%-вого розчину
– маса 42%-вого розчину
Врахуємо, що в сухій солі масова частка розчиненої речовини 100%
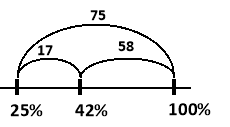 Складаємо відрізки та знаходимо їх довжини:
Складаємо відрізки та знаходимо їх довжини:
![]()
![]()
Відповідь: m1 = 386,67 г, m2 = 113,33 г.
«Коромисло Івашини» також можна використовувати для виконання розрахунків при розчиненні у воді або у готових розчинах кристалогідратів. Вказаний спосіб дуже спрощує розрахунки. Кристалогідрати – це сухі на дотик речовини, але в своєму складі вони містять воду, тому до них слід відноситись як до твердих розчинів.
Задача №4
Яку кількість 20%-вого розчину купрум (ІІ) сульфату (CuSO4) та мідного купоросу (CuSO45H2O) необхідо взяти для приготування 400 г розчину купрум (ІІ) сульфату (CuSO4) з масовою часткою розчиненої речовини 36%?
Розв’язання
Спочатку необхідно знайти масову частку купрум (ІІ) сульфату в мідному купоросі:
Mr(CuSO45H2O) = Mr(CuSO4) + 5Mr(H2O) = 160 + 5×18 = 250
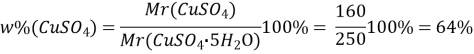
Далі використовуємо правило «коромисло Івашини»:
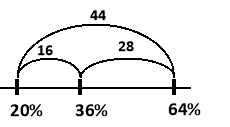
![]()
![]()
Відповідь: m1 = 254,55 г, m2 = 145,45 г.
Задача №5
Скільки води та залізного купоросу слід узяти для приготування 300г 25%-вого розчину ферум(II) сульфату(FeSO4)?
Розв’язання
Знаходимо масову частку FeSO4 в залізному купоросі:
Mr(FeSO4 7H2O) = Mr(FeSO4)+7Mr(H2O) = 152+7×18 = 278
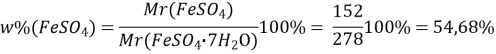
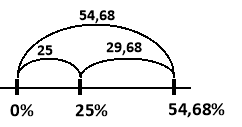
![]()
![]()
Таким чином необхідно взяти 162,84 г води та 137,16 г залізного купоросу.
Висновок
В заключній частині давайте ще раз розглянемо алгоритм використання правила «коромисло Івашини»:
- Будуємо відрізок на якому вказуємо відсоткові конценрації обох розчинів, що змішуються:
![]()
-
 В середній частині утвореного відрізку вказуємо значення відсоткової концентрації нового (третього) розчину:
В середній частині утвореного відрізку вказуємо значення відсоткової концентрації нового (третього) розчину:
- Визначаємо довжини трьох відрізків:
-
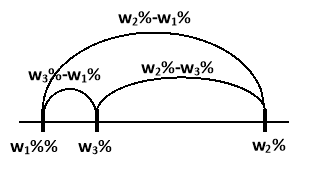 Використовуємо формули для знаходження мас змішуваних розчинів:
Використовуємо формули для знаходження мас змішуваних розчинів:
![]()
![]()
P.S.
Колеги, якщо когось з вас зацікавив вказаний спосіб розв’язування задач, використовуючи правило «коромисло Івашини» та виникли запитання звертайтесь за електронною адресою igor19701970@ukr.net
Бажаю успіхів! З повагою Івашина Ігор Іванович.

про публікацію авторської розробки
Додати розробку
