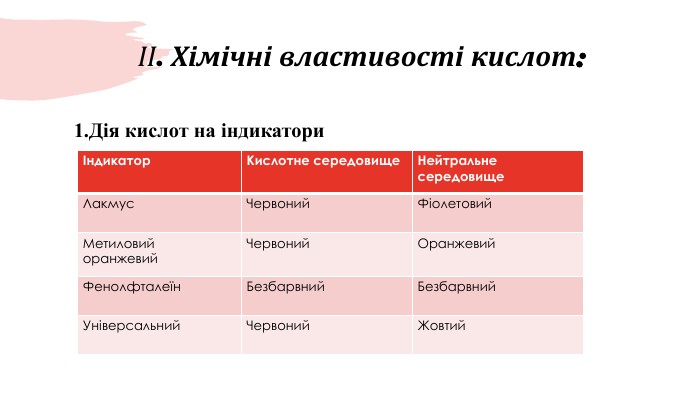
Презентація до уроку "Хімічні властивості кислот"
Про матеріал
В даній презентації містяться рівняння реакцій, що підтрерджують хімічні властивості кислот, а також різні завдання для узагальнення знань учнів. Перегляд файлу
Зміст слайдів

Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку