Презентація до уроку: "Солі. Фізичні властивості солей"





















Солі - складні речовини, що складаються з атомів металічних елементів і кислотних залишків. Алгоритм складання формули солі: 1. Записуємо символ металічного елемента на першому місці і кислотного залишку. Na PO42. Вказуємо валентності. ІІІІ3. Обчислюємо найменше спільне кратне для значень валентностей. 34. Знаходимо індекси, поділивши найменше спільне кратне на значення валентностей. 3 Al SO4 Н2 SO4ІІІІІ
Солі - складні речовини, що складаються з атомів металічних елементів і кислотних залишків. Алгоритм складання формули солі: 1. Записуємо символ металічного елемента на першому місці і кислотного залишку. Na PO42. Вказуємо валентності. ІІІІ3. Обчислюємо найменше спільне кратне для значень валентностей. 34. Знаходимо індекси, поділивши найменше спільне кратне на значення валентностей. 3 Al SО4ІІІІІ62
Солі - складні речовини, що складаються з атомів металічних елементів і кислотних залишків. Алгоритм складання формули солі: 1. Записуємо символ металічного елемента на першому місці і кислотного залишку. Na PO42. Вказуємо валентності. ІІІІ3. Обчислюємо найменше спільне кратне для значень валентностей. 34. Знаходимо індекси, поділивши найменше спільне кратне на значення валентностей. 3 Al (SО4) ІІІІІ623
Солі - складні речовини, що складаються з атомів металічних елементів і кислотних залишків. Алгоритм складання формули солі: 1. Записуємо символ металічного елемента на першому місці і кислотного залишку. К СO32. Вказуємо валентності. ІІІ3. Обчислюємо найменше спільне кратне для значень валентностей. 24. Знаходимо індекси, поділивши найменше спільне кратне на значення валентностей. 2 Н2 СO3
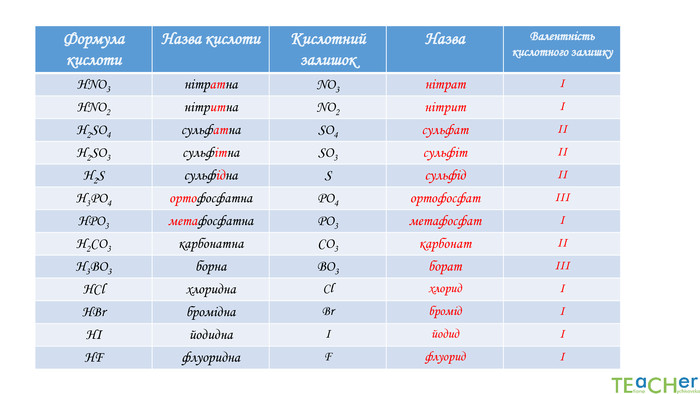
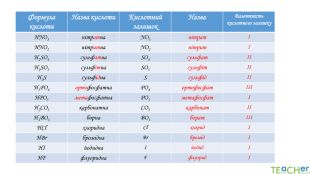
{5 C22544 A-7 EE6-4342-B048-85 BDC9 FD1 C3 A}Формула кислоти. Назва кислоти. Кислотний залишок. Назва. Валентність кислотного залишку. HNO3 нітратна. NO3нітратІHNO2нітритна. NO2нітритІН2 SO4 сульфатна. SO4 сульфатІІН2 SO3сульфітна. SO3сульфітІІН2 Sсульфідна. SсульфідІІН3 РО4 ортофосфатна. РО4 ортофосфатІІІНРО3 метафосфатна. РО3метафосфатІН2 СО3карбонатна. СО3карбонатІІН3 ВО3борна. ВО3боратІІІНСlхлоридна. ClхлоридІHBrбромідна. BrбромідІHIйодидна. IйодидІHFфлуоридна. FфлуоридІ
Солі - складні речовини, що складаються з атомів металічних елементів і кислотних залишків. Назви солей:1. Для елементів зі сталою валентністю:назва елемента + назва кислотного залишку2. Для елементів зі змінною валентністю: назва елемента + валентність + назва кислотного залишку Na3 PO4 - натрій ортофосфат, Al2(SO4)3 - алюміній сульфат, K2 CO3 - калій карбонат. Fe. Cl3 – ферум (ІІІ) хлорид, Fe. SO4 – ферум (ІІ) сульфат
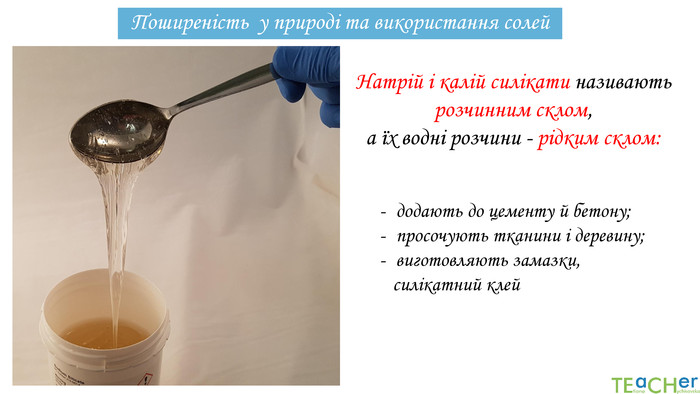
Поширеність у природі та використання солей. Магній хлорид Mg. Cl2 зустрічається у вигляді мінералу бішофіту. У результаті реакції зі снігом бішофіт викликає його танення. Бішофіт використовують для отримання магнію і оздоровлення опорно-рухової системи у санаторному лікуванніNa2 CO3 - кальцинована сода. Соду використовують в побуті для чищення і прання білизни. Сода споживається скляною, миловарною, целюлозно-паперовою, текстильною, нафтовою і іншими галузями промисловості
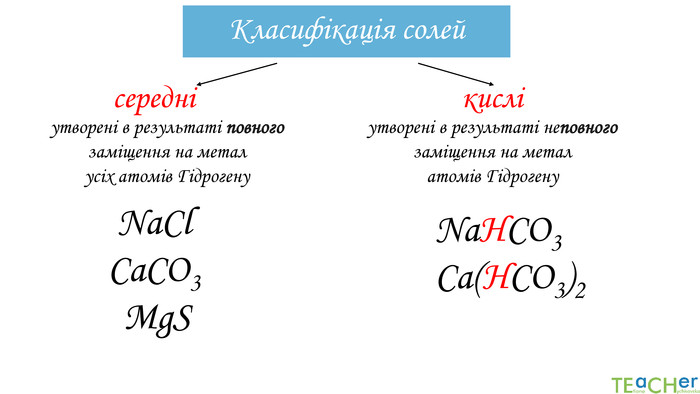
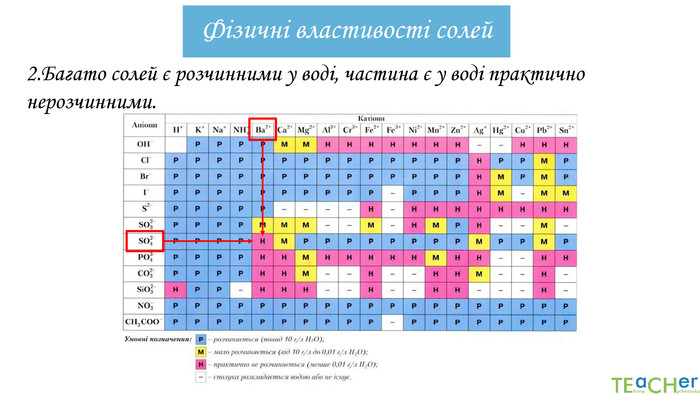
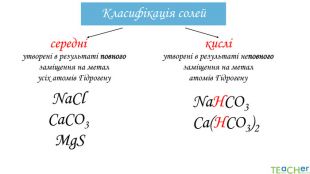
Підведемо підсумки!Солями називають складні речовини, що складаються з атомів металічних елементів і кислотних залишків. Солі поділяються на середні і кислі. Солі – це сполуки йонної будови, тому за звичайних умов – це тверді кристалічні речовини з високими температурами плавлення. Багато солей є розчинними у воді. Солі поширені у природі і мають використання у промисловості.


про публікацію авторської розробки
Додати розробку
























-

Рязанова Татьяна
03.02.2026 в 08:21
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Кузьменко Ольга Сергіївна
06.05.2025 в 16:48
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Фертак Наталя Володимирівна
14.04.2025 в 21:13
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Рибак Наталія Іванівна
09.04.2025 в 21:58
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Павленко Тетяна Петрівна
26.02.2025 в 20:52
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Сарахман Вікторія
19.02.2025 в 10:01
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Юсин Надія Улянівна
11.04.2024 в 21:09
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Мельник Тетяна Сергіївна
08.02.2024 в 08:48
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Безсонова Оксана
03.05.2023 в 17:36
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Пась Любов Григорівна
10.04.2023 в 21:12
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Клюй Татьяна
31.01.2023 в 18:31
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Змієвська Людмила Іванівна
05.04.2022 в 08:22
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Санін Євген
26.01.2022 в 21:15
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Крамар Лариса
13.07.2021 в 13:18
Дякую!
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Біліченко / Bilichenko Марина / Maryna
24.03.2021 в 15:09
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Біліченко / Bilichenko Марина / Maryna
24.03.2021 в 15:09
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Отрощенко Юлія Володимирівна
26.02.2021 в 14:46
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Михайленко Лариса Анатоліївна
21.02.2021 в 21:04
Дякую. Дуже гарна презентація. Змістовна та бездоганно зроблена.
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
Показати ще 15 відгуків