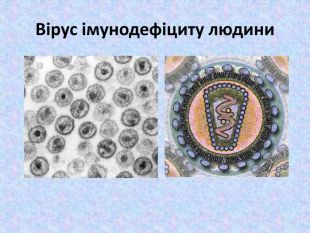
Презентація до уроку з біології на тему " Імунодефіцитні стани"
Про матеріал
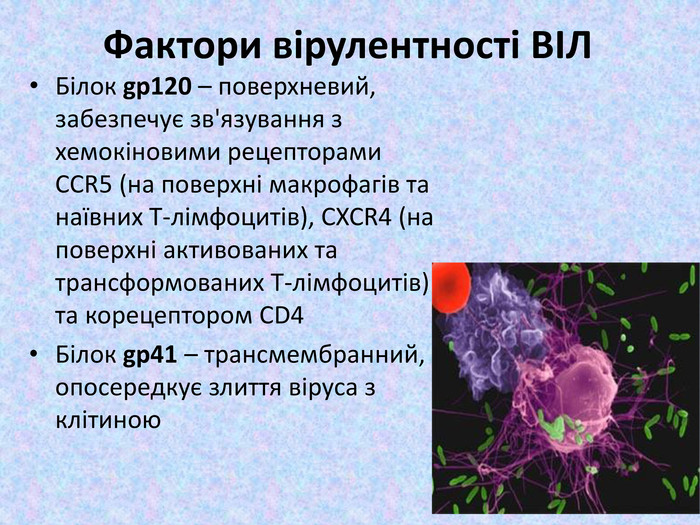
Імунодефіцити - порушення імунологічної реактивності, обумовлені випаданням одного або декількох компонентів імунного апарату або неспецифічних чинників, що тісно взаємодіють з ним.Вказано класифікація імунодифіцитних станів та їх приклади.
Перегляд файлу
Зміст слайдів
Середня оцінка розробки
Оцінки та відгуки
ppt
До підручника
Біологія 9 клас (Соболь В. І.)
Оцінка розробки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку