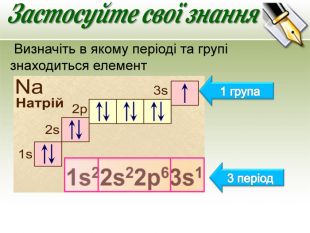
Презентація до уроку з хімії для 8 класу "Енергетичні рівні та підрівні. Їх заповнення електронами в атомах хімічних елементів (продовження).
Про матеріал
Конспект уроку з хімії для 8 класу "Енергетичні рівні та підрівні. Їх заповнення електронами в атомах хімічних елементів (продовження). Перегляд файлу
Зміст слайдів
pptx
Оцінка розробки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку



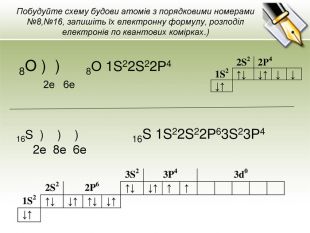
![Скорочені електронні формулиІноді записують електронні формули в скороченому вигляді. Для цього відокремлюють ту частину формули, яка відповідає будові атома найближчого інертного газу. В електронній формулі атома Сульфуру можна виділити електрони, які відповідають будові атома Неону: S 1s2 2s2 2р6 3s2 3р4 Тому електорнну формулу можна записати так: S [Ne] 3s2 3р4 Скорочені електронні формулиІноді записують електронні формули в скороченому вигляді. Для цього відокремлюють ту частину формули, яка відповідає будові атома найближчого інертного газу. В електронній формулі атома Сульфуру можна виділити електрони, які відповідають будові атома Неону: S 1s2 2s2 2р6 3s2 3р4 Тому електорнну формулу можна записати так: S [Ne] 3s2 3р4](/uploads/files/96066/194034/209656_images/3.jpg)
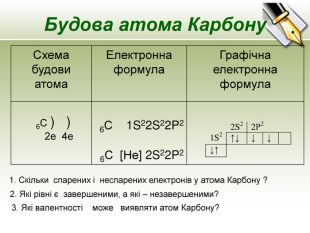
![Будова атома Карбону {5940675 A-B579-460 E-94 D1-54222 C63 F5 DA}Схема будови атома. Електронна формула. Графічна електронна формула6 С ) ) 2е 4е 6 С 1 S22 S22 P26 С [Не] 2 S22 P21. Скільки спарених і неспарених електронів у атома Карбону ?2. Які рівні є завершеними, а які – незавершеними?3. Які валентності може виявляти атом Карбону? Будова атома Карбону {5940675 A-B579-460 E-94 D1-54222 C63 F5 DA}Схема будови атома. Електронна формула. Графічна електронна формула6 С ) ) 2е 4е 6 С 1 S22 S22 P26 С [Не] 2 S22 P21. Скільки спарених і неспарених електронів у атома Карбону ?2. Які рівні є завершеними, а які – незавершеними?3. Які валентності може виявляти атом Карбону?](/uploads/files/96066/194034/209656_images/4.jpg)
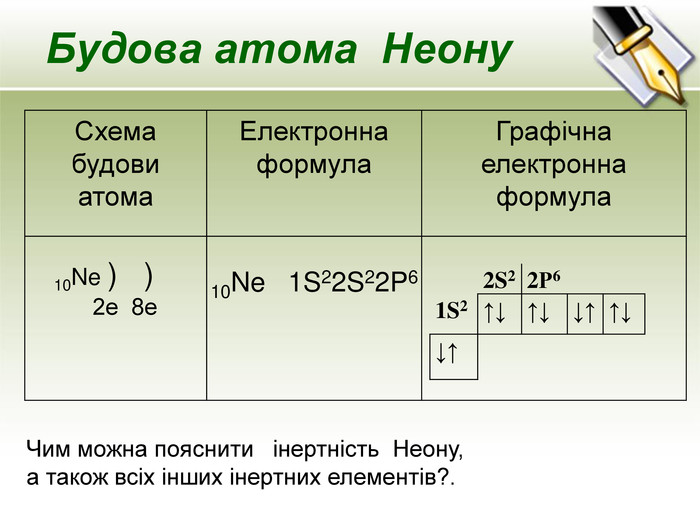
![Будова атома Фосфору{5940675 A-B579-460 E-94 D1-54222 C63 F5 DA}Схема будови атома. Електронна формула. Графічна електронна формула 15 Р 1 S22 S22 P63 S23 Р3 15 Р [Nе] 3 S23 Р31. Скільки спарених і неспарених електронів у атома Фосфору?2. Які рівні є завершеними, а які – незавершеними?3. Які валентності може виявляти атом Фосфору? 15 Р ) ) ) 2е 8е 5е 3 S23 P33d0 2 S22 P6↑↓↑↑↑ 1 S2↑↓↓↑↑↓↓↑ ↓↑ Будова атома Фосфору{5940675 A-B579-460 E-94 D1-54222 C63 F5 DA}Схема будови атома. Електронна формула. Графічна електронна формула 15 Р 1 S22 S22 P63 S23 Р3 15 Р [Nе] 3 S23 Р31. Скільки спарених і неспарених електронів у атома Фосфору?2. Які рівні є завершеними, а які – незавершеними?3. Які валентності може виявляти атом Фосфору? 15 Р ) ) ) 2е 8е 5е 3 S23 P33d0 2 S22 P6↑↓↑↑↑ 1 S2↑↓↓↑↑↓↓↑ ↓↑](/uploads/files/96066/194034/209656_images/6.jpg)