Презентація до уроку з теми "Реакції обміну між розчинами електролітів. Йонно-молекулярні рівняння хімічних реакцій"
Про матеріал
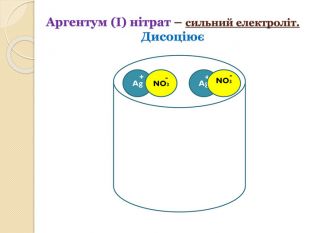
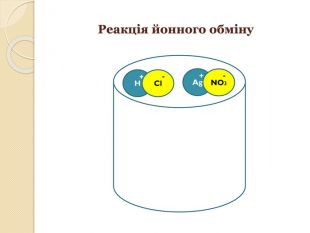
Дана презентація до уроку з теми "Реакції обміну між розчинами електролітів.
Йонно-молекулярні рівняння
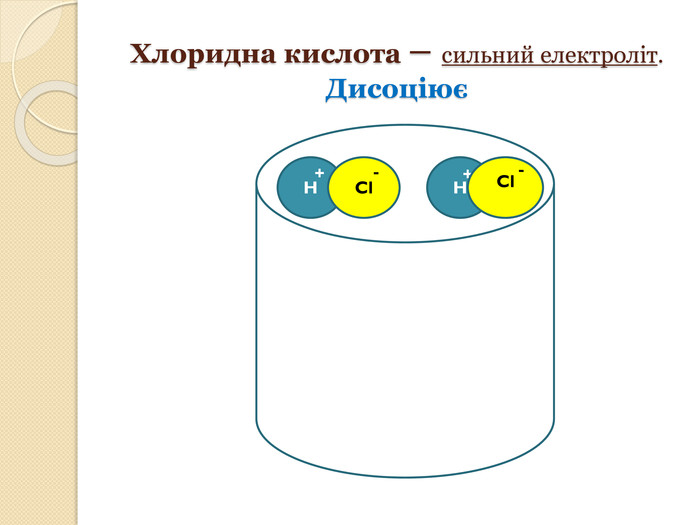
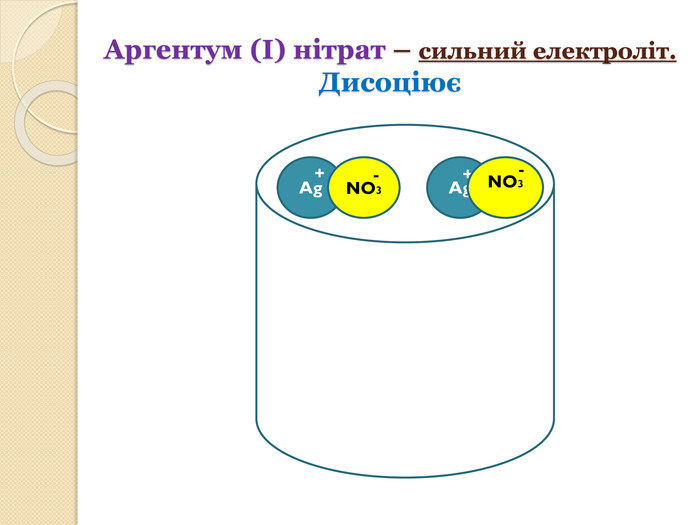
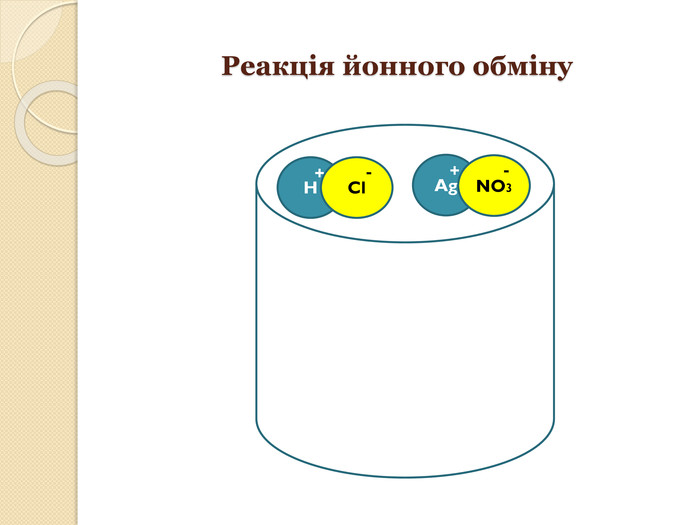
хімічних реакцій" розкриває дані хімічні поняття, дає змогу наочно представити хід протікання реакцій йонного обміну. Перегляд файлу
Зміст слайдів
pptx
Оцінка розробки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку