Презентація "Добування металів"
Про матеріал
Презентація створена для допомоги вчителю при вивченні теми :"Добування металів".
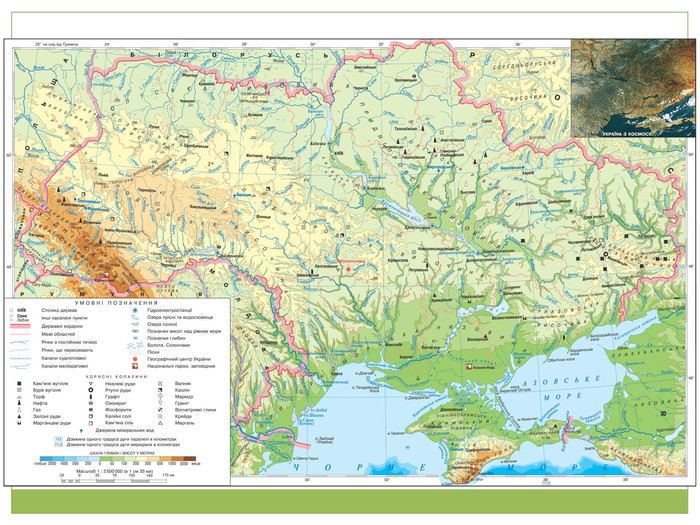
Велика кількість фото сприяє розумінню в учнів велич і грандіозність металургічних виробництв.
Перегляд файлу
Зміст слайдів
Середня оцінка розробки
Оцінки та відгуки
-
Все добре
-
Щиро дякую за презентацію. Допомогла в підготовці до уроку.
ppt
До підручника
Хімія (профільний рівень) 10 клас (Буринська Н.М. та інші)
Оцінка розробки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку