Презентація "Добування оксидів, основ, кислот та солей"
Про матеріал
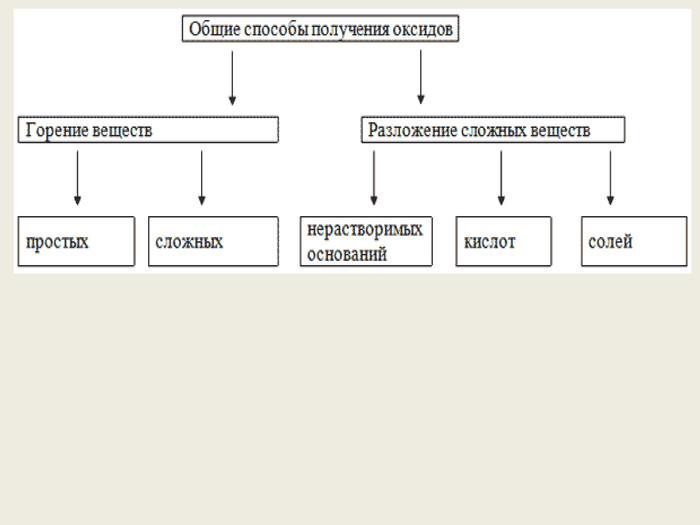
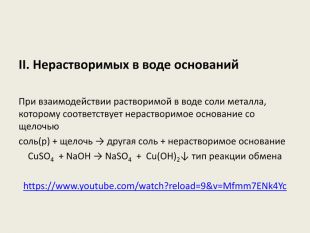
Презентація до уроку в 8-х класах на тему "Способи добування оксидів, основ, кислот та солей" Перегляд файлу
Зміст слайдів
pptx
Оцінка розробки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку