Презентація «Хімічні властивості лугів і нерозчинних гідроксидів» 8 клас
Про матеріал
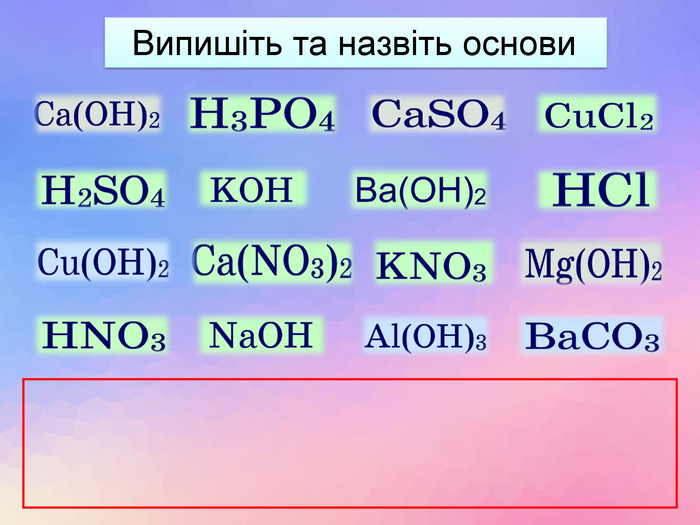
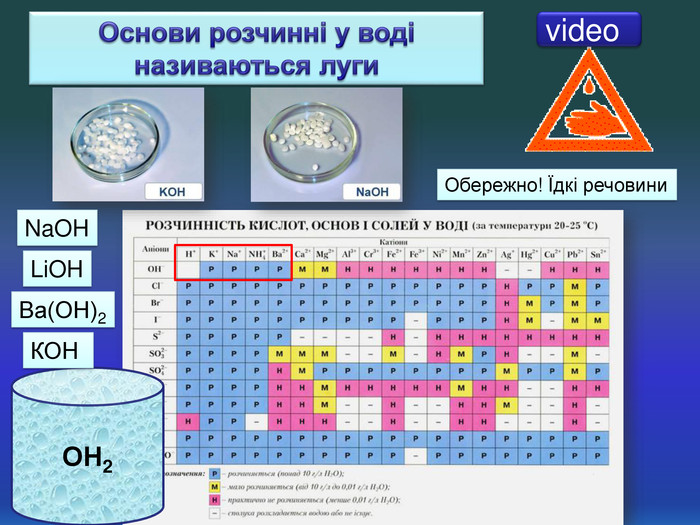
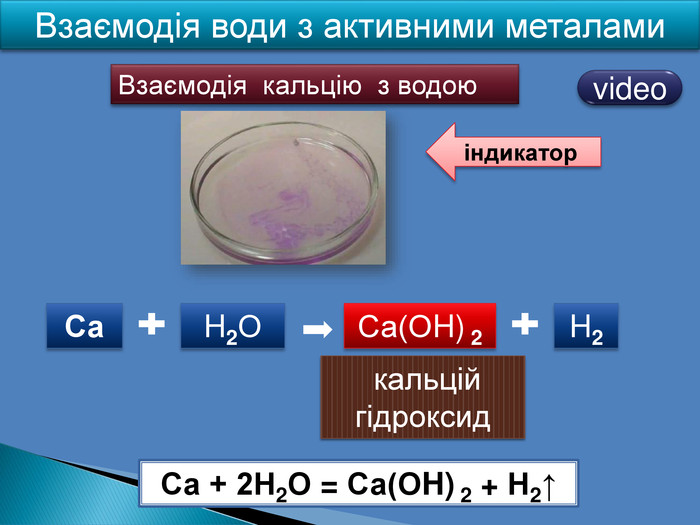
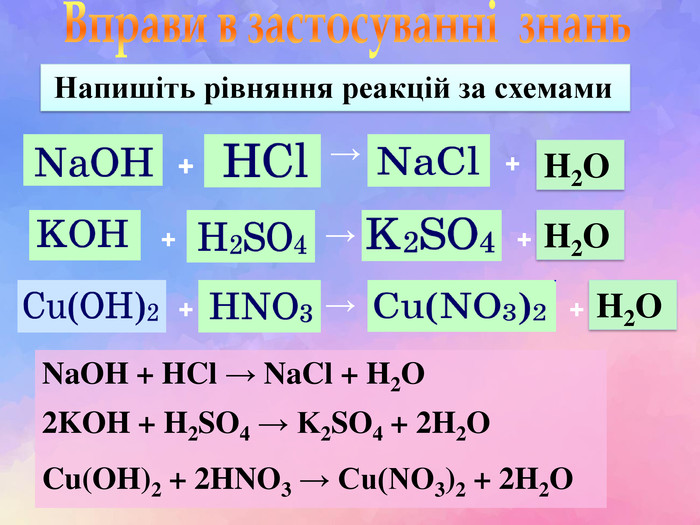
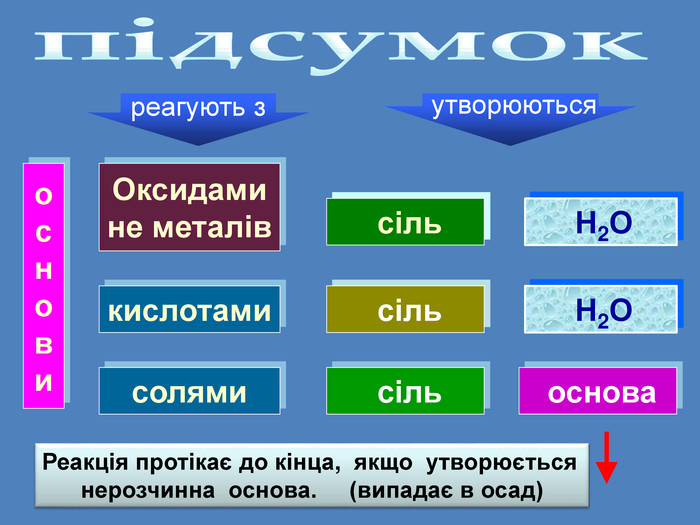
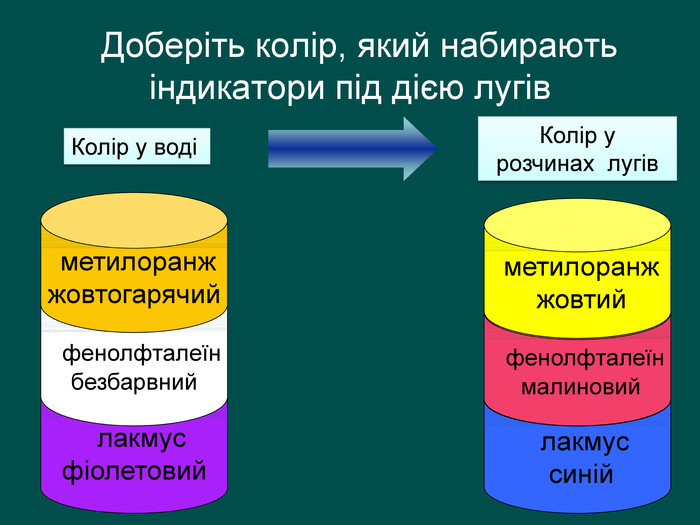
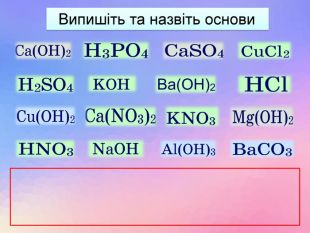
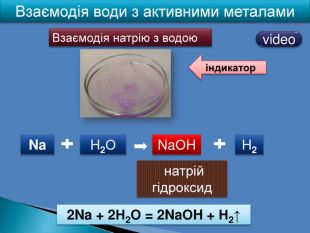
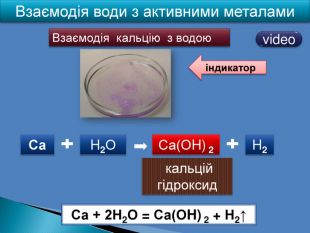
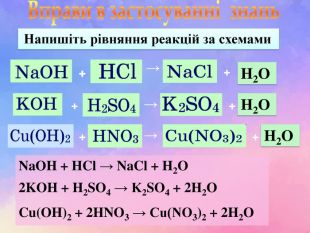
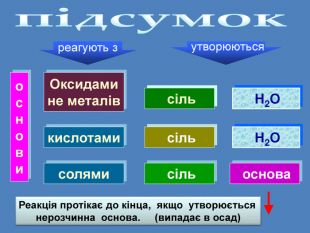
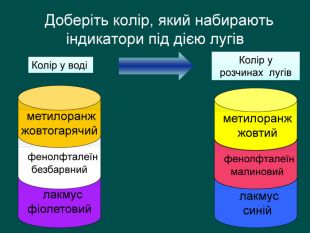
| Презентація допоможе в проведенні уроків на теми: «Хімічні властивості лугів: дія на індикатори, взаємодія з кислотами, кислотними оксидами, солями». «Нерозчинні основи: взаємодія з кислотами і розкладання внаслідок нагрівання». |
Перегляд файлу
Зміст слайдів
Середня оцінка розробки
Оцінки та відгуки
-
Дякую!
pptx
Оцінка розробки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку