Презентація «Класифікація неорганічних сполук, їхні склад і номенклатура» 8 клас

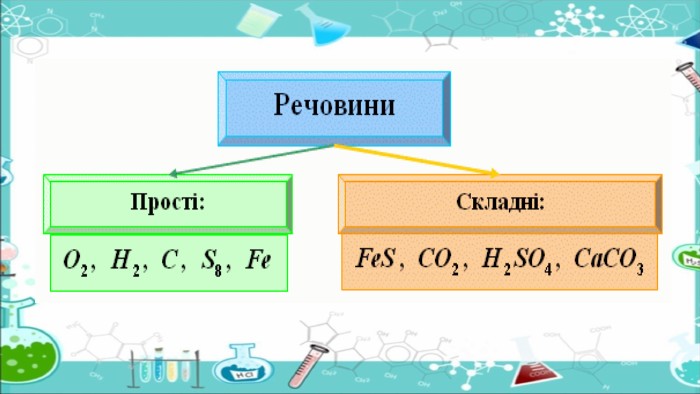

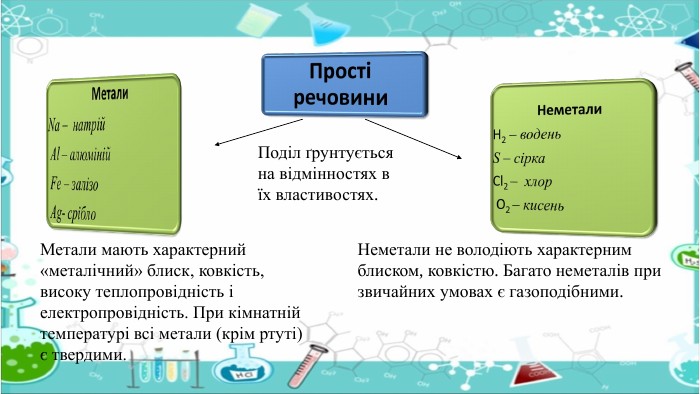


















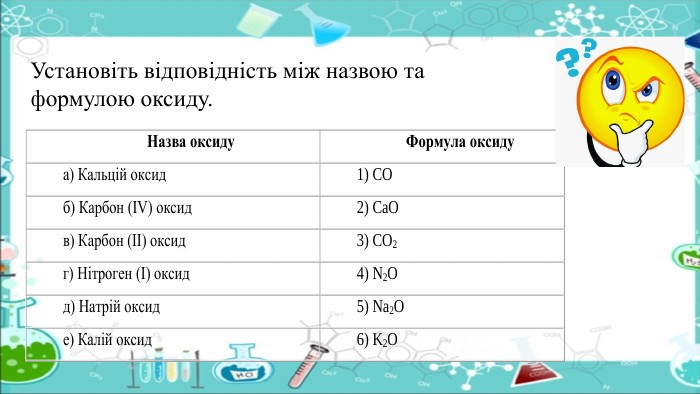

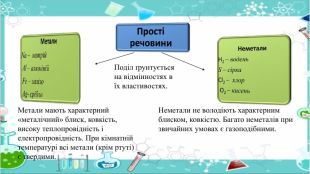
Неметали. H2 – водень. S – сірка. Cl2 – хлор O2 – кисень. Прості речовини. Поділ ґрунтується на відмінностях в їх властивостях. Метали мають характерний «металічний» блиск, ковкість, високу теплопровідність і електропровідність. При кімнатній температурі всі метали (крім ртуті) є твердими. Неметали не володіють характерним блиском, ковкістю. Багато неметалів при звичайних умовах є газоподібними.
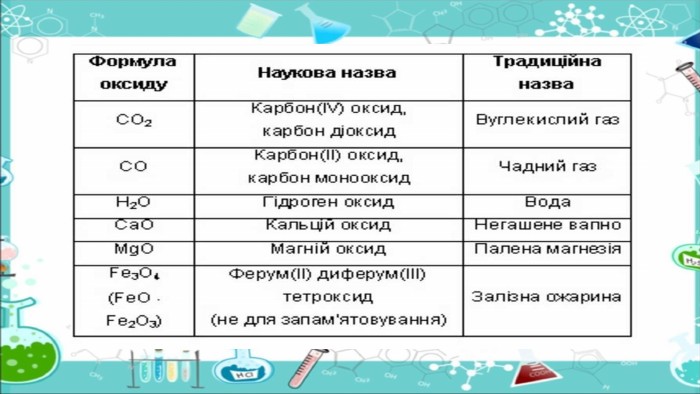
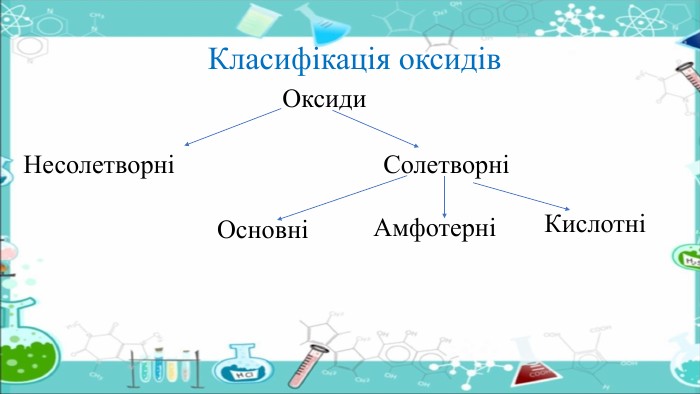
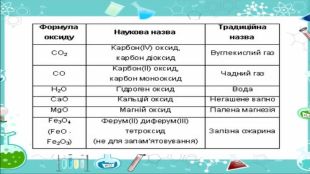
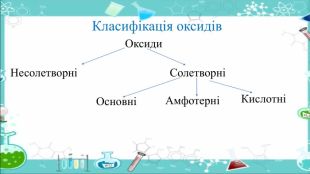
Солетворні оксиди – оксиди, яким відповідають основні або кислотні сполуки. Солетворні оксиди поділяють на такі групи:кислотні оксиди – оксиди, гідрати яких є кислотами. До цієї групи належать більшість оксидів неметалічних елементів та оксиди металічних елементів зі ступенем окиснення, більшим ніж +3, наприклад: SO3, CO2, NO2, Cr. O3, Mn2 O7. Кислотні оксиди називають ангідридами кислот, тобто «безводними кислотами»; основні оксиди – оксиди, гідрати яких є основами. До цієї групи належать оксиди металічних елементів зі ступенем окиснення, не більшим ніж +3, наприклад: Ca. O, Na2 O, Mg. O, Ba. O, Fe. O;амфотерні оксиди – оксиди, що виявляють властивості як кислотних, так і основних оксидів. До них належать: Be. O, Zn. O, Al2 O3, Fe2 O3, Cr2 O3. Несолетворні оксиди – оксиди, яким не відповідає ані кислота, ані основа. До них належать: NO, N2 O, CO, Si. O.
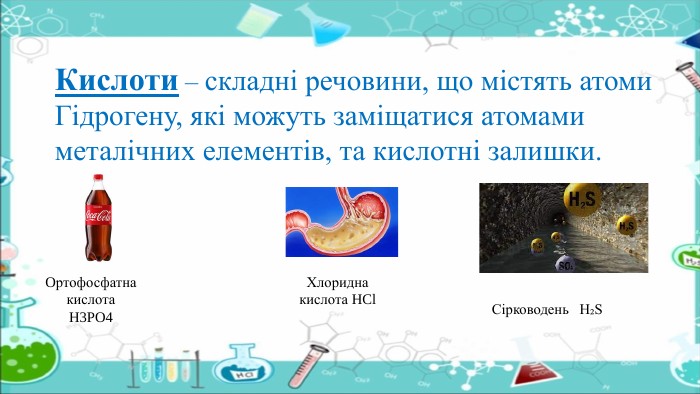
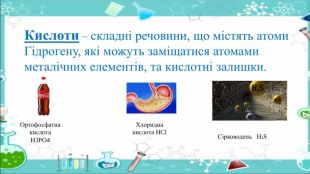
Загальна формула кислот – НКНазви кислот складають так: Нn + кислотний залишок, наприклад: H2 SO4, HNO3. Кислотним залишком називають частину молекули кислоти, сполучену з атомами Гідрогену. Н2 SO4 атоми Гідрогенукислотний залишок. Валентність кислотного залишку визначається кількістю атомів Гідрогену, здатних заміщуватися металами.
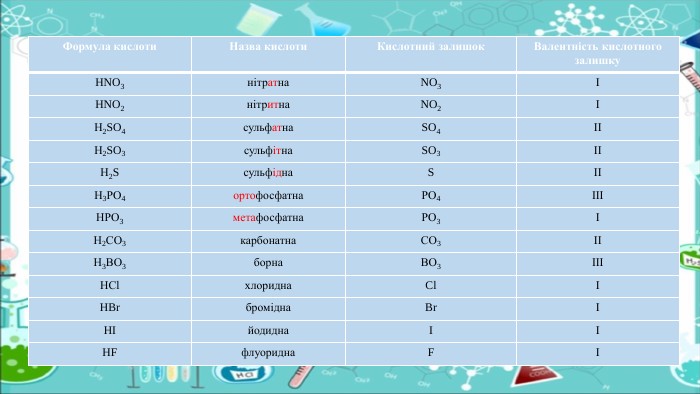
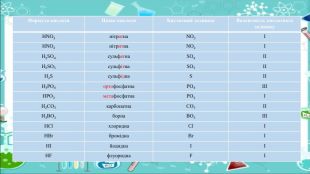
Формула кислоти. Назва кислоти. Кислотний залишок. Валентність кислотного залишку. HNO3 нітратна. NO3ІHNO2нітритна. NO2ІН2 SO4 сульфатна. SO4 ІІН2 SO3сульфітна. SO3ІІН2 Sсульфідна. SІІН3 РО4 ортофосфатна. РО4 ІІІНРО3 метафосфатна. РО3ІН2 СО3карбонатна. СО3ІІН3 ВО3борна. ВО3ІІІНСlхлоридна. ClІHBrбромідна. BrІHIйодидна. IІHFфлуоридна. FІ
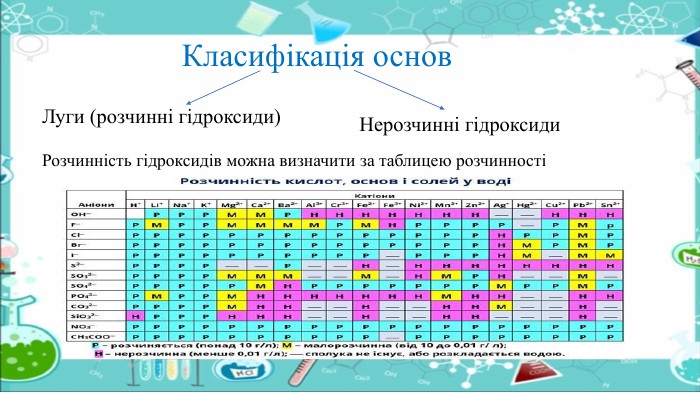
Загальна формула основ – Ме(ОН)х. Номенклатура Назви основ складають так: Для елементів зі сталою валентністю: Назва елемента + слово «гідроксид»Наприклад: Ca(OH) – кальцій гідроксид, Na. OH – натрій гідроксид. Для елементів зі змінною валентністю: Наприклад: Fe(OH) – ферум (ІІ) гідроксид, Cu(OH) – купрум (ІІ) гідроксид.
Те, який суфікс застосовують у назві солі, залежить від цілого ряду чинників, а саме:1) якщо до складу солі входить кислотний залишок безоксигенової кислоти (наприклад, хлоридної, (соляної) HCl), тоді використовується суфікс –ид (наприклад, хлорид);2) якщо до складу солі входить кислотний залишок кислоти, в назві якої є закінчення –а (наприклад, сульфатна H2 SO4), у назві солі використовується суфікс –ат (наприклад, сульфат);3) якщо до складу солі входить кислотний залишок кислоти, в назві якої є суфікс –ист (наприклад, сірчиста H2 SO3) , у назві солі використовується суфікс –іт (наприклад, сульфіт).
Якщо до складу солі входить металічний елемент, що має змінну валентність, то його валентність у даній сполуці вказують римськими цифрами в дужках одразу (без пробілу) після назви металу. Fe2(SO4)3 — ферум(III) сульфатІснують солі, до складу яких замість металічного хімічного елемента входить одновалентна група амонію NH4 I (йон амонію NH4+ ).
Класифікація солей. Середні солісолі до складу яких входить металічний хімічний елемент і кислотний залишок. Na. Cl - натрій хлорид;Al2(SO4)3- алюміній сульфат;NH4 NO3 - амоній нітрат. Кислі солісолі, до складу яких, крім металічного хімічного елемента і кислотного залишку, входять атоми Гідрогенунатрій гідрогенкарбонат Na. HCO3. Основні солісолі, до складу яких, крім металічного хімічного елемента і кислотного залишку, входять гідроксогрупи OHMg. OHCl — магній гідроксидхлорид;Fe(OH)(NO3)2 — ферум(III) гідроксиднітрат. Подвійні соліЯкщо атоми Гідрогену заміщуються атомами кількох різних металів, такі солі називаються подвійними. KNa. SO4 — калій натрій сульфат; KAl(SO4)2 — калій алюміній сульфат
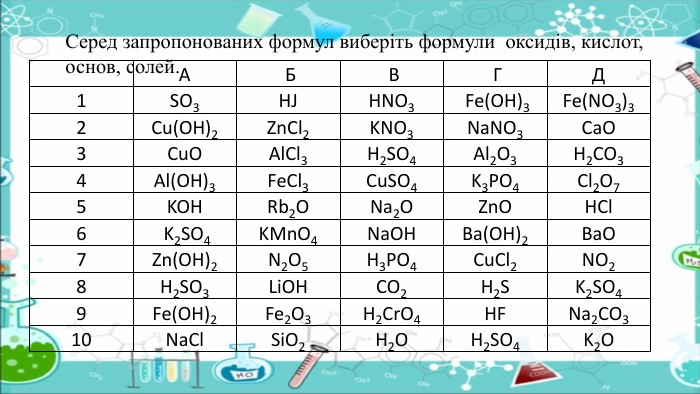
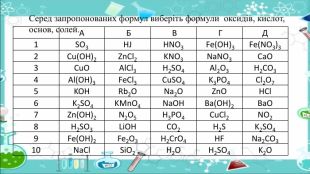
А Б В ГД1 SO3 HJHNO3 Fe(OH)3 Fe(NO3)32 Cu(OH)2 Zn. Cl2 KNO3 Na. NO3 Ca. O3 Cu. OAl. Cl3 H2 SO4 Al2 O3 H2 CO34 Al(OH)3 Fe. Cl3 Cu. SO4 K3 PO4 Cl2 O75 KOHRb2 ONa2 OZn. OHCl6 K2 SO4 KMn. O4 Na. OHBa(OH)2 Ba. O7 Zn(OH)2 N2 O5 H3 PO4 Cu. Cl2 NO28 H2 SO3 Li. OHCO2 H2 SK2 SO49 Fe(OH)2 Fe2 O3 H2 Cr. O4 HFNa2 CO310 Na. Cl. Si. O2 H2 OH2 SO4 K2 OСеред запропонованих формул виберіть формули оксидів, кислот, основ, солей.


про публікацію авторської розробки
Додати розробку
























-

Мульський Руслан
01.09.2025 в 20:32
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Токар Олексій
02.03.2025 в 17:45
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Ціпотан Людмила
26.02.2025 в 21:05
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Скубенич Оксана
12.02.2025 в 20:38
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Печончик Жанна
12.02.2025 в 11:27
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Потапова Галина Іванівна
13.01.2025 в 22:14
Дякую!
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Юзьвяк Любов Михайлівна
06.02.2024 в 19:04
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Бицина Оксана Валеріївна
05.02.2024 в 21:08
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Тихончук Олександр
04.02.2024 в 18:19
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Крамар Світлана
16.08.2023 в 11:26
Дякую!
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Палій Людмила Олександрівна
14.02.2023 в 19:36
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Карук Виктория Сергіївна
12.02.2023 в 14:56
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Радченко Тетяна Василівна
17.01.2023 в 11:27
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Воронівська Наталья Гуріївна
14.01.2023 в 23:33
Дякую !
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
Показати ще 11 відгуків