Презентація "Метан. Молекулярна, електронна і структурна формули метану, поширення у природі"
Про матеріал
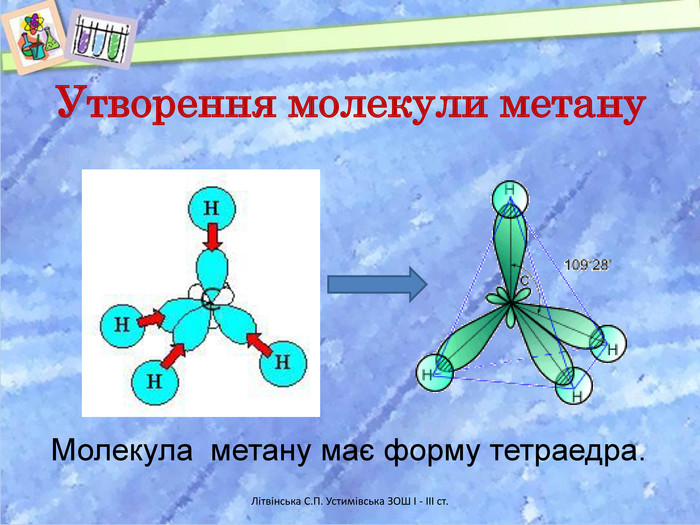
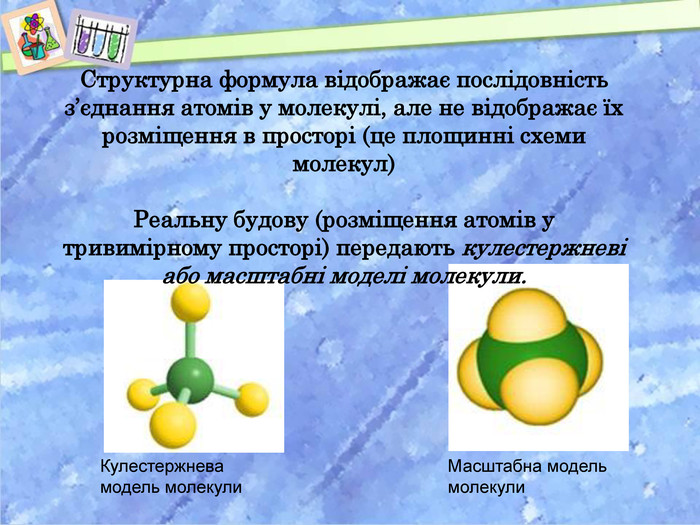
Презентація "Метан. Молекулярна, електронна і структурна формули метану, поширення у природі" допоможе візуалізувати викладення матеріалу. Допоможе познайомитися з будовою молекули метану, типом гібридизації електронних орбіталей атома Карбону, навчитися писати молекулярну, структурну, електронну формули молекули, описувати фізичні властивості метану та поглибити знання про поширення метану в природі.
Перегляд файлу
Зміст слайдів
Середня оцінка розробки
Оцінки та відгуки
-
-
Дякую за роботу!
-
Дякую за роботу!

Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку