Презентація "Практична робота №1. Реакції йонного обміну між електролітами у водних розчинах.
Про матеріал
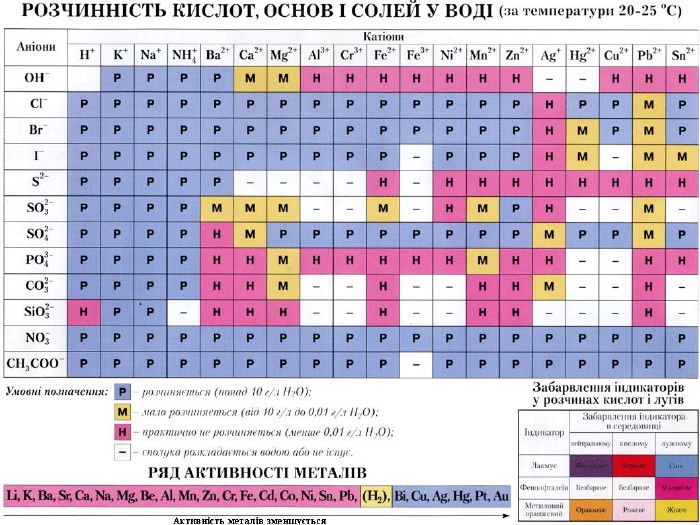
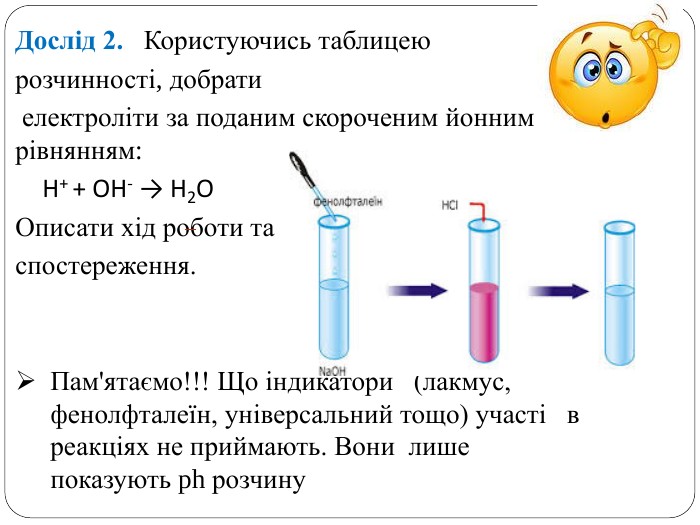
Презентація до практичної роботи №1 "Реакції йонного обміну між електролітами у водних розчинах". Хімія, 9 клас Перегляд файлу
Зміст слайдів
Середня оцінка розробки
Оцінки та відгуки
-
дякую!
-
-

Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку