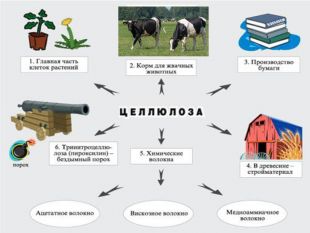
Презентація "Вуглеводи"





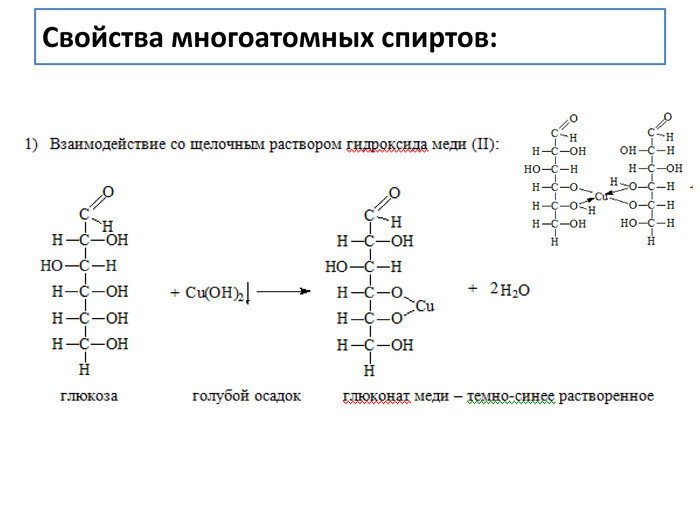
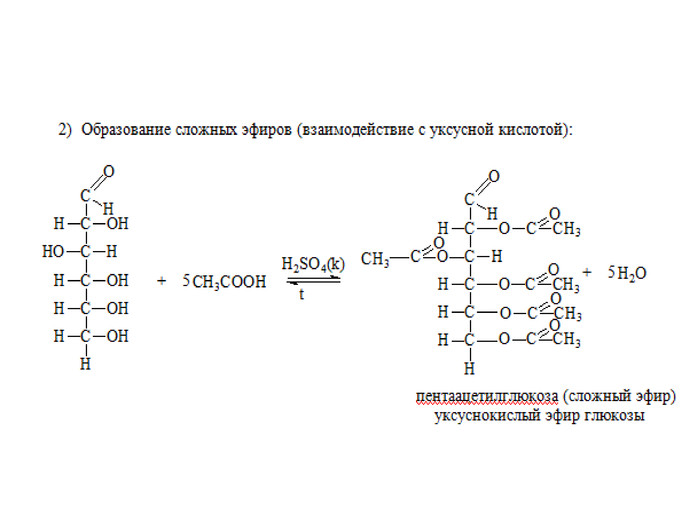

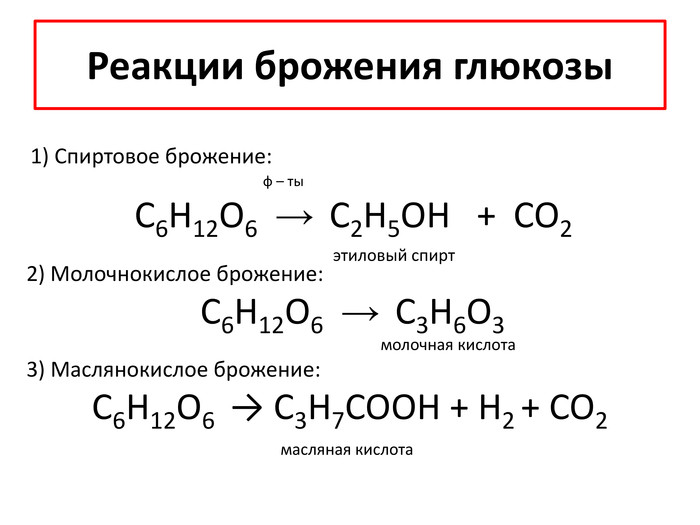
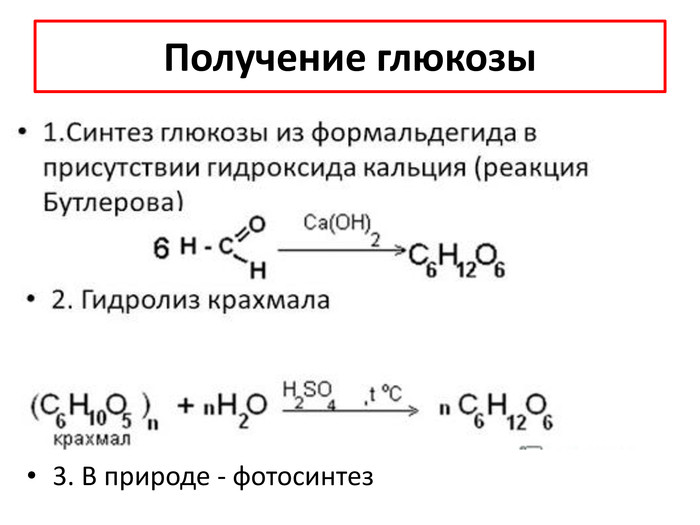














Фишер впервые определил строение некоторых органических веществ: кофеина, пурина, мочевой кислоты, глюкозы и фруктозы. Открыл методы их синтеза. Установил особенности реакций с участием ферментов, предложил классификацию белков. За исследования и синтез сахаридов и производных пурина получил Нобелевскую премию. Эмиль Герман Фишер (1852–1919)
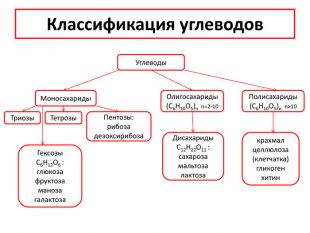
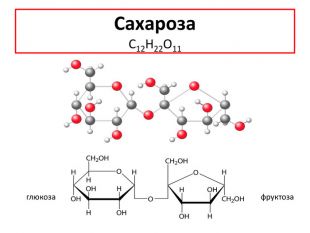
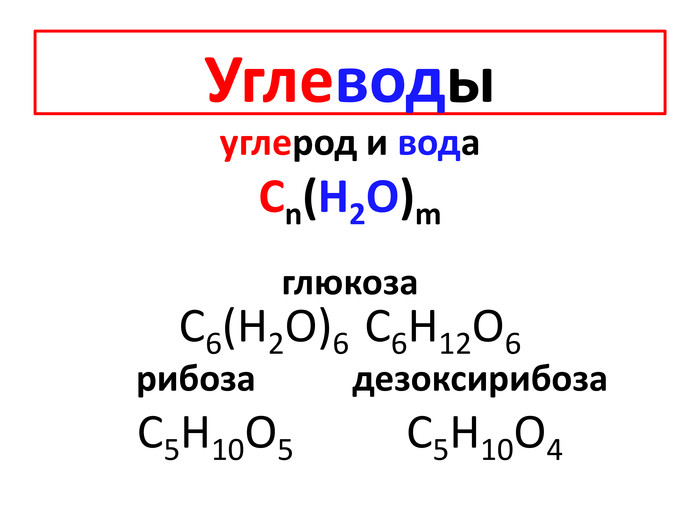
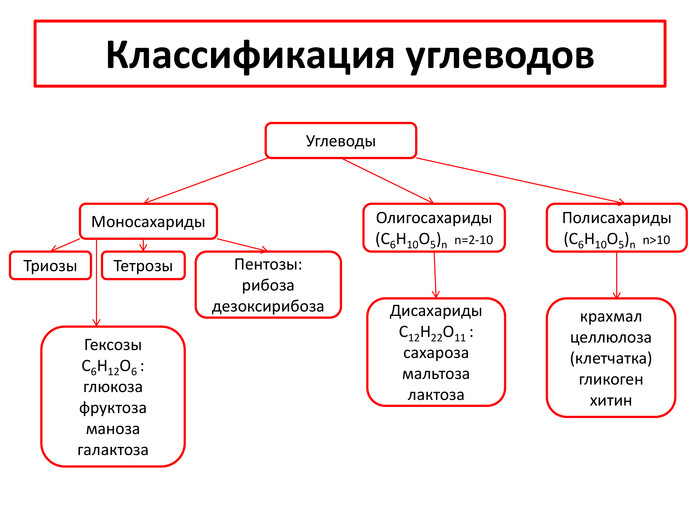
Классификация углеводов. Углеводы. Моносахариды. Дисахариды. C12 H22 O11 :сахарозамальтозалактоза. Полисахариды(C6 H10 O5)n n>10 Триозы. Тетрозы. Олигосахариды(C6 H10 O5)n n=2-10 Пентозы:рибозадезоксирибоза. Гексозы C6 H12 O6 :глюкозафруктозаманоза галактозакрахмалцеллюлоза (клетчатка)гликогенхитин
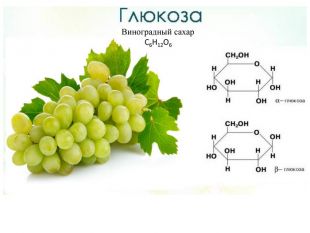
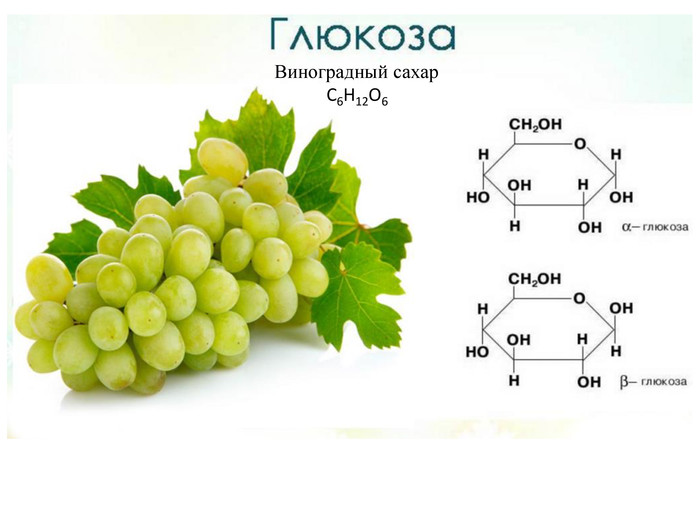
Физические свойства Глюкоза (виноградный сахар)— бесцветное кристаллическое вещество без запаха,плотность 1,54 г/см3, температура плавления 146 °С. При нагревании выше этой температуры вещество разлагается, не доходя доточки кипения. Глюкоза сладкая на вкус, но в полтора раза менеесладкая, чем сахароза. Хорошо растворяется в воде.
Николай Андреевич Бунге — российский и украинский химик немецкого происхождения. Работал в областях электрохимиии и химических технологий. Исследовал органические соединения и электролиз растворов, усовершенствовал методику газового анализа. Изучал процесс производства сахара из сахарной свеклы и условия его протекания. Сделал весомый вклад в развитие отечественной сахарной промышленности.3 декабря 1842, Варшава —31 декабря 1914, Киев
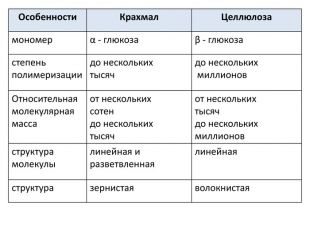
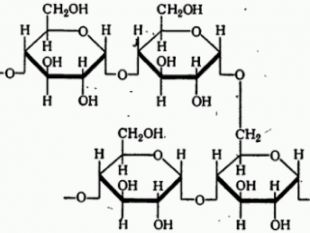
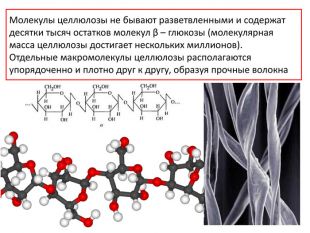
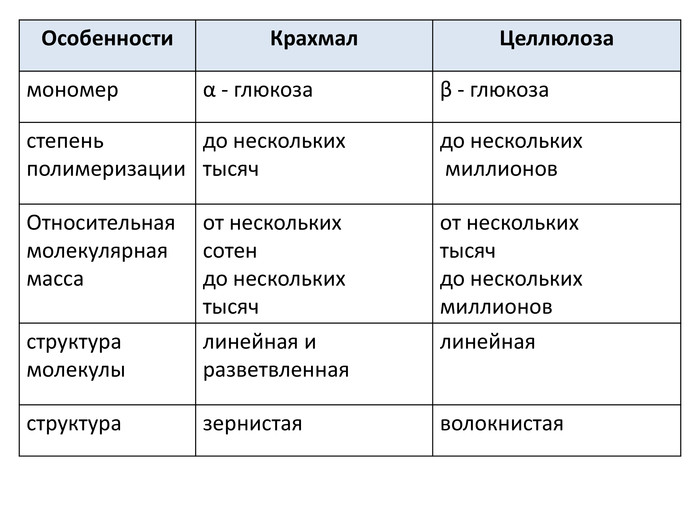
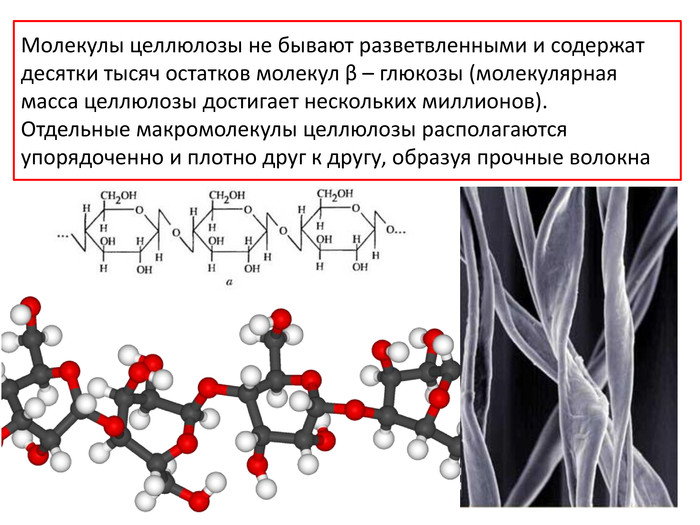
{0505 E3 EF-67 EA-436 B-97 B2-0124 C06 EBD24}Особенности. Крахмал. Целлюлозамономерα - глюкозаβ - глюкозастепеньполимеризациидо нескольких тысячдо нескольких миллионов. Относительная молекулярная массаот нескольких сотен до нескольких тысячот нескольких тысяч до нескольких миллионовструктурамолекулылинейная и разветвленнаялинейнаяструктуразернистаяволокнистая
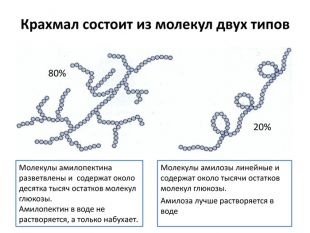
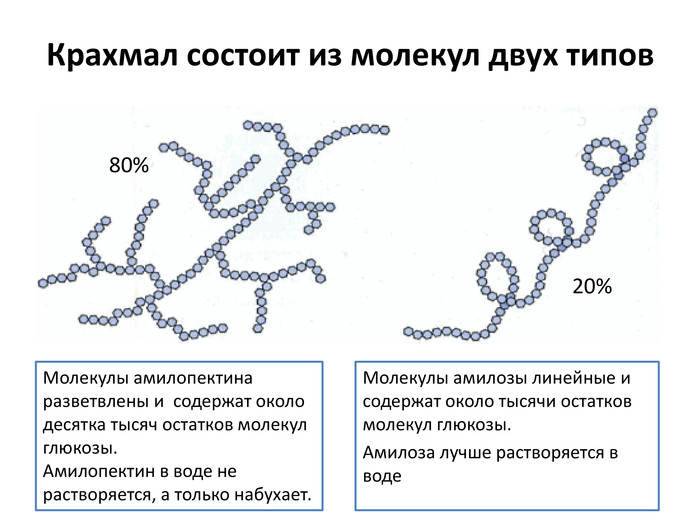
Крахмал состоит из молекул двух типов. Молекулы амилозы линейные и содержат около тысячи остатков молекул глюкозы. Амилоза лучше растворяется в воде. Молекулы амилопектина разветвлены и содержат около десятка тысяч остатков молекул глюкозы. Амилопектин в воде не растворяется, а только набухает.20%80%
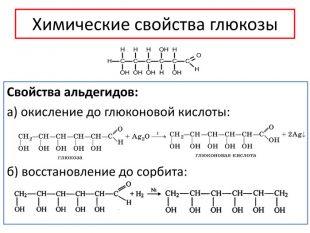
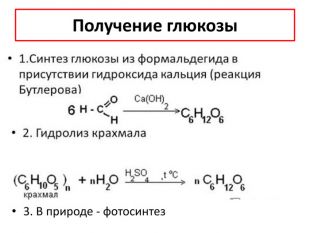
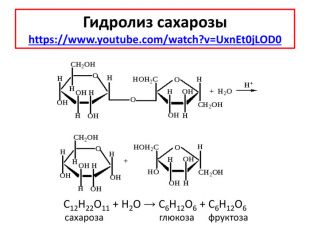
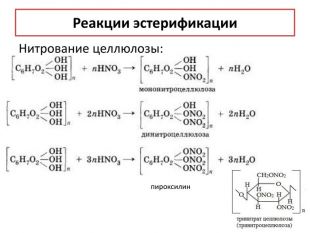
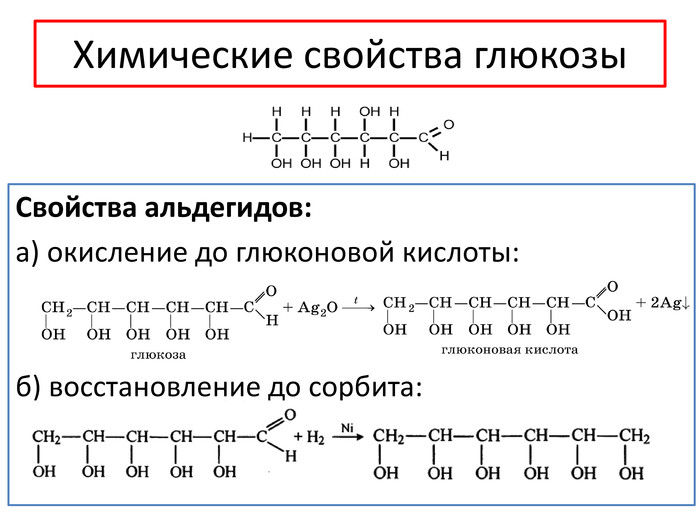
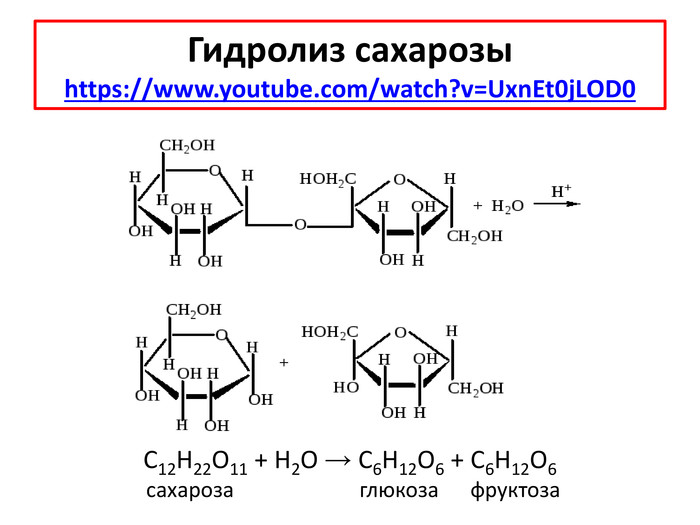
Химические свойстваhttps://www.youtube.com/watch?v=D5e. KSQm. Fux. UПри длительном нагревании в кислой среде или под действием ферментов крахмал подвергается гидролизу: (С6 H10 O5)n + n. H2 O → n. C6 H12 O6 α - глюкоза. Гидролиз крахмала может протекать ступенчато, с образованием различных промежуточных продуктов:
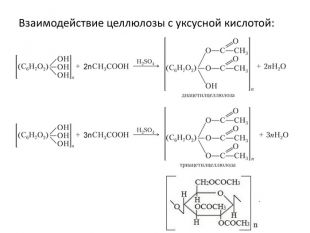
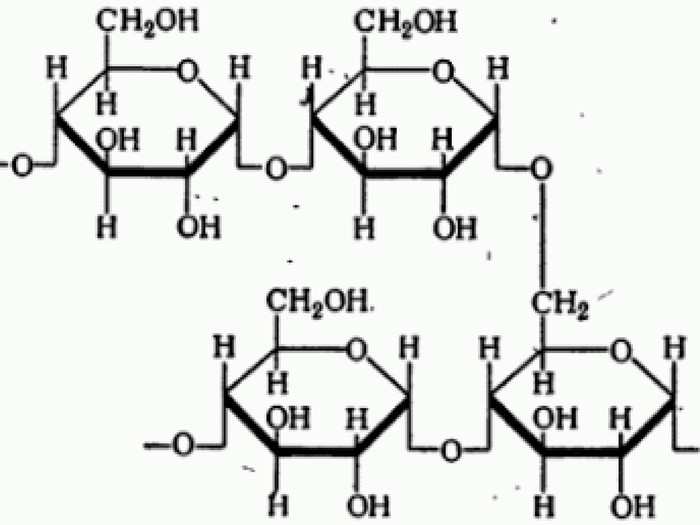
Целлюлоза взаимодействует с водой, подвергаясь гидролизу при значительно более жестких условиях по сравнению с крахмалом — при длительном кипячении с кислотой. Продуктом гидролиза также является глюкоза: (С6 H10 O5)n + n. H2 O → n. C6 H12 O6https://www.youtube.com/watch?v=t. Mz. Ov. B70a. Hw. Целлюлозу, а точнее древесину, ее содержащую, используют как топливо. Как и большинство органических веществ, целлюлоза сгорает до углекислого газа и воды: (С6 H10 O5)n + O2→ CO2 + H2 O
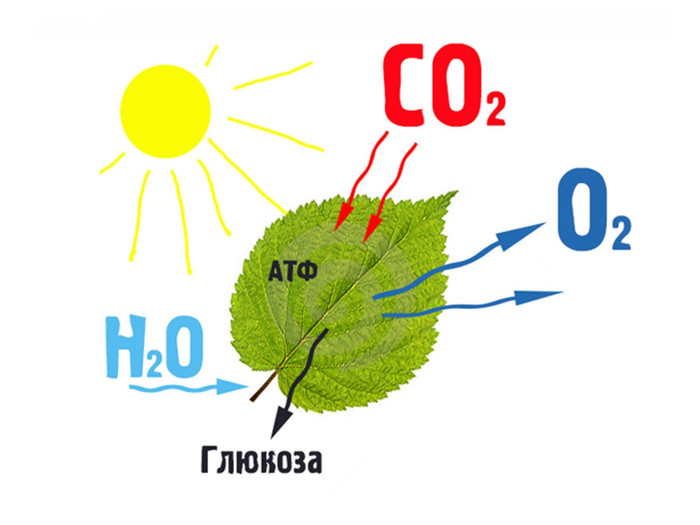
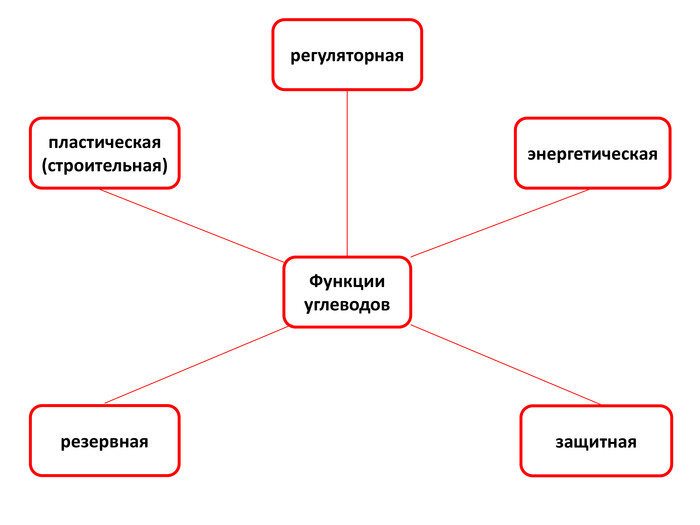
Биологическая роль углеводов. Для большинства организмов природные углеводы выполняют две основные функции:являются источником углерода, который необходим для синтеза белков, нуклеиновых кислот, липидов;обеспечивают до 70% потребности организма в энергии. При окислении 1 г углеводов выделяется приблизительно 16,9 к. Дж энергии. Другими функциями углеводов являются следующие: Резервная. Крахмал и гликоген представляют собой формы хранения питательных веществ, выполняя функцию временного депо глюкозы. Структурная. Целлюлоза и другие полисахариды растений образуют прочный остов; в комплексе с белками и липидами они входят в состав биомембран всех клеток. Защитная. Кислые гетерополисахариды выполняют роль биологического смазочного материала, выстилая трущиеся поверхности суставов, слизистой пищеварительных путей, носа, бронхов, трахей. Особое значение имеет специфическая функция углеводов – участие в образовании гибридных (комплексных) молекул, а именно гликопротеинов и гликолипидов. Так, гликопротеины служат маркерами в процессах узнавания молекулами и клетками друг друга, определяют антигенную специфичность, обусловливают различия групп крови, выполняют рецепторную, каталитическую и другие функции.
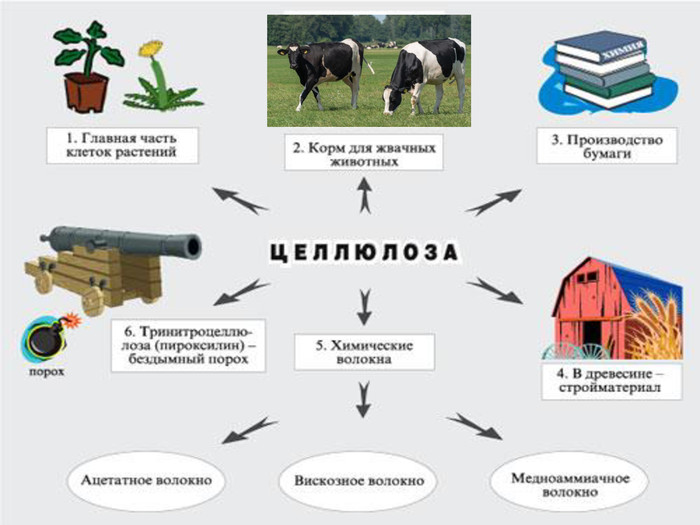
Домашнее задание. Проработать § 25, повторить § § 23, 24 Решить задачи №№ 184,186 на С.158 Интеллект-карточки: «Применение крахмала» «Применение целлюлозы»Учебные проекты: «Углеводы в пищевых продуктах: выявление и биологическая роль», «Натуральные волокна растительного происхождения: свойства, действие на организм человека, применение», «Искусственные волокна: применение в быту и промышленности»siledim@ukr.netsvetlanatisina40@gmail.comhttps://silence40.blogspot.com/p/7.html
-
 Оксана Проценко Григорівна 06.02.2022 в 22:41ДЯКУЮЗагальна:5.0Структурованість5.0Оригінальність викладу5.0Відповідність темі5.0
Оксана Проценко Григорівна 06.02.2022 в 22:41ДЯКУЮЗагальна:5.0Структурованість5.0Оригінальність викладу5.0Відповідність темі5.0 -
 Мелеганич Оксана 02.01.2021 в 20:30Загальна:4.7Структурованість5.0Оригінальність викладу4.0Відповідність темі5.0
Мелеганич Оксана 02.01.2021 в 20:30Загальна:4.7Структурованість5.0Оригінальність викладу4.0Відповідність темі5.0


про публікацію авторської розробки
Додати розробку