Презнтація «Реакції обміну між електролітами» 9 клас
Про матеріал
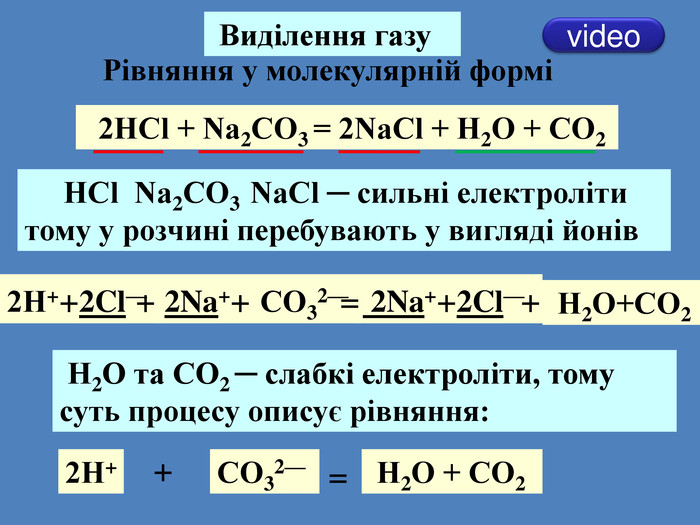
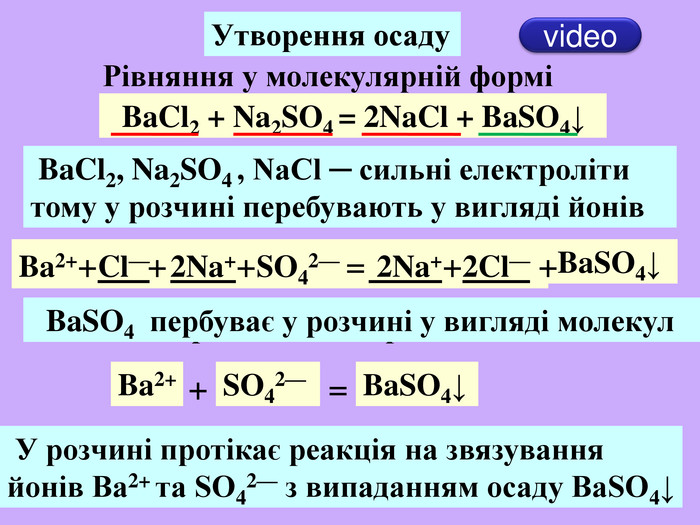
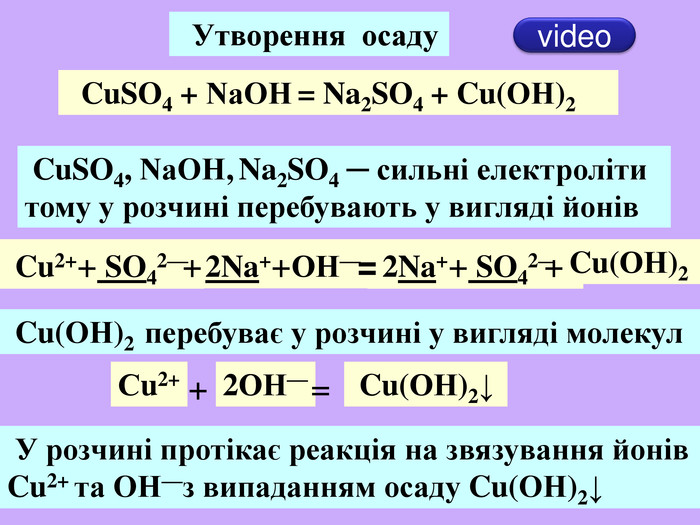
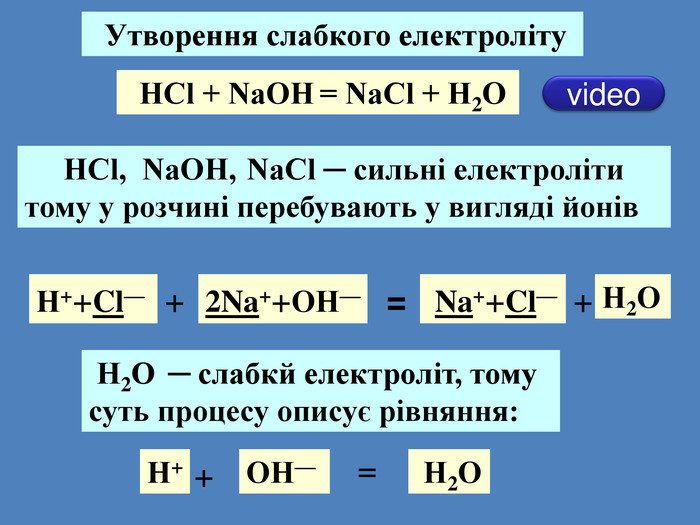
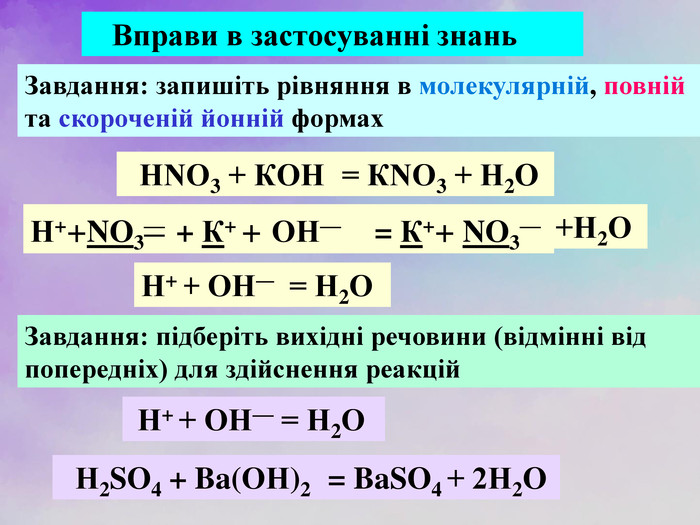
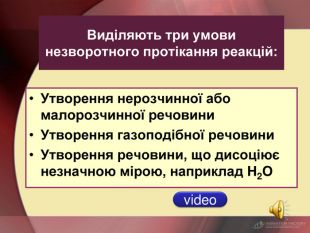
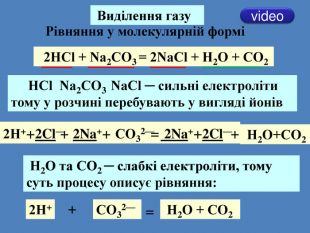
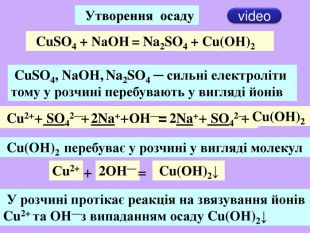
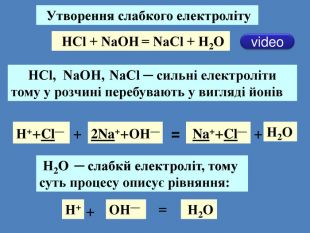
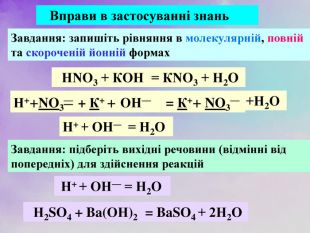
| Презентація допоможе учням та вчителю при проведенні уроку на тему «Реакції обміну між розчинами електролітів, умови їх перебігу. Йонно-молекулярні рівняння хімічних реакцій.» Та суттєво доповнить Демонстрації 3.Реакції обміну між електролітами у водних розчинах. |
Перегляд файлу
Зміст слайдів
pptx
До підручника
Хімія 9 клас (Григорович О.В.)
Оцінка розробки

Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку