Сценарій турніру хіміків-дослідників "Залізо.Сполуки Феруму"
Турнір направлений на залучення учнів загальноосвітніх шкіл та шкіл нового типу до участі в наукових дослідженнях, пошуковій роботі щодо вивчення будови, властивостей, біологічної ролі, практичного значення заліза та сполук Феруму; розвивитку творчі здібності учнів, логічного мислення, популяризацію хімії як науки, розвиток бережливого ставлення до природи та рідного краю; зміцнення міжпредметних зв'язків з біологією, географією, літературою, фізикою, математикою.
Криворізька спеціалізована загальноосвітня школа
І-ІІІ ступенів №4
з поглибленим вивченням іноземних мов
Сценарій турніру
хіміків-дослідників
за темою

Підготували:
Фейзопуло Людмила Володимирівна
Вчитель вищої категорії, вчитель старший вчитель
Кулик Вікторія Вадимівна
Вчитель ІІ категорії
Кривий Ріг
Мета та завдання турніру: виявляти інтелектуально обдарованих учнів; залучати учнів загальноосвітніх шкіл та шкіл нового типу до участі в наукових дослідженнях, пошуковій роботі щодо вивчення будови, властивостей, біологічної ролі, практичного значення заліза та сполук Феруму; розвивати творчі здібності учнів, логічно мислити, популяризувати хімію як науку, прищеплювати любов до природи та рідного краю; здійснювати міжпредметні зв’язки з біологією, географією, літературою, фізикою, математикою.
Проведення турніру - 9 лютого 2017 року
Програма турніру хіміків-дослідників
Доброго дня шановні учасники, журі та гості! Сьогодні ми проводимо турнір між командами нашого району і побачимо їх глибокі знання, кмітливість, артистичні здібності учасників та їх вміння сприймати з гумором як перемогу так і поразку, адже це тільки гра. Отже, розпочинаємо наш турнір.
Серед металів найголовніший,
Найважливіший, старовинний елемент,
У важкій індустрії славний,
Знайомий з ним школяр і студент
Народився в вогняній стихії,
Розплав його тече рікою.
Важливіше немає в металургії,
Він потрібен всій країні рідній.
(Залізо)
Він і являється темою нашого турніру, яка звучить так: «Залізо. Сполуки Феруму».
Давайте познайомимось з програмою турніру, яка складається з 5 конкурсів:
- Презентація команд “Давайте познайомимось...”
- Брейн – ринг. «Залізо. Сполуки Феруму»
2.1 Персоналії, хімічні реакції, великі помилки.
- “Увага, знаки!”
2.3. Конкурс “Підказка”
3. У хімічній лабораторії
4. Конкурс капітанів.
5. Конкурс «Знайди невідому речовину під час розв’язання задачі»
6. Підведення підсумків турніру.
Щоб серед наших учасників обрати кращу команду, нам допоможе наше вельмишановне журі:
Журі турніру: __________________________________________________
__________________________________________________________________________
Для початку давайте проведемо жеребкування, та дізнаємось з ким першим будемо знайомитись.
Жеребкування:
(вам потрібно швидко та правильно виконати моє завдання, хто буде перший і правильно виконає той виступає першим, другий і головне щоб завдання було виконано вірно і т.д.)
Завдання. Установіть послідовність утворення продуктів під час відновлення заліза в доменній печі з червоного залізняку:
А) FeO Б) Fe2O3 В) Fe3O4 Г) Fe
Відповідь: б – в – а – г
(якщо сировиною для виробництва чавуну є червоний залізняк, то процес відновлення заліза в доменній печі відбувається в такій послідовності:
- 3Fe2O3 + CO →t 2Fe3O4 + CO2
- Fe3O4 + CO →t 3FeO + CO2
- FeO + CO →t Fe + CO2
- Презентація команд “Давайте познайомимось...”
(ви повинні презентувати свою команду, хто був найкращий той отримує максимальну кількість балів 5, потім 4, 3, 2, 1)
- Брейн – ринг. «Залізо. Сполуки Феруму»
2.1 Персоналії, хімічні реакції, великі помилки.
(вам потрібно дати відповідь швидко та правильно на мої питань. Після кожного питання ви повинні записати відповідь на маленьких листочках і віддати журі. Хто відповів першим і вірно той отримує 3 бали, і т. д.)
- Укажіть продукт взаємодії заліза з хлором:
А) FeCl2 Б) FeCl3 В) FeOHCl2 Г) Fe(OH)2Cl
2. Укажіть речовину, яку використовують як відновник у доменній печі:
А) CH4 Б) CO В) H2 Г) NH3
3. Скільки всього алотропних модифікацій заліза:
А) 4 Б) 3 В) 5 Г) 1
4. Яка кислота не реагує з залізом:
А) H2SO4 к Б) HNO3 к В) H2SO4 р Г) HNO3 р
5. Який заряд йону має Ферум в берлінській лазурі:
А) Fe2+ Б) Fe3+ В) Fe0 Fe+4
6. Як називається промисловий спосіб отримання металу, який відновлює метали із розплавлених хлоридів, оксидів або гідроксидів за допомогою електролізу:
А) Пірометалургійний Б) Алюмінотерапія
В) Електрометалургійний Г) Гідрометалургійний
7. Формула ферум(ІІІ) оксиду:
А) Fe3O4 Б) Fe2O3 В) FeO
8. Масова частка Феруму в сполуці Fe2O3:
А) 77,8 % Б) 70 % в) 72,4 %
9. У складі якого мінералу міститься Ферум:
А) карналіт Б) пірит В) малахіт Г) мірабіліт
10. Укажіть назву речовини Х у схемі реакцій:
Fe + Cu(NO3)2 → X + Cu
А) ферум(ІІ) нітрат Б) ферум(ІІ) нітрит В) ферум(ІІІ) нітрат Г) ферум(ІІІ) нітрит
2.2 “Увага, знаки!”
1. Установіть відповідність речовин та умов буквам у схемі перетворень:
+А +Б +В +Г
Fe → FeCl2 → Fe(OH)2 → FeO → Fe
1. Cl2 2. HCl 3. NaOH 4. tº 5. CO
(відповідь: А - 2, Б – 3, В – 4, Г – 5)
- Установіть відповідність між формулою та назвою природних речовин Ферума:
1. Лимоніт А. Fe3O4
2. Гематит Б. Fe2O3
3. Магнетит В. FeS2
4. Сидерит Г. Fe2O3 *nH2O
5. Пірит Д. FeСО3
(відповідь: А – 3, Б – 2, В – 5, Г – 1, Д – 4)
- Установіть відповідність між способами добування сталі та посудиною в якій здійснюється цей процес:
1. Киснево-конвертерний спосіб А. 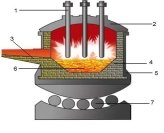 (добування сталі в електропечі)
(добування сталі в електропечі)
2. Мартенівський спосіб Б. 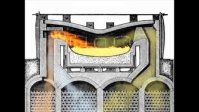 (мартенівська піч)
(мартенівська піч)
3. Виробництво сталі в електропечах В. 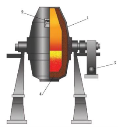 (конвертер)
(конвертер)
(відповідь: А – 3, Б – 2, В – 1)
2.3. Конкурс “Підказка”
(я загадала речовину, для того щоб вам її відгадати буду давати вам деякі підказки. Якщо ви відгадаєте з першої підказки, отримаєте 3 бали, з другої – 2 бали, з третьої – 1 бал.)
Підказка на 3 бали: Цей експонат у перекладі з грецької має назву «камінь, що висікає вогонь».
Підказка на 2 бали: Мінерал відомий та використовується людиною з давніх-давен. Лише в середині першого тисячоліття до н. е. кельти (числені давні племена індоєвропейської мовної групи, які проживали на території від Чехії до Ірландії, вперше навчилися виплавляти залізні руди й одержувати сталь) замінили його осталеним залізом, і в такому вигляді кресало проіснувало до винаходу сірників 1827 року.
Підказка на 1 бал. Його синоніми – сірчаний колчедан, купоросний колчедан, руда залізна печінкова, камінь інкський. Напишіть формулу цього мінералу.
(відповідь: ПІРИТ FeS2)
- У хімічній лабораторії
Команди повинні виконати відповідно до інструкції лабораторні досліди, дотримуючись техніки безпеки; написати рівняння хімічних реакцій відповідно до схеми перетворень у молекулярному та іонному вигляді
(Ви повинні виконати два завдання, але дотримуватись правил техніки безпеки при роботі з реактивами.
Інструкція
Завдання 1. Доведіть на практиці, що залізо може витіснити мідь, для цього у вас є всі необхідні реактиви.
(Залізо, як більш активний метал, витісняє мідь зі сполук купруму, яким є мідний купорос. Якщо залізний цвях або скріпку покласти у розчин мідного купоросу, вона досить швидко вкриється міддю.)
Завдання 2. У вас є дві пронумеровані пробірки, в одній із них FeCl2, в іншій FeCl3. Вам потрібно за допомогою реактивів, які знаходяться на парті дізнатись де Ферум має валентність 2, а де 3. Написати рівняння хімічних реакцій у молекулярному, іонному та скороченому вигляді.
- Одержання ферум(ІІ)гідроксиду:
FeCl2 + 2NaOH → Fe(OH)2↓ + 2NaCl
Fe2+ + 2Cl- + 2Na+ + 2OH- → Fe(OH)2↓ + 2Na+ + 2Cl-
Fe2+ + 2OH- → Fe(OH)2↓
Утворюється осад зеленуватого кольору
- Одержання ферум(ІІІ)гідроксиду:
FeCl3 + 3NaOH → Fe(OH)3↓ + 3NaCl
Fe3+ + 3Cl- + 3Na+ + 3OH- → Fe(OH)3↓ + 3Na+ + 3Cl-
Fe3+ + 3OH- → Fe(OH)3↓
Утворюється осад бурого кольору
- Конкурс капітанів.
Капітан команди повинен бути готовий виголосити промову з теми «Залізо. Сполуки Феруму»
(Капітан повинен сказати свою промову з теми: «Залізо. Сполуки Феруму», за найкращу промову максимальну кількість балів ви можете отримати 5)
- Конкурс «Знайди невідому речовину під час розв’язання задачі»
(учасники, вам потрібно взяти цілий лист паперу, та на ньому здійснити ланцюжок перетворень, і також дізнатись яку речовину я пропустила. Ви повинні написати рівняння реакцій. За завдання ви отримуєте максимальну кількість балів – 5, завдання не на швидкість, а на правильність)
Fe → FeCl2 → Fe(OH)2 → X → Fe2(SO4)3
(відповідь: 1. Fe + 2HCl → FeCl2 + H2
2. FeCl2 + 2NaOH → Fe(OH)2↓ + 2NaCl
3. 4Fe(OH)2 + 2H2O + O2 → 2Fe(OH)3
4. 2Fe(OH)3 + 3H2SO4 → Fe2(SO4)3 + 6H2O)
- Підведення підсумків турніру.
Поки наше журі підраховує кількість балів, ви можете переглянути цікаве відео.
Слово надається _____________________________.
Вітаємо переможців, та дякуємо за участь в турнірі та до нових зустрічей.
Виступ команди «Булат»
Презентація «Давайте познайомимось»
Добрий день! Здравствуйте! Бон жур! Хелоу!
Ми учні школи, яка всім відома.
В районі, у місті, і навіть в країні -
Загальноосвітня спеціалізована номер 4.
Досягнення школи досить вагомі -
Вона одна з кращих в Металургійному районі.
Ми, всі разом, команда «Булат»:
Буня, Ліза і Лозінський Влад,
Анастасія, Артем, Маргарита.
Чудові ми друзі й душа в нас відкрита.
На цей турнір ми прийшли позмагатись,
Помірятись силою і навчатись.
Здобутті знання збережемо дбайливо.
Розумом і працею піднімемо країну.
Тема турніру цікава нам стала,
Бо навкруги нас море метала:
Золото, срібло, мідь і тітан,
Цинк, алюміній, меркурій, тантал,
Барій, ванадій, кальцій і хром,
Торій, уран, нептуній, плутон…
Можна багато іще називати,
Але сьогодні ми хочем віддати
Гарні слова, і хвалу, і шану
Найважливішому трударю – металу.
Це – Залізо – батько роду
Що панує на Землі
Бо із нього, друже, роблять
Цвях, опори, кораблі,
Крани, дріт, машини різні
Та багато механізмів
І в людському тілі є,
Нам здоров’я придає.
Ми про Ферум багато вивчали:
Властивості, склад і будову,
Бо знали: теорія й практика поряд крокують
Й великі можливості людям дарують.
Люди давно Залізо вже знали,
«небесним металом» його величали.
З метеоритів його добували
І більше, ніж золото цінували.
З туманів космічних залізо злітало,
Землю пилом своїм огортало.
Оксиди і солі тут утворили
І в надрах родовища заполонили.
Мільйони років промайнуло і нині
Землю кварцити пасами покрили.
На всіх континентах родовища є,
Але найближче нам наше, своє!
Півтора століття тому
Олександр Поль тут жив
І на схилах Дубової
Рудні поклади відкрив.
Найбагатший наш – Кривбас,
Скіфів пам’ятає.
І руда у нас така,
Кращої немає.
А червоний залізняк
Залягає скрізь, та так,
Що можна зверху накопати,
Або із шахти діставати.
А у вчених думка є
Що відомо нині
Понад 300 мінералів
Залізо носіїв.
Гематит, магнетит, гетит і лепідокрокіт,
Лімоніт і сидерит, ільменіт та шалюзит.
Не забудемо сказати про сульфіди і фосфати,
Силікати, карбонати, гідроксиди, молібдати.
Щоб залізо чисте мати,
З рудою треба працювати:
Збагатити, відновити,
Дуже у печі нагріти,
Відділити зайвий шлак -
Вийде класно!!!
Чи не так?
Розжарене величчя стало
В конвертерах золотаво - білим.
І, утворивши зливки сталі,
Прямує на обробку далі.
На блюмінгу підвищить якість,
І мчить в прокатне виробництво,
Яке кує, штампує, ріже.
Весь сортамент, як те намисто.
А головне, я не змовчу,
Є вміст заліза й вуглецю
Чавун і сталь – наша надія -
Основа чорної металургії.
Як би люди зараз жили
Якби залізом не володіли?
Це - подарунок Божий на Землі,
За нього щиро дякуємо ми.
Іще ІІІ тисячі років тому назад
В Індії вперше зробили булат.
Твердий, пружний, своєрідний
До чеснот людських подібний.
Ми всі разом – кулак,
Але різні собою.
Команда «Булат»
Готова до бою!
Виступ капітана
Шановні, пані та панове!
Дозвольте вимовить промову
Про залізо як предмет науки,
Про Ферум і його сполуки.
Ферум – гарний елемент.
Склад заліза визначає.
А нуклід його природний
Чотири ізотопи має.
Цікавий Ферум елемент.
Він наших роздумів предмет.
Амфотерний і основний
Хоч поділ цей, скоріш, умовний.
Його кислоти пасивують,
Тому завжди у нім мандрують.
З розбавленою кислотою
Ферум буває сам собою.
У чистім кисні спалахтить -
Окалину утворить вмить.
Якщо над полум’ям горить -
Оксид (+2) буде чорніть.
Якщо повільно, ще й з водою,
В народі зветься це - іржою.
Окиснення, як не крути.
Ступінь у ферума (+3).
Сіль кров’яна - червона й жовта -
Знайде залізо де завгодно.
І скаже правильно завжди:
Де Ферум (ІІ) чи Ферум (ІІІ).
Оксиди, солі та основи
Людям служить завжди готові.
Згадаймо комплекси та сплави -
Велика у заліза слава.
Сплав заліза з вуглецем
Є тому всьому вінцем!
Сталь – основа промислова,
А чавун – її підпора!
А який він трудівник,
З вдячністю згадаємо!
Ми на прикладах простих
Це спостерігаємо!
Якщо чорно-білий принтер
Чомусь не працює,
Ультра дисперсний магнетит
Враз його врятує.
А залізний купорос
Силу дужу має.
Від багатьох шкідників
Рослини захищає.
Ферум (ІІ) чи (ІІІ) хлорид,
Якщо розчиняти,
Вийде гарний коагулянт
Щоб воду очищати.
Про здоров’я ми згадаєм,
Анемії скажем «Ні!»,
Бо заліза препарати
Як воїни на війні.
Захищають і лікують,
Стимулюють, активують,
Скрізь показують себе,
На поправку діло йде!
Залізо, за його чесноти,
Людство дуже поважає.
І з великою пошаною
Голову перед ним схиляє.


про публікацію авторської розробки
Додати розробку
