Тема уроку: "Окисно-відновні реакції, їхнє значення".
Тема уроку:Окисно-відновні реакції, їхнє значення.
Мета уроку:
Освітня: поглибити знання учнів про окисно-відновні реакції, навчивши учнів складати рівняння окисно-відновних реакцій методом електронного балансу.
Розвивальна: розвивати вміння і навички роботи в команді, вчити самостійно здобувати знання з різних джерел інформації та оформлювати їх у вигляді презентації, формувати вміння виступати перед аудиторією, використовуючи можливості мультимедійної техніки.
Виховна: виховувати пізнавальний інтерес учнів до вивчення хімії, товариськість і взаємодопомогу.
Програмне забезпечення: програмно-методичний комплекс «Хімія. 9 клас», Microsoft PowerPoint, Word, Paint, Internet Explorer.
Обладнання: Періодична система хімічних елементів Д. І. Менделєєва, пам’ятки з алгоритмом складання рівнянь окисно-відновних реакцій методом електронного балансу, правила визначення ступенів окиснення елементів в речовинах, акумулятор, чорна скринька, бенгальські вогні,
презентація «Окисно- відновні реакції навколо нас».
Стіна цікавих повідомлень. (Учні одержали завдання підготувати повідомлення про одну окисно- відновну реакцію та розмістили своє повідомлення на стіні цікавих повідомлень. План повідомлення: 1) заголовок; 2) рівняння реакції з електронним балансом; 3) значення реакції; 4) малюнок чи фото.)
Тип уроку:комбінований.
Форми роботи: використання таблиць, опорних конспектів, індивідуальна робота, фронтальне опитування, демонстраційний експеримент, розповідь вчителя, робота біля дошки, самостійна робота в зошитах, бесіда.
Базові поняття та терміни: окисно-відновні реакції, окисники, відновники, окиснення, відновлення, метод електронного балансу.
Епіграф: «Знання збираються по краплині, як вода в долоні»
Українське прислів’я
Хід уроку:
 (Слайд 1)
(Слайд 1)
І. Організаційний момент.
Добрий день! Я рада бачити вас всіх в гуморі. Діти! А чи доводилося чути вам, як співає людська душа? Вона може співати від щастя, радості. Наші радість і щастя складаються з успіхів, перемог, просто усмішок, які дарують нам люди. Я бажаю попрацювати на уроці так, щоб у його кінці, прислухавшись до стану своєї душі, ви відчули її спів. Сподіваюсь, ми з вами добре попрацюємо.
 Сьогодні на уроці ми продовжуємо говорить про окисно-відновні реакції, зокрема розглянемо їх значення. (Слайд 2)
Сьогодні на уроці ми продовжуємо говорить про окисно-відновні реакції, зокрема розглянемо їх значення. (Слайд 2)
Отже цілі, які ми ставимо: повторити теоретичний матеріал про окисно-відновні реакції, удосконалити навики складання електронного балансу; розкрити значення окисно-відновних реакцій.
 Діти! Давайте ще раз згадаємо хто ж є основоположником теорії ОВР. (Слайд 3)
Діти! Давайте ще раз згадаємо хто ж є основоположником теорії ОВР. (Слайд 3)
Це відомий український учений, який у 1914 році розробив теорію окисно-відновних реакцій Лев Володимирович Писаржевський.
Діти, для того, щоб я могла оцінити вашу роботу впродовж уроку ви будете заповнювати
Індивідуальну картку оцінювання знань учня ____класу_________________
|
Завдання |
тест |
Робота біля дошки |
Інд.завд., повідомлення |
Додатково |
|
Максимальна кільк. балів |
7 |
2 |
2 |
1 |
|
Набрано балів |
|
|
|
|
|
Всього |
|
|||
(Слайд 4)
ІІ. Актуалізація опорних знань
1.Знайти відповідність (Повторимо основні поняття, що стосуються ОВР, на дошці прикріплено поняття, а вам треба знайти до них відповідне визначення)
- Окисно-відновні реакції – це…
- Відновник –це…
- Окисник – це…
- Окиснення– це…
- Відновлення– це…
- Тільки окисниками можуть бути …
- Тільки відновниками виступають у окисно-ввідновних реакціях…
2. Визначити ступінь окиснення елементів у формулах (Слайд 5)
NaOH, CaCO3 , NO , H2SO4, H2O , NH ,KMnO4, CaO, Na2SO4, CO2 3
3. Вправа на відповідність «Хтось знаходить, а хтось втрачає»
( Завдання роздруковані на листочках. Учні по одному виходять до дошки , прикріплюють під відповідним надписом і пояснюють процес, який відображає схема)
Які процеси відображають схеми?
а) ![]()
![]()
![]() (окиснення)
(окиснення)
б) ![]()
![]()
![]() (відновлення)
(відновлення)
( Обговорення відповідей)
4. (Слайд 6) Покажіть відповідність між рівнянням реакції та речовиною – окисником, яка приймає участь в даній реакції:
- MnO2 +2H2→Mn + 2H2O А. Cu
- SnO + C→ Sn + CO Б. Mn
- 2CuO + C → 2Cu + CO2 В.Sn
Взаємоперевірка відповідей до 2 та 4 завдань (Слайд 7)
Отже, у процесі окисно-відновної реакції відновник віддає електрони, тобто окиснюється; окисник приєднує електрони, тобто відновлюється. Причому будь-яка окисно-відновна реакція являє собою єдність двох протилежних перетворень — окиснення та відновлення, що відбуваються одночасно та без відриву одне від одного.
(Слайд 8) Отже, що означають такі схеми?
![]()
Окиснення: Речовина A як відновник віддає один електрон.
![]()
Відновлення: Речовина В як окисник приймає електрон.
![]()
Окисно-відновнареакція: Речовина Авіддає електрон речовині В.
ІІІ. Мотивація теми.
Слово вчителя
Світ навколо нас великий і різноманітний. Життя оточує нас усюди. Воно існує як у крижаних полярних зонах, так і в розпечених пустелях. Ми зустрічаємо життя всюди, починаючи з освітленої сонцем поверхні моря і закінчуючи самими темними глибинами океану. Під нашими ногами трудиться незліченна кількість мікроорганізмів, роблячи ґрунт родючим і придатним для росту рослин, які, у свою чергу, необхідні іншим формам життя. Земля так насичена життям, що це приголомшує нашу уяву. Життя — це найбільша цінність нашої планети й унікальна її особливість. Навколишній світ — це гігантська «хімічна лабораторія», у якій щомиті відбуваються тисячі реакцій, переважно — окисно-відновні, і доки ці реакції відбуваються, доки є умови для їхнього перебігу, можливо й саме життя.
Показ практичного значення вивчення нового матеріалу.
Перегляд відео «Як утворилась планета Земля»
Навколо нас в природі відбувається велика кількість хімічних реакцій: виверження вулкану, фотосинтез, дихання, травлення… Ми, люди, також широко використовуємо хімічні процеси. Наприклад, горіння сірника, добування металів з руд, приготування їжі та інше. Серед цих процесів велика кількість належить до окисно-відновних реакцій.
Окисно-відновні реакції надзвичайно поширені і важливі. Найважливіші процеси на планеті пов'язані із цим типом хімічних реакцій. В усі часи ці реакції привертали до себе увагу. Вони були оспівані і в літературі, і в музиці, і в образотворчому мистецтві. Де саме вони зустрічаються, яка їх роль в природі і житті людини ми з’ясуємо на сьогоднішньому уроці. А ще я хочу, щоб ви наприкінці уроку дали мені обґрунтовану відповідь на питання: Окисно-відновні реакції – «Добро чи зло»?
Проблемне питання:Фантастична ситуація: А що було б, якби зникли окисно–відновні реакції? ( учні відповідають, метод «мікрофону»)
Вчитель:Отже, вони всюди. Наша планета – величезна макролабораторія.
Презентація з обговоренням.«ОВР НАВКОЛО НАС».
Учні заздалегідь отримали картки з завданням:
- Кожна пара розповідає про значення ОВР. Також учні, на основі вивченого матаріалу, створили «стіну» цікавої інформації до уроку. На сьогоднішньому занятті ми будемо сюди звертатись за додатковою інформацією.
- Готує дослідницький практикум «Навчаю – вчусь»
Сьогодні на уроці кожна пара продемонструє поодному досліду, який ви підготували заздалегідь. І це є секретом для інших, представить його всім, дасть пояснення з точки зору ОВР та де можна використати продукти реакції
Перший учень : значення окисно-відновних процесів в природі.
Другий учень: значення окисно-відновних реакцій в житті людини.
Третій учень: значення окисно-відновних реакцій в техніці.
Четвертий учень: руйнівна роль ОВР.
П’ятий учень: значення окисно-відновних реакцій в побуті.
Шостий учень: значення окисно-відновних реакцій в металургіїі.
Заслуховуються повідомлення учнів.
Також учні, на основі вивченого матаріалу, створили «стіну» цікавої інформації до уроку. На сьогоднішньому занятті ми будемо сюди звертатись за додатковою інформацією.
Прогнозовані результати:

Перший учень: (Слайд 9)
Окисно-відновні реакції найбільш поширені і відіграють значну роль у природі. Завдяки окисно-відновним процесам на ранніх стадіях існування нашої планети утворились гірські породи і мінерали.
(Слайд 10)
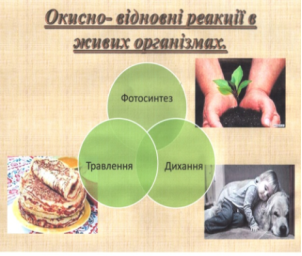 Вони є основою життєдіяльності, адже з ними пов’язані найважливіші функції живої системи – це дихання, обмін речовин, фотосинтез у рослин. Під час дихання органічні речовини окиснюються до кінцевих продуктів - вуглекислого газу і води, використовуючи для цього кисень.
Вони є основою життєдіяльності, адже з ними пов’язані найважливіші функції живої системи – це дихання, обмін речовин, фотосинтез у рослин. Під час дихання органічні речовини окиснюються до кінцевих продуктів - вуглекислого газу і води, використовуючи для цього кисень.
(Слайд 11)
 А під час фотосинтезу вуглекислий газ відновлюється в органічних сполуках, а кисень вивільняється у повітря. Під дією сонячного світла в зелених рослинах відбувається процес фотосинтезу. Він включає десятки хімічних реакцій, однак сумарне рівняння одне:
А під час фотосинтезу вуглекислий газ відновлюється в органічних сполуках, а кисень вивільняється у повітря. Під дією сонячного світла в зелених рослинах відбувається процес фотосинтезу. Він включає десятки хімічних реакцій, однак сумарне рівняння одне:

(Слайд 12 )
)
Процеси гниття, бродіння, тління, утворення перегною; утворення мінеральних солей з перегною в ґрунті - це все окисно-відновні реакції. У живій природі окисно-відновні процеси єосновою всіх процесів обміну речовин, які є джерелом енергії.
(Слайд 13)

Такі процеси, як виверження вулканів, згоряння метеоритних тіл, грозові розряди в атмосфері завжди супроводжуються окисно-відновними процесами.
У 79р. н.е. «загорів» вулкан Везувій. До цього часу він був мальовничою горою, яка на 1300 метрів підносилась над Неаполітанською затокою. Але 24 серпня над Везувієм здійнялась хмара незвичайної форми, яка згодом ставала все темнішою. Посипався попіл, важкі камені, в повітрі відчувався запах спаленої сірки. Виверження вулкану повністю знищило місто Помпей. Місто зникло під шаром попелу, який досягав 3 метрів. Ці окисно-відновні процеси знайшли своє відображення в мистецтві: живопису.
(Слайд 14)
 Видатний російський художник Карл Павлович Брюлов, побувавши у 1830році на місці розкопок давньоримського місця Помпеї, зруйнованого виверженням вулкану Везувію, розпочинає роботу над картиною» «Останній день Помпеї», що вразила сучасників художника своєю романтичною щирістю та величчю і справила сенсацію і в Росії і за
Видатний російський художник Карл Павлович Брюлов, побувавши у 1830році на місці розкопок давньоримського місця Помпеї, зруйнованого виверженням вулкану Везувію, розпочинає роботу над картиною» «Останній день Помпеї», що вразила сучасників художника своєю романтичною щирістю та величчю і справила сенсацію і в Росії і за
кордоном.
(Слайд 15)
 З точки зору хімії у районах вулканів і на дні кратерних озер утворюються поклади самородної сірки. Це відбувається внаслідок таких окисно-відновних реакцій:
З точки зору хімії у районах вулканів і на дні кратерних озер утворюються поклади самородної сірки. Це відбувається внаслідок таких окисно-відновних реакцій:
2H2S + O2 = 2S +2H2O
H2S + 2SO2 = H2SO4+ 2S

(Слайд 16)
Іван Франко оспівував грозу у своєму вірші «Гримить». Послухайте його під музику АнтоніоВівальді, якого також надихали окисно - відновні процеси, що проходять під час грози.
Гримить! Благодатна пора наступає,
Природу розкішная дрож пронимає,
Жде спрагла земля плодотворної зливи,
І вітер над нею гуляє бурхливий,
І з заходу темная хмара летить —
Гримить!
Гримить! Тайна дрож пронимає народи,-
Мабуть, благодатная хвиля надходить...
Мільйони чекають щасливої зміни,
Ті хмари — плідної будущини тіни,
Що людськість, мов красна весна, обновить...
Гримить!
(Слайд 17)
 Під час грози азот сполучається з киснем і утворюється нітроген (ІІ) оксид, який далі перетворюється в нітроген (ІV ) оксид, який сполучається з водою і киснем і на землю ллються кислотні дощі. Завдяки цим процесам на кожний гектар землі щорічно потрапляє від 4 до 15 кг нітрогеновмісних сполук:
Під час грози азот сполучається з киснем і утворюється нітроген (ІІ) оксид, який далі перетворюється в нітроген (ІV ) оксид, який сполучається з водою і киснем і на землю ллються кислотні дощі. Завдяки цим процесам на кожний гектар землі щорічно потрапляє від 4 до 15 кг нітрогеновмісних сполук:
N2+ O2 = 2NO
2NO + O2 = 2NO2
4NO2 + O2 +2H2O = 4HNO3
(Слайд 18)

Другий учень. Окисно-відновні реакції мають велике значення і в житті людини – це отримання тепла в наших домівках при спалювання вугілля, дров, газу, добування багатьох органічних речовин; виробництво цілого ряду будівельних матеріалів, лікарських препаратів, вітамінів, гормонів, ферментів; виробництво кисломолочних  продуктів, сирів, спирту тощо.
продуктів, сирів, спирту тощо.
(Слайд 19)
Природоохоронні заходи, які застосовують для очищення навколишнього середовища, а саме стічних вод і ґрунту від побутового і промислового забруднення ґрунтуються на процесах окиснення і відновлення. Певні види бактерій здатні розкладати, мінералізувати органічні сполуки, які потрапляють у воду та ґру (Слайд 20)
(Слайд 20)
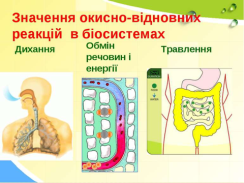 Життя організму неможливе без поповнення його тканин енергією, будівельним матеріалом, вітамінами, мінеральними речовинами і водою. Воно здійснюється за рахунок їжі. Щоб з харчових продуктів вивільнилась енергія і вони стали придатними для включення в обмін речовин. Іжа в травному апараті піддається механічній і хімічній обробці, ця обробка відбувається під впливом ферментів до складових частин, які придатні до всмоктування в кишечнику і подальшого засвоєння в тканинах.
Життя організму неможливе без поповнення його тканин енергією, будівельним матеріалом, вітамінами, мінеральними речовинами і водою. Воно здійснюється за рахунок їжі. Щоб з харчових продуктів вивільнилась енергія і вони стали придатними для включення в обмін речовин. Іжа в травному апараті піддається механічній і хімічній обробці, ця обробка відбувається під впливом ферментів до складових частин, які придатні до всмоктування в кишечнику і подальшого засвоєння в тканинах.
(Слайд 21)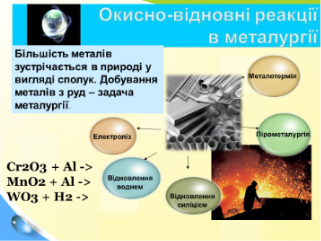
Третій учень. Значення окисно-відновних реакцій в техніці дуже велике. Більшість рідкісних, важливих в техніці металів ( нікель, вольфрам, молібден, хром, алюміній) та інші) отримують за допомогою окисно-відновних реакцій. Найактивніші метали – це лужні та лужноземельні – шляхом електролізу із їх солей. В основі електролізу також лежать окисно-відновні процеси.
Окисно-відновні процеси використовуються в металургії під час виплавки чавуна та сталі, одержання та очищення кольорових металів, рідкісних металів:

(Слайд 2 2)
2)
Виробництво чавуну, сталі, деяких неметалів: фосфору, хлору, йоду; добування амоніаку, нітратної і сульфатної кислот ґрунтуються на окисно-відновних процесах.
(Слайд 2 3)
3)
Четвертий учень: корозія металів, потемніння срібла. Нажаль, продукти харчування мають властивість псуватися. Це також окисно-відновна реакція.
Пожежа неконтрольований процес горіння, що заподіює матеріальну шкоду життю і здоров’ю людей, інтересам суспільства і держави.
(Слайд 24)

На пам'ятниках Тарасу Шевченку, Богдану Хмельницькому в Києві, Петру І в Санкт-Петербурзі (названому «Мідним вершником»), зроблених із бронзи (сплаву міді з оловом) утворюється зелений наліт, який періодично зчищають. Хімічних змін зазнає навіть срібло. Всі знають, що із часом срібні предмети темніють. Але найбільшого впливу кисню на відкритому повітрі за підвищеної вологості зазнає залізо. Іржа «з'їдає» не менш ніж 20 % від усієї його  кількості, що виробляється, а це — мільйони тонн. Явище руйнування металів унаслідок хімічних реакцій з речовинами навколишнього середовища називають корозією.
кількості, що виробляється, а це — мільйони тонн. Явище руйнування металів унаслідок хімічних реакцій з речовинами навколишнього середовища називають корозією.
(Слайд 25)
Залізо, перебуваючи за звичайних умов на повітрі, повільно реагує водночас із киснем і водою (водяною парою). Таке перетворення можна описати схемами:
Fе + О2 + Н2О → Fе(ОН)2
Fе(ОН)2 + О2 + Н2О → Fе(ОН)3
Мідь реагує відразу з трьома речовинами: киснем, водою (водяною парою) і вуглекислим газом, що є у повітрі:
Сu + О2 + H2O + CO2→ (СuОН)2СО3
(Слайд 26)
 Чи замислювались ви, чому картини стародавніх майстрів, наприклад Рафаеля, Леонардо да Вінчі, Фрагонара, мають таку темну палітру?
Чи замислювались ви, чому картини стародавніх майстрів, наприклад Рафаеля, Леонардо да Вінчі, Фрагонара, мають таку темну палітру?
У старовину багато картин писали масляними фарбами, до складу яких входили деякі сполуки Плюмбуму, наприклад, основний карбонат Рb3(ОН)2(СО3)2 - свинцеві білила. Під дією сірководню, що є в повітрі, свинцеві білила перетворювалися на чорний плюмбум(ІІ) сульфід, тому картини поступово тьмяніли:
Рb3(ОН)2(СO3)2 + H2S →PbS + Н2О + СО2.
(Слайд 27)
 Для реставрації картини поверхню її слід обробити будь-яким окисником, наприклад гідроген пероксидом:
Для реставрації картини поверхню її слід обробити будь-яким окисником, наприклад гідроген пероксидом:
РbS + Н2О2 → РbSО4 + Н2О.
Зараз через свою отруйність свинцеві білила в масляних фарбах майже не застосовуються.
(Слайд 28)
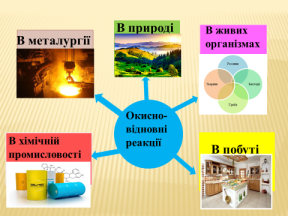 Отже, з цих повідомлень ми дізналися про значення окисно-відновних реакцій у житті людини та розвитку виробництва і можна зробити наступний висновок:
Отже, з цих повідомлень ми дізналися про значення окисно-відновних реакцій у житті людини та розвитку виробництва і можна зробити наступний висновок:
- Окисно-відновні реакції належать до найбільш поширених.
- В живій природі енергія, яка виділяється під час ОВР, забезпечує життєдіяльність організмів.
- ОВР лежать в основі процесів металургії, технічного виробництва амоніаку, нітратної та сульфатної кислот, горіння паливних матеріалів, хімічних джерел
електричного струму.
- Іноді ОВР відіграють негативну роль .
Отже, цей висновок можна вважати підсумком нашого уроку, якщо додати, що крок за кроком накопичувався досвід використання окисно-відновних реакцій. Вивчення цих процесів продовжується і в наш час. Отже, окисно-відновні реакції відіграють надзвичайно важливу роль у природі, виробництві, техніці та побуті.

(Слайд 29)
Ви почули багато цікавого матеріалу, який підготували ваші однокласники. Отже, «Окисно-відновні реакції – «добро чи зло»?
У вас на партах лежать стікери. Ви на них пишете аргумент на користь ОВР, або ж, навпаки, проти ОВР. У нас у класі ось знаходяться терези, на яких ви бачите з одного боку є наліпка «Добро», а з другого боку – «Зло». Відповідно ви поміщаєте на терези свої стікери. І подивимось , що ж у нас переважить
«Окисно-відновні реакції – «добро чи зло»?
V. Дидактична гра «Чорна» скриня .
Діти, ви впродовж вивчення теми готували на уроки цікаві факти про окисно – відновні реакції, а сьогодні я вам підготувала цікавинку – загадку.
(Слайд 30)
 П’ять місяців на поверхні Марсу працював космічний апарат «Фенікс», який передав на Землю багато цінної інформації, зокрема, що на цій планеті є замерзла вода. Але 30 листопада 2008 року NASA (національне управління по аеронавтиці та дослідженні космічного простору) оголосила про завершення його місії, так як з апаратом протягом тижня не могли встановити зв’язку. Найбільш імовірною причиною виходу з ладу Фенікса вчені називають пристрій, аналог якого знаходиться в скрині. Ви з ним добре знайомі, часто користуєтесь його послугами. Що знаходиться в скрині?
П’ять місяців на поверхні Марсу працював космічний апарат «Фенікс», який передав на Землю багато цінної інформації, зокрема, що на цій планеті є замерзла вода. Але 30 листопада 2008 року NASA (національне управління по аеронавтиці та дослідженні космічного простору) оголосила про завершення його місії, так як з апаратом протягом тижня не могли встановити зв’язку. Найбільш імовірною причиною виходу з ладу Фенікса вчені називають пристрій, аналог якого знаходиться в скрині. Ви з ним добре знайомі, часто користуєтесь його послугами. Що знаходиться в скрині?
(Слайд 31)
Метод «Прес» .
Етапи методу:
1. Висловлюємо свою думку: «Я вважаю …»
2. Пояснюємо причину такої точки зору: «Тому, що …»
3. Наводимо додатковіаргументи на підтримкусвоєїпозиції: «Наприклад, …»
4. Узагальнюємо, формулюємо висновки: «Отже …», «Таким чином …»
Отже, питання: «Як ви вважаєте, чи можливе було б виникнення життя на нашій планеті без окисно-відновних реакцій?»
VІ. Підбиття підсумків уроку
Підсумкова бесіда
— Яке завдання стояло перед нами на уроці?
— Який результат нашого уроку?
--- З яким настроєм підійшли до кінця уроку?
 (Слайд 32)
(Слайд 32)
VII. Домашнє завдання. Опрацювати матеріал § 14; Написати казку (фантастичну історію) на тему «Життя на Землі без окисно – відновних реакцій»
Дозаповняйте індивідуальні карти та здайте.
(Слайд 33)

VIІI.Фейеверк - декоративні вогні різноманітних кольорів і форм, які одержують при спалюванні піротехнічних сумішей задля розваги. Піротехнічні суміші містять речовини - окисники.
І закінчимо урок окисно – відновною реакцією.(Підпалити бенгальські вогні)


про публікацію авторської розробки
Додати розробку
