Тестові завдання "Вуглеводні"
Тестові завдання з теми : «Вуглеводні: алкани, алкени, алкіни, алкадієни, арени»
Варіант №1
Рівень А. У завданнях 1-10 позначте правильну відповідь
(кожне завдання оцінюється в 0,5 бали)
1. Вуглеводні – це…
а) сполуки, що мають подібну будову і властивості, але різняться між собою на одну або декілька груп СН2;
б) сполуки, що утворені Карбоном;
в) сполуки до складу яких входять лише два елементи Карбон (С) та Гідроген (Н);
г) сполуки, у яких валентність атома Карбону чотири.
2. Загальна формула алканів:
а) СnH2n+2;
б) СnH2n-2;
в) СnH2n;
г) СnH2n-6.
3. Які сполуки називають гомологами:
а) сполуки, що складаються лише з Карбону та Гідрогену;
б) сполуки, що мають однаковий кількісний і якісний склад, але різну будову;
в) сполуки, що мають подібну будову молекул і подібні властивості, але відрізняються на групу СН2;
г) сполуки Карбону з Нітрогеном.
4. Теорія хімічної будови органічних сполук належить:
а) О.М.Бутлерову;
б) Г. Менделю;
в) А.Лавуазьє;
г) Д.І. Менделєєву.
5. Ненасичений вуглеводень, який має потрійний зв’язок – це:
а) етилен;
б) ацетилен;
в) хлорметан;
г) бензен.
6. Сьомий представник гомологічного ряду етиленових має назву:
а) гептен;
б) гептін;
в) гексан ;
г) гексін.
7. Вкажіть, які фізичні властивості характеризують етилен:
а) безбарвний газ, майже без запаху, малорозчинний у воді. У природі у вільному стані не зустрічається. Утворюється під час переробки нафти;
б) газ блакитного кольору, не розчиняється у воді;
в) рідина із специфічним запахом, кипить при температурі 80 ᵒС;
г) безбарвний газ, майже без запаху, розчинний у воді і у органічних розчинниках.
8. Які продукти реакції утворюються при горінні бензену:
а) СО та Н2О;
б)СО2 та Н2О;
в) С2Н2 та Н2О;
г) С2Н2 та СО2.
9. Який тип реакцій характерний для насичених вуглеводнів:
а) обміну;
б) заміщення;
в) приєднання;
г) окиснення.
10. При гідратації етилену утворюється:
а) етиловий спирт;
б) оцтовий альдегід;
в) брометан;
г) оцтова кислота.
Рівень Б. У завдання 11-12 встановіть відповідності та закінчіть речення
(кожне завдання оцінюється в 1,5 бали)
11. Встановіть відповідність між реакцією та її назвою:
А. Гідратація 1. СН2=СН2 + Н2 → СН3-СН3
Б. Гідрування 2. СН2=СН2 + Н2О → С2Н5ОН
В. Крекінг 3. СН4 → С+2Н2
12. Закінчіть речення:
а) Гомологи – це...
б) СnH2n-1 – формула…
Рівень В. У завдання 13-14 дайте розгорнуту відповідь
(кожне завдання оцінюється в 2 бали)
13. Порівняйте хімічні властивості насичених та ненасичених вуглеводнів. Наведіть приклади хімічних реакцій.
14. Зобразити структурну та електронну формулу бутану.
Тестові завдання з теми : «Вуглеводні: алкани, алкени, алкіни, алкадієни, арени»
Варіант №2
Рівень А. У завданнях 1-10 позначте правильну відповідь
(кожне завдання оцінюється в 0,5 бали)
1. Насичені вуглеводні – це…
а) сполуки, що мають подібну будову і властивості, але різняться між собою на одну або декілька груп СН2;
б) сполуки, що утворені Карбоном;
в) сполуки до складу яких входять лише два елементи Карбон (С) та Гідроген (Н);
г) сполуки, що складаються з Карбону на Гідрогену, в яких усі валентності атомів Карбону, що вільні після утворенням зв’язків С-С, насичені атомами Гідрогену.
2. Загальна формула алкінів:
а) СnH2n+2;
б) СnH2n-2;
в) СnH2n;
г) СnH2n-6.
3. Що таке ізомери?
а) сполуки, що складаються лише з Карбону та Гідрогену;
б) сполуки, що мають однаковий кількісний і якісний склад, але різну будову;
в) сполуки, що мають подібну будову молекул і подібні властивості, але відрізняються на групу СН2;
г) сполуки Карбону з Нітрогеном.
4. Алкадієни ( прості дієни) - це:
а) вуглеводні з одним потрійним зв’язком ;
б) вуглеводні з двома подвійними зв’язками ;
в) вуглеводні з одинарними зв’язками ;
г) вуглеводні з двома потрійними зв’язками.
5. Ненасичений вуглеводень, який має подвійний зв’язок – це:
а) етилен;
б) ацетилен;
в) гептадієн;
г) бензен.
6. Дев’ятий представник гомологічного ряду ацетиленових має назву:
а) нонін;
б) октін;
в) октен ;
г) нонен.
7. Вкажіть, які фізичні властивості характеризують бензол:
а) безбарвний газ, майже без запаху, малорозчинний у воді. У природі у вільному стані не зустрічається. Утворюється під час переробки нафти;
б) газ блакитного кольору, не розчиняється у воді;
в) рідина із специфічним запахом, кипить при температурі 80 ᵒС;
г) безбарвний газ, майже без запаху, розчинний у воді і у органічних розчинниках.
8. Які продукти реакції утворюються при горінні метану:
а) СО та Н2О;
б)СО2 та Н2О;
в) С2Н2 та Н2О;
г) С2Н2 та СО2.
9. Який тип реакцій характерний для ненасичених вуглеводнів:
а) обміну;
б) заміщення;
в) приєднання;
г) окиснення.
10. При гідрування етену утворюється:
а) пропанол;
б) етан;
в) оцтова кислота;
г) бутадієн.
Рівень Б. У завдання 11-12 встановіть відповідності та закінчіть речення
(кожне завдання оцінюється в 1,5 бали)
11. Встановіть відповідність між реакціями та їх продуктами:
А. С6Н6 + Br2 1. С6Н5CH3+ HBr
Б. С6Н6 + CH3Br 2. CHBr3 + HBr
В. CH2Br2 + Br2 3. С6Н5Br + HBr
12. Закінчіть речення:
а) Ароматичні вуглеводні – це...
б) СnH2n-2 – формула …
Рівень В. У завдання 13-14 дайте розгорнуту відповідь
(кожне завдання оцінюється в 2 бали)
13. Порівняйте хімічні властивості насичених та ароматичних вуглеводнів. Наведіть приклади хімічних реакцій.
14. Зобразити структурну та електронну формулу бензолу.
Тестові завдання з теми : «Основні класи неорганічних сполук»
Варіант №1
Рівень А. У завданнях 1-10 позначте правильну відповідь
(кожне завдання оцінюється в 0,5 бали)
1.Оксиди – це…
а) сполуки, що мають подібну будову і властивості, але різняться між собою на одну або декілька груп СН2;
б) сполуки, що утворені декількома елементами, одним з яких є Оксиген;
в) сполуки до складу яких входять лише два елементи Карбон (С) та Гідроген (Н);
г) сполуки, що складаються з Гідрогену та кислотного залишку.
2. Користуючись витискувальним рядом металів, визначте, який метал витісняє водень із кислот:
а) Ag;
б) Pt;
в) Сu;
г) Fe.
3. Формула нітратної кислоти:
а)NO2;
б)HNO2;
в)NaOH;
г)НNO3.
4. У якому середовищі лакмус має фіолетове забарвлення?
а) нейтральному;
б) кислому ;
в) лужному ;
г) його не використовують як індикатор.
5. Хімічне рівняння ... + НС1 → FeCl2 + Н2 буде правильним, якщо крапки замінити на:
а) Fe;
б) Fe3O4;
в) FeO;
г) Fe2O3.
6. Яке з перерахованих тверджень не є характерним для кислот?
а) взаємодіють з кислотними оксидами ;
б) взаємодіють з основними оксидами;
в) змінюють забарвлення індикаторів;
г) майже всі кислоти безбарвні .
7. Оксигеновмісна кислота:
а) хлоридна;
б) бромводнева;
в) сульфатна;
г) йодводнева.
8. До основних оксидів належить:
а) HNO3;
б) Fe2O3;
в) CaCl2;
г) NaOH.
9. Формула сульфур (IV) оксиду:
а) SiO2;
б) SO3;
в) SO2;
г) H2S03.
10. Вкажіть речовину, яка на Землі перебуває в рідкому, твердому і газоподібному стані:
а)H2O;
б) SiCl4;
в) А1203;
г) НС1.
Рівень Б. У завдання 11-12 напишіть рівняння та закінчіть речення
(кожне завдання оцінюється в 1 бал)
11. Складіть рівняння реакції між калієм і ортофосфатною кислотою і розрахуйте загальну суму коефіцієнтів.
12. Закінчіть речення:
а) Основи – це...
б) Кислоти поділяють на…..
Рівень В. У завдання 13-14 дайте розгорнуту відповідь
(кожне завдання оцінюється в 2,5 бали)
13. Яка маса сульфур (IV) оксиду прореагувала з водою, якщо в результаті утворилося 0,82 г сульфітної кислоти?
14. Допишіть рівняння реакцій, назвіть продукти реакції:
а) Zn(OH)2 + H2SО4 →
б) КОН + H2SО3 →
в) FeO + HCl →
г) А12О3 + H2SО4 →
д) Ca(OH)2+SО2 →
Тестові завдання з теми : «Основні класи неорганічних сполук»
Варіант №2
Рівень А. У завданнях 1-10 позначте правильну відповідь
(кожне завдання оцінюється в 0,5 бали)
1.Кислоти – це…
а) сполуки, що мають подібну будову і властивості, але різняться між собою на одну або декілька груп СН2;
б) сполуки, що утворені декількома елементами, одним з яких є Оксиген;
в) сполуки до складу яких входять лише два елементи Карбон (С) та Гідроген (Н);
г) сполуки, що складаються з Гідрогену та кислотного залишку.
2. Користуючись витискувальним рядом металів, визначте, який метал витісняє водень із кислот:
а) Ag;
б) Mn;
в) Hg;
г) Au.
3. Формула сульфідної кислоти:
а) H2S;
б) H2SiO3;
в) H2SO4;
г) H2SO3.
4. У якому середовищі метилоранж має червоне забарвлення?
а) нейтральному;
б) кислому ;
в) лужному ;
г) його не використовують як індикатор.
5. Хімічне рівняння СO2 + Н2О = ... буде правильним, якщо крапки замінити на:
а) СНзСООН;
б) Н2СO3;
в) Н2С204;
г) CO.
6. Яке з перерахованих тверджень не є характерним для кислот?
а) взаємодіють з кислотними оксидами ;
б) взаємодіють з основними оксидами;
в) змінюють забарвлення індикаторів;
г) майже всі кислоти безбарвні .
7. Безоксигеновмісна кислота:
а) нітратна;
б) бромводнева;
в) сульфатна;
г) ортофосфатна.
8. До кислотних оксидів належить:
а) HNO3;
б) Fe2O3;
в) СО2;
г) СO.
9. Формула сульфітної кислоти:
а) SiO2;
б) Н2S;
в) Н2SO4;
г) H2SО3.
10. Al2O3 належить до:
а) амфотерних оксидів;
б) кислотних оксидів;
в) основних оксидів;
г) солей.
Рівень Б. У завдання 11-12 напишіть рівняння та закінчіть речення
(кожне завдання оцінюється в 1 бал)
11. Складіть рівняння реакції між алюмінієм і сульфатною кислотою і розрахуйте загальну суму коефіцієнтів.
12. Закінчіть речення:
а) Кислоти – це...
б) Оксиди поділяють на…..
Рівень В. У завдання 13-14 дайте розгорнуту відповідь
(кожне завдання оцінюється в 2,5 бали)
13. Який об’єм водню (н.у.) виділиться, якщо з водою прореагує 3,9 г калію?
14. Допишіть рівняння реакцій, назвіть продукти реакції:
а) Cu(OH)2+HBr →
б) ZnO + H2SO4 →
в) Fe2О3 + HCl →
г) КОН + N2О5 →
д) Ва(ОН)2+СО2 →
Тестові завдання з теми : «Основні класи неорганічних сполук. Кислоти.»
Варіант №1
Рівень А. У завданнях 1- 4 позначте правильну відповідь
(кожне завдання оцінюється в 1 бал)
1. Позначте формулу нітратної кислоти:
A. HNО2
Б. H2SО4
B. HNО3
Г. НВг
2. Установіть відповідність між формулою кислоти та її назвою:
A. H2S 1. Сульфатна
Б. Н3РО4 2. Сульфідна
B. H2SО4 3. Ортофосфатна
Г. Н2СО3 4. Хлоридна
5. Карбонатна
3. Установіть відповідність між назвою кислоти і групою, до якої вона належить:
A. Сульфітна
Б. Бромідна
B. Сульфідна
Г. Нітратна
1. Одноосновна, безоксигенова
2. Одноосновна, оксигеновмісна
3. Двохосновна, оксигеновмісна
4. Двохосновна, безоксигенова
4. Установіть відповідність між вихідними речовинами та продуктами реакцій:
A. Алюміній і сульфатна кислота
Б. Натрій і ортофосфатна кислота
B. Кальцій і хлоридна кислота
1. СаСl2+Н2
2. Na3PО4+H2
3. A12(SО4)3 + H2
Рівень Б. У завданнях 5 - 7 виконайте завдання і запишіть відповідь
(кожне завдання оцінюється в 2 бали)
- Знайдіть масу солі, яка утвориться в результаті зливання 0,5 л розчину з масовою часткою натрій гідроксиду 20% (густина 1,22 г/см3) і 0,5 кг розчину з масовою часткою сульфатної кислоти 19,6%.
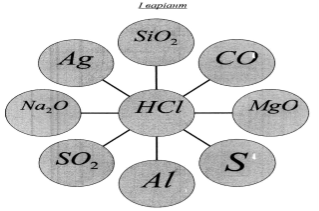
- З'єднайте рисками формулу хлоридної кислоти та формули тих речовин, з якими вона може вступати в хімічну реакцію. Написати рівняння реакцій, вказати типи реакцій.
- Складіть рівняння реакції між натрієм і ортофосфатною кислотою і розрахуйте загальну суму коефіцієнтів.
Рівень В. У завданні 8 замість крапок вставте пропущені слова
( завдання оцінюється в 2 бали)
- Формула сульфатної кислоти - …..
Фізичні властивості сульфатної кислоти –
Хімічні властивості сульфатної кислоти –
Галузі застосування сульфатної кислоти –
Тестові завдання з теми : «Основні класи неорганічних сполук. Кислоти.»
Варіант №2
Рівень А. У завданнях 1- 4 позначте правильну відповідь
(кожне завдання оцінюється в 1 бал)
1. Позначте формулу ортофосфатної кислоти:
A. HРО3
Б. H2SО4
B. H3РО4
Г. НВг
2. Установіть відповідність між формулою кислоти та її назвою:
A. HСІ 1. Сульфітна
Б. Н3РО4 2. Сульфідна
B. H2S 3. Ортофосфатна
Г. Н2СО3 4. Хлоридна
5. Карбонатна
3. Установіть відповідність між назвою кислоти і групою, до якої вона належить:
A. Хлоридна
Б. Карбонатна
B. Сульфідна
Г. Нітратна
1. Одноосновна, безоксигенова
2. Одноосновна, оксигеновмісна
3. Двохосновна, оксигеновмісна
4. Двохосновна, безоксигенова
4. Установіть відповідність між вихідними речовинами та продуктами реакцій:
A. Барій і хлоридна кислота
Б. Магній і ортофосфатна кислота
B. Алюміній і хлоридна кислота
1. АlСl3 + Н2
2. Mg3(PО4)2 + H2
3. ВаСl2+Н2
Рівень Б. У завданнях 5 - 7 виконайте завдання і запишіть відповідь
(кожне завдання оцінюється в 2 бали)
- У розчин сульфатної кислоти масою 200 г з масовою часткою 0,2% опустили 9,5 г магнію. Визначити об’єм газу, який утворився внаслідок реакції.
- З'єднайте рисками формулу сульфатної кислоти та формули тих речовин, з якими вона може вступати в хімічну реакцію. Написати рівняння реакцій, вказати типи реакцій.

- Складіть рівняння реакції між ферумом і сульфатною кислотою і розрахуйте загальну суму коефіцієнтів.
Рівень В. У завданні 8 замість крапок вставте пропущені слова
( завдання оцінюється в 2 бали)
- Формула хлоридної кислоти - …..
Фізичні властивості хлоридної кислоти –
Хімічні властивості хлоридної кислоти –
Галузі застосування хлоридної кислоти…
Тестові завдання з теми : «Природні джерела вуглеводнів»
Варіант №1
Рівень А. У завданнях 1- 10 позначте правильну відповідь
(кожне завдання оцінюється в 0,5 бала)
1. Нафта – …
A. безбарвна рідина, без запаху;
Б. масляниста рідина темно-бурого або майже чорного кольору з характерним запахом;
B. рідина бурого кольору, що не має запаху;
Г. газ блакитного кольору.
2. За хімічним складом нафта – це…
A. складна суміш вуглеводнів з різною молекулярною масою, головним чином рідких, з домішками інших органічних речовин;
Б. складна суміш вуглеводнів з різною молекулярною масою, головним чином твердих, з домішками інших неорганічних речовин;
B. складна суміш вуглеводнів з однаковою молекулярною масою, головним чином твердих, з домішками інших органічних речовин;
Г. складна суміш вуглеводнів з різною молекулярною масою, головним чином рідких, з домішками інших неорганічних речовин.
3. Для підвищення виходу бензину і поліпшення його якості застосовують процес, який називається:
A. гідруванням;
Б. перегонкою;
B. крекінгом;
Г. гідратацією.
4. Вкажіть температуру кипіння лігроїну:
A. від 120 до 240;
Б. від 180 до 240;
B. від 270 до 350;
Г. від 300 і вище.
5. Основною складовою частиною природного газу є:
A. бутан;
Б. пропан;
B. ацетилен;
Г. метан.
6. Вкажіть розміри молекул газойлю:
А. С12 – С18;
Б. С18 – С25;
B. С8 – С14;
Г. С5 – С11.
7. Природний газ, нафта, вугілля належать до:
A. термічних;
Б. невідновлювальних;
B. відновлювальних;
Г. каталітичних.
8. Крекінг поділяють на:
A. каталітичний та заміщений;
Б. обмінний та термічний;
B. обмінний та каталітичний;
Г. каталітичний та термічний..
9. Вкажіть застосування мазуту:
A. котельне рідке паливо, парафін, гудрон, вазелін;
Б. моторне, авіаційне і автомобільне паливо;
B. пальне для дизелів і тракторних двигунів;
Г. пальне для тракторів, розчинник у лакофарбовій промисловості.
10. Яка масова частка метану в природному газі:
A. 80-90%;
Б. 35-65%;
B. 100%;
Г. 15-35%.
Рівень Б. У завданнях 11 - 12 встановіть відповідність та закінчить речення
(кожне завдання оцінюється в 2 бали)
- Встановіть відповідність між вуглеводневою фракцією та розміром її молекул:
A. Лігроїн; 1. С8 - С14
Б. Мазут; 2. С18 – С25
B. Газойль; 3. С5 - С11
Г. Бензин. 4. Від С20 і вище.
12. Супутні нафтові гази є сумішшю…..
Рівень В. У завданні 13 розв’яжіть задачу
( завдання оцінюється в 3 бали)
- Природний газ одного з родовищ складається з 85% метану, 8% етану, 2% пропану, 2% азоту і 3% вуглекислого газу. (Склад даний в об’ємних частках). Обчисліть, скільки повітря необхідно для спалювання цього газу об’ємом 2 м3 (н.у.)? Об’ємну частку кисню в повітрі прийняти рівною 21%.
Тестові завдання з теми : «Природні джерела вуглеводнів»
Варіант №2
Рівень А. У завданнях 1- 10 позначте правильну відповідь
(кожне завдання оцінюється в 0,5 бала)
1. Нафта – …
A. складна суміш вуглеводнів з різною молекулярною масою, головним чином твердих, з домішками інших неорганічних речовин;
Б. складна суміш вуглеводнів з різною молекулярною масою, головним чином рідких, з домішками інших органічних речовин;
B. складна суміш вуглеводнів з однаковою молекулярною масою, головним чином твердих, з домішками інших органічних речовин;
Г. складна суміш вуглеводнів з різною молекулярною масою, головним чином рідких, з домішками інших неорганічних речовин.
2. За хімічним складом супутні гази – це…
A. складна суміш вуглеводнів з різною молекулярною масою, головним чином рідких, з домішками інших органічних речовин;
Б. складна суміш вуглеводнів з різною молекулярною масою, головним чином твердих, з домішками інших неорганічних речовин;
B. складна суміш легких вуглеводнів з меншим вмістом метану (до 40 %) і високим вмістом його гомологів;
Г. складна суміш легких вуглеводнів з високим вмістом метану (до 90 %) і малим вмістом його гомологів;
3. В результаті якого процесу нерозгалужені сполуки перетворюються в більш розгалужені молекули:
A. гідрування;
Б. перегонки;
B. крекінгу;
Г. гідратації.
4. Вкажіть температуру кипіння мазуту:
A. від 120 до 240;
Б. від 180 до 240;
B. від 270 до 350;
Г. від 300 і вище.
5. Які гомологи містяться в природному газі:
A. бутан, етан, пропан;
Б. бензен,етилен, ацетилен;
B. метан, ацетилен, бензен;
Г. метан та бензен.
6. Вкажіть розміри молекул гасу:
А. С12 – С18;
Б. С18 – С25;
B. С8 – С14;
Г. С5 – С11.
7. Первинна переробка нафти полягає в:
A. перетворенні нерозгалужених сполук у більш розгалужені молекули;
Б. розщепленні низькокиплячих фракцій у сполуки з більшою молекулярною масою;
B. розщепленні важкокиплячих фракцій (гасової) у сполуки з меншою молекулярною масою;
Г. перегонці, тобто розділенні на різні продукти (фракції).
8. На виробництві перегонка нафти здійснюється у:
A. трубчастій печі;
Б. ректифікаційні колоні;
B. доменній печі;
Г. теплообміннику.
9. Вкажіть застосування газойлю:
A. котельне рідке паливо, парафін, гудрон, вазелін;
Б. моторне, авіаційне і автомобільне паливо;
B. пальне для дизелів, котельне паливо;
Г. пальне для тракторів, розчинник у лакофарбовій промисловості.
10. Яка масова частка метану в супутному газі:
A. 80-90%;
Б. до 40%;
B. 100%;
Г. 15-35%.
Рівень Б. У завданнях 11 - 12 встановіть відповідність та закінчить речення
(кожне завдання оцінюється в 2 бали)
- Встановіть відповідність між вуглеводневою фракцією та температурою кипіння її компонентів:
A. Лігроїн; 1. Від 270 до 350;
Б. Мазут; 2. Від 120 до 240;
B. Газойль; 3. Від 40 до 200;
Г. Бензин. 4. Від 300 і вище.
12. На відміну від природного газу, в супутних газах … вміст метану до … %, а … його …
Рівень В. У завданні 13 розв’яжіть задачу
( завдання оцінюється в 3 бали)
- Природний газ одного з родовищ складається з 92% метану, 3% етану, 1,6% пропану, 2% азоту, 0,4% бутану і 1% інші негорючі гази. (Склад даний в об’ємних частках). Обчисліть, скільки повітря необхідно для спалювання цього газу об’ємом 5 м3 (н.у.)? Об’ємну частку кисню в повітрі прийняти рівною 21%.
Тестові завдання з теми : «Бензен як представник ароматичних вуглеводнів»
Варіант №1
Рівень А. У завданнях 1- 10 позначте правильну відповідь
(кожне завдання оцінюється в 0,5 бала)
1. Вкажіть клас органічних сполук, представником яких є бензен:
A. алкани;
Б. арени;
B. алкіни;
Г. алкени.
2. Виберіть твердження, яке відповідає реакції горіння вуглеводнів:
A. каталітичне відщеплення водню від молекул;
Б. перетворення молекул нормальної будови в розгалужені;
B. розщеплення молекул та утворення сполук з меншою молекулярною масою;
Г. окисно-відновна взаємодія з киснем, що призводить до утворення вуглекислого газу та води.
3. Визначте тип реакції, найхарактерніший для ароматичних вуглеводнів:
A. приєднання;
Б. заміщення;
B. полімеризації;
Г. циклізації.
4. Виберіть суміш для нітрування бензену:
A. H2SO4 та NO2;
Б. NH3 та HNO2;
B. H2SO4 та HNO2;
Г. H2SO4 та HNO3.
5. Вкажіть сполуку, з якої добувають бензен в промисловості:
A. гексан;
Б. ацетилен;
B. метан;
Г. циклогексан.
6. Вкажіть природну сировину для одержання бензену:
А. кам’яне вугілля;
Б. підземні води;
B. гірничі поклади;
Г. торф.
7. Вкажіть сполуку, яка утворюється при повній гідрогенізації бензену:
A. гексан;
Б. гексен;
B. циклогексан;
Г. циклогексен.
8. Встановіть сполуку, яка утворюється при взаємодії бензену з хлором при освітленні:
A. хлорбензен;
Б. 1,3-дихлорбензен;
B. 1,2,3,4,5,6-гексахлорциклогексан;
Г. 1,3,5-трихлорбензен.
9. В присутності яких каталізаторів проходить галогенування бензену:
A. FeBr3, AlCl3;
Б. Pt;
B. V;
Г. NH3.
10. Продукт заміщення всіх шести атомів Гідрогену на атоми Хлору – гексахлоробензен, використовується для:
A. протравлювання насіння зернових культур перед висівання;
Б. для боротьби зі шкідниками;
B. для усунення грибкових захворювань;
Г. для боротьби із бур’янами.
Рівень Б. У завданнях 11 - 13 встановіть послідовність та відповідність
(кожне завдання оцінюється в 1,5 бали)
- Встановіть відповідність між формулами та назвами речовин:
A. C6H5Cl 1. гексахлорциклогексан;
Б. C6H5NO2 2. циклопентан;
B. C6H12 3. хлорбензен;
Г. C5H10 4. циклогексан;
Д. C6H5Cl6 5. нітробензен;
- Встановіть послідовність реагентів для здійснення перетворень СН4 → С2Н2 → С6Н6 → C6H5Cl
A.t = 1500 C;
Б.Cl2, AlCl3;
B. C, 500 С;
Г. Pt, 300 С;
Д. Cl2, світло;
Е. CH3Cl ,Na (мет.).
- Встановіть відповідність між реакцією та продуктами реакцій:
A. C6H6 + Br2 1. C6H5CH3 + HBr
Б. C6H6 + 3Сl2 2. C6H5 Br +HBr
B. C6H6 + CH3Br 3. C6H5Cl6
Г. C6H6 + 3H2 4. C6H12
Рівень В. У завданні 14 розв’яжіть задачу ( завдання оцінюється в 2,5 бали)
- Визначити масу бензену, отриманого при пропусканні 210 кг циклогексану над платиновим каталізатором, якщо масова частка виходу бензену складає 0,85 від теоретично можливого.

про публікацію авторської розробки
Додати розробку
