Урок "Електролітична дисоціація"
nvk13kovel
![]() Комунальний заклад «Навчально-виховний комплекс
Комунальний заклад «Навчально-виховний комплекс
«Загальноосвітня школа І-ІІІ ст.. № 13 – колегіум» м. Ковеля»
Підсумковий урок з теми
«Електролітична дисоціація»
Підготувала:
вчитель хімії
Палашевська
Мирослава Петрівна
Мета: Узагальнити і систематизувати набуті знання про речовини-електроліти, явище електролітичної дисоціації, розвивати в учнів вміння мислити логічно та послідовно, використовувати теоретичні знання на практиці.
Тип уроку: підсумково-узагальнюючий, нестандартний, з ігровими елементами.
Обладнання: підручники, таблиці розчинності електролітів, картки з завданнями, набір реактивів (розчини електролітів), пробірки.
Хід уроку
І. Організаційний момент.
ІІ. Повідомлення теми і мети уроку.
ІІІ. Актуалізація опорних знань.
Фронтальна бесіда з класом.
- Які речовини називають електролітами?
- Які класи речовин належать до електролітів?
- Який процес називають дисоціацією?
- Що таке ступінь дисоціації? За якою формулою визначається?
- На які групи поділяються електроліти?
- Які частини утворюються під час дисоціації електролітів?
- Що називають аніонами? Катіонами?
- Які іони утворюються в результаті дисоціації HNO3, MgCl2, Ca(OH)2 (написати на дошці).
- Які речовини дисоціюють ступінчасто?
- Які реакції називаються реакціями іонного обміну?
- В яких випадках реакції іонного обміну відбуваються до кінця?
IV. Узагальнення і систематизація знань
- На демонстраційному столі є набір реактивів (розчини електролітів)
CuSO4; Na2CO3; HCl; NaOH; H2SO4. Довести за допомогою експерименту утворення осаду, газоподібної сполуки, малодисоційованої сполуки та записати на дошці молекулярні, повні та скорочені йонні рівняння реакцій.
а) 1 учень – утворення осаду
CuSO4+2NaOH→Cu(OH)2+Na2SO4
Cu2++SO2-+2Na++2OH→Cu(OH)2↓+2Na++SO42-
Cu2++2OH-→Cu(OH)2↓
б) 2 учень – утворення газоподібної сполуки:
Na2CO3+2HCl→2NaCl+CO2↑+H2O
2Na++CO32-+2H++2Cl-→2Na++2Cl-+CO2↑+H2O
Co32-+2Cl+→CO2↑+H2O
в) 3 учень – утворення малодисоційованої сполуки:
2NaOH+H2SO4→Na2SO4+2H2O
![]()
![]()
![]()
Всі учні класу працюють над цим завданням самостійно в робочих зошитах.
1 ряд –утворення осаду.
2 ряд – утворення газоподібної сполуки
3 ряд – утворення малодисоційованої сполуки
- Гра «Хрестики-нулики»
|
1 |
2 |
3 |
|
4 |
5 |
6 |
|
7 |
8 |
9 |
Грають два учні за правилами гри «хрестики-нулики». За кожним номером є завдання. Виграє той, хто перший закреслить лінію.
-
Які речовини потрібно взяти для протікання реакції:

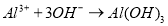

- Яка із речовин у водному розчині дисоцією з утворенням іону Cu2+^
a) CuCl2 b) Cu2O
3. Які йони утворюються в результаті дисоціації H2SO4.
4. Які йони змінюють універсальний індикатор на червоний колір.
5. Які йони змінюють універсальний індикатор на синій колір.
6. Які йони змінюють фенол-фталеїн на червоний колір.
7. Які речовини необхідно взяти, щоб пройшла реакція нейтралізації.
8. Вкажіть сильний електроліт:
H2CO3, H2SiO3, H2SO4
9. Яка з зазначених речовин проводить електричний струм:
а) спирт
б) бензин
в) суха NaCl
г) розчин NaCl
Вчитель викликає до дошки двох учнів для розв’язання задач по даній темі.
1 учень. Які кількості речовини іонів утвориться при розчиненні у воді 0,1 моль НІ?
2 учень. Мікстура масою 100г. містить 2 г. NaBr. Яка маса брому у вигляді Br- міститься у мікстурі?.
Для учнів всього класу завдання на дошці. Обчислити кількість іонів Al3+, що утворились в результаті дисоціації 133,5г. розчину з масовою часткою AlCl3 10%.
Висновок
IV. Як результат уроку необхідно оцінити набуті знання учнів з даної теми.
V. Підсумок
На сьогоднішньому уроці узагальнили і систематизували набуті знання учнів про речовини-електроліти, явище електролітичної дисоціації, взаємодію речовин-електролітів, реакції іонного обміну.
Д/з. Виконати вправи 57, 58


про публікацію авторської розробки
Додати розробку
