Урок. "Кислота на кухні"


















Актуальність проекту. Одним із актуальних напрямів інноваційного розвитку природничої освіти є STEM-орієнтований підхід до навчання. STEM-освіта має на меті комплексно формувати ключові фахові, соціальні й особистісні компетенції учнів, які, в подальшому, визначають конкурентну спроможність на ринку праці: критичного мислення, творчості, здатності і готовності до розв’язання комплексних задач (проблем), співпраці, управління, здійснення інноваційної діяльності та ін. Проект розроблений на основі основного курсу хімії для 9 класу. В основі розробки інтеграція природничих наук, що є основою STEM-ocвіти. Учні отримують завдання, попередньо об’єднавшись в групи. На уроці команди демонструють знання з предметів природничого циклу, об’єднують інформацію та роблять висновок стосовно оцтової кислоти, її властивостей, сфери добування та застосування.
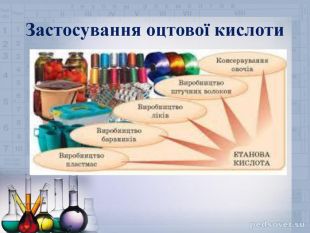
Завдання проекту. Навчити працювати з різними джерелами інформації;Розкрити історію відкриття та походження оцтової кислоти;Розрізняти та розраховувати масову частку кислоти в розчинні;Скласти рівняння хімічних реакцій оцтової кислоти;Використовувати здобуті знання та навички в побуті для раціонального використання кислоти в різних сферах; Володіти навичками для використання оцтової кислоти в кулінарії;Обґрунтувати значення розчинів оцтової кислоти у природі та житті людини;Оцінити роль оцтової кислоти в виробництві лікарських та косметичних виробах; Організувати просвітницьку роботу серед учнів школи.
Етапи проекту. На уроці хімії визначити: - форми та методи дослідження, створити групи, - розподілити функцій між учасниками; - об’єднати учнів в 6 груп:1 група – «Історики. Географи»; 2 група – «Хіміки»;3 група – «Фізики. Технологи»;4 група – «Біологи»;5 група – «Математики»;6 група – «Інформатики».
Історія – Географія. Найперша згадка про оцет відноситься до стародавнього Вавилону і датується 5000 р до н. е. У Китаї перші письмові згадки оцту відносяться до періоду династії Чжоу (247р. до н. е.), а в Японії - до правління імператора Одзин (399 – 404 н. е.). Той факт, що оцет зі спирту виробляють оцтовокислі бактерії, був доведений в 1864 році Луї Пастером.
Фізика – Технології Формула: CH3 COOHМолярна маса: 60,052 г/моль. Структурна формула: Кульково-стрижнева модель. Молекулярна формула: CH3 COOH, C2 H4 O2 Систематична назва: Етанова кислота. Молекулярна маса: 60,053 г/моль Оцтова кислота – безбарвна, прозора гігроскопічна рідина, яка необмежено розчиняється у воді.
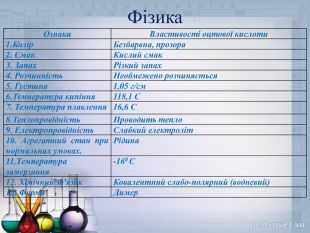
Фізика. Ознаки. Властивості оцтової кислоти1. Колір. Безбарвна, прозора2. Смак. Кислий смак3. Запах. Різкий запах4. Розчинність. Необмежено розчиняється5. Густина1,05 г/см 6. Температура кипіння118,1 С7. Температура плавлення16,6 С8. Теплопровідність. Проводить тепло9. Електропровідність. Слабкий електроліт10. Агрегатний стан при нормальних умовах. Рідина11. Температура замерзання -160 С12. Хімічний зв'язок Ковалентний слабо-полярний (водневий)13. Форма. Димер
Хімія. Хімічні властивості етанової кислотиа) металами2 CH3 СООН + Mg →(CH3 COO)2 Mg + H2 Утворена сіль – магній етаноат (історична назва – ацетат магнію);б) основними оксидами2 CH3 СООН + Са. О →(CH3 COO)2 Са+ H2 О;в) лугами. CH3 CООН + Na. OH → CH3 COONa + H2 Oг) солями ( слабкіших за неї кислот, наприклад карбонами, силікатами)2 CH3 СООН + Na2 СО3→ 2 CH3 COONa + H2 О + CO2
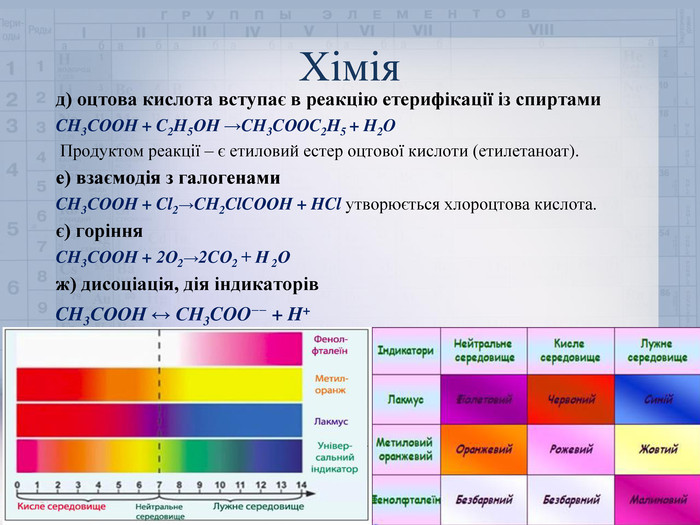
Хіміяд) оцтова кислота вступає в реакцію етерифікації із спиртами CH3 СООН + C2 H5 ОН →CH3 CОOC2 H5 + H2 O Продуктом реакції – є етиловий естер оцтової кислоти (етилетаноат). е) взаємодія з галогенами CH3 СООН + Cl2→CH2 Cl. CООН + HCl утворюється хлороцтова кислота.є) горіння. CH3 СООН + 2 О2→2 CО2 + Н 2 Ож) дисоціація, дія індикаторів. CH3 COOH ↔ CH3 COO−− + H+
Математика. Задача 1. Добути 50 г 6-% оцту із 60-% оцтової есенції (кислоти). Задача 1. Дано:m (розч)1 = 50 гw1(реч) = 6 %w2(реч) = 60 %Знайтиm(реч) - ?Розв’язок𝑤реч=m(реч)m (розч)∗100%mреч1= 𝑤реч∗ m (розч)100%mреч1= 6%∗ 50 г100%mреч1 = 3гmрозч.= m реч.∗ 100%𝑤речmрозч.= 3 г∗ 100%60% mрозч.= 5 г m (води) = 45 г. Відповідь: mрозч.= 5 г 60% есенції, що необхідно взяти для приготування 50 г 6% оцту.
Математика. Задача 2. Скільки грамів 80%-вої оцтової есенції потрібно для виготовлення 300 г оцту з масовою часткою кислоти 9%. Задача 2. Дано:m (розч)1 = 300 гw1(реч) = 9 %w2(реч) = 80 %Знайтиm(реч) - ? Розв’язок𝑤реч=m(реч)m (розч)∗100%mреч1= 𝑤реч∗ m (розч)100%mреч1= 9%∗ 300 г100%mреч1 = 27 гmрозч.= m реч.∗ 100%𝑤речmрозч.= 27 г∗ 100%80% mрозч.=33,75 г Відповідь: mрозч.=33,75 г
Підсумки проекту. Застосовуючи знання з різних предметів (хімія, фізика, інформатика, географія, технології, біологія, медицина, історія, математика) учні навчилися самостійно здобувати знання, що є однією із ключових компетентностей НУШ; оволоділи новими знаннями про оцтову кислоту, та її особливості; комплексно формувати ключові компетенції – математична грамотність, спілкування державною мовою, компетентності в природничих науках та технологіях, екологічна грамотність і здорове життя, інформаційно-цифрова. Що визначають конкурентну спроможність на ринку праці: здатність і готовність до розв’язання комплексних задач.


про публікацію авторської розробки
Додати розробку