Урок на тему: "Метан.Гомологи метану"
Дана розробка уроку розрахована для 9 класу. Так як учні тільки починають вивчати органічну хімію, тому необхідно на перших уроках звернути увагу на будову молекули метану та номенклатуру гомологічного ряду метану (до десятого представника). У даній розробці поясненно будову метану із сучасної наукової точки зору і також закцентовано увагу на застосуванні метану і його продуктів (сажа, водень, хлорометан, тетрахлорометан). При поясненні чи при закріпленні матеріалу, що стосується номеклатури гомологів метану радив би скористатися "хімічним годинником", оскільки він гарно візуалізує матеріал. Вправи на осмислення орієнтовані на логічне та критичне мислення.
Конспект уроку на тему:
«Метан. Гомологи метану»
Розробив:
вчитель хімії Смілянської загальноосвітньої школи І-ІІІ ступенів №6,
Смілянської міської ради у Черкаській області
м. Сміла – 2018
Конспект уроку на тему:
«Метан. Гомологи метану»
Клас: 9
Дата:
Тема: «Метан. Гомологи метану»
Мета: а)навчальна: розширити знання про будову органічних сполук (зокрема метану); ознайомити учнів із гомологічним рядом метану; сформувати уявлення учнів про фізичні властивості метану його застосування та поширення у природі; навчитися записувати структурні формулу метану; навчитися складати формулу гомологічного ряду метану(до десятого представника) та давати їм назву (до десятого представника)
б)розвиваюча: розвити логічне мислення, вміти записувати формули гомологічного ряду метану, давати їм назви та записувати відповідні брутто-формули; працювати в парах; розвити вміння критичного мислення.
в)виховна: виховувати уважність, кмітливість, дисциплінованість, працьовитість, толерантність по відношенню один до одного.
Тип уроку: урок вивчення нового матеріалу та набуття нових вмінь.
Методи: бесіда, розповідь вчителя, інтерактивні вправи.
Реактиви та обладнання: Періодична система хімічних елементів Д. І. Менделєєва; таблиця гомологічного ряду метану, підручник.
Результати навчання: мати уявлення про фізичні властивості метану, давати назви гомологам метану та вміти записувати їх формули, розуміти принципи утворення назв гомологів метану; знати про походження та застосування метану.
План уроку
|
Поряд-ковий номер |
Етапи уроків |
Методи проведення |
Тривалість |
|
1 |
Організаційний момент |
Розповідь вчителя |
1 хв |
|
2 |
Актуалізація опорних знань |
Фронтальна бесіда |
6хв |
|
3 |
Постановка проблеми, мотивація навчальної діяльності |
Розповідь вчителя |
3 хв |
|
4 |
Вивчення нового матеріалу |
Розповідь з демонстраціями |
18 хв |
|
5 |
Осмислення знань |
Вправи, бесіда |
9 хв |
|
6 |
Узагальнення та систематизація знань |
Бесіда |
5 хв |
|
7 |
Домашнє завдання |
Розповідь |
3 хв |
ЗМІСТ УРОКУ
І.Організаційний момент
− Доброго дня, діти!
ІІ. Актуалізація опорних знань
Бліц-запитання. Відповідь так або ні.
- Запропонував назву «органічні речовини» (Й.-Я. Берцеліус)
- Яку речовину Веллер назвав як «життєва сила» (сечовина)
- Вітаїзм – це вчення вітаміни.
- Карбон в органічній хімії має валентність 3.
- У чому різниця між зв’язками: одинарним, подвійними та потрійним.
- У літературі органічну хімію називають «хімією Гідрогену».
- За якими спільними властивостями було об’єднано органічні речовини.
- Насичені органічні речовини, які мають одинарний зв'язок.
- Ненасичені органічні речовини, які мають подвійний та потрійний зв'язок
- Продовжіть речення. «Органічні речовини застосовують у галузях народного господарства:…..»
- Вкажіть спільні ознаки для органічних та неорганічних сполук.
ІІІ. Постановка проблеми, мотивація навчальної діяльності.
Органічні речовини мають важливе значення для людини. Їхня кількість щоденно збільшується і ми дуже часто їх використовуємо у повсякденному житті, навіть над цим не замислюючись. Існування людини у повсякденному житті без органічних сполук сьогодні дуже важко уявити. Почнемо вивчати її з найпростішої речовини як метан. Що такого особливо має метан? Яке значення він має житті людини? Звідки метан береться у природі? Сьогодні на уроці ми про це й дізнаємось.
ІV. Вивчення нового матеріалу
План
1. Будова молекули метану
2. Фізичні властивості, поширеність та застосування метану
3.Номенклатура алканів (гомологічного ряду до десятого представника)
- Метан як найпростіший представник алканів
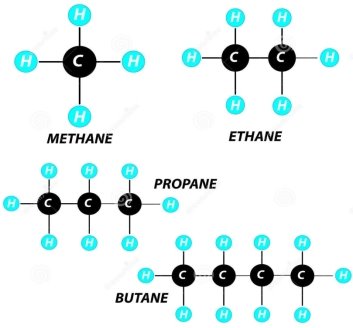
Найпростішими органічними речовинами є вуглеводні, які складаються лише з двох атомів Карбону і Гідрогену. Загальна формула алканів CnH2n+2. Найпершим представником є метан. Формула якого CH4. (пояснення ведеться за допомогою куле стрижневою моделюю, складеною з пластиліну) [1].
Перед цим потрібно згадати будову електронну будову Карбону (див. рис.1)
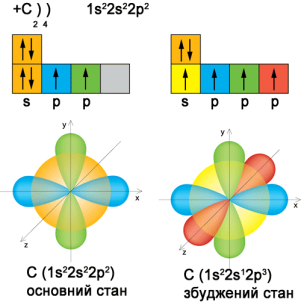
Рис. 1. Електронна будова Карбону [2]
Отже, Карбон у збудженому стані має вільні 4 електрони, які знаходяться на одній s орбіталі та трьоx р.
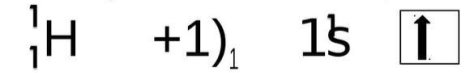
Внаслідок перекриття s-s (Одна s-орбіталь Карбону та Одна s-орбіталь Гідрогену) та p-p прикривань (Три p-орбіталi Карбону та Три p-орбіталi Гідрогену), які у свою чергу утворюють 4 σ-звязки C−H.
Структурна формула метану (див. рис. 2)
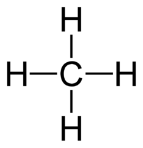
Рис.2. Структурна формула метану
Пригадаємо, які за будовою зв’язки C−H.
- Ковалентні зв’язки.
Молекула має sp3 гібридизацію4 ковалентних зв’язки C−H (σ-звязки), напрямлених до вершини тетраедра < 109°5`.Молекула має форму правильної тригональної піраміди (тетраедра) (див. рис. 2 та рис. 3).
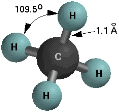
Рис. 3. Кулестрежнева будова метану [3]
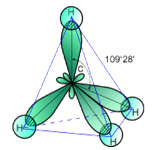
Рис. 3. Просторовий вигляд молекули метану [4]
2.Фізичні властивості, поширеність та застосування метану
- Фізичні властивості метану:
- Безбарвний газ
- Без запаху
- Удвічі легший за повітря (підтвердимо за допомогою розрахунків)
- У воді не розчиняється, а розчиняється у органічних розчинниках
У природі утворюється внаслідок гниття рослин без доступу повітря. Багато міститься у болотному газі, вугільних шахтах.
Запаси у Україні метану у вигляді природного газу становлять 1,5 трлн м3 [1]
Застосування:як дешеве паливо та в органічному синтезі
Використовуються продукти перетворення метану:
- Сажа – виготовлення гуми, друкарських фарб
- Водень –виготовлення амоніаку
- Хлорометан –у медицині як знеболюючий засіб
- Тетрахлорометан – засіб гасіння вогню
Вважається парниковим газом, який міститься в атмосфері.
3.Номенклатура алканів (гомологічного ряду до десятого представника)
Номенклатура утворюється за наступною схемою
Префікс + суфік «ан» = назва алкану (див. табл. 1.)
Таблиця 1.
Номеклатура алканів (гомологічного ряду до десятого представника)
|
Число атомів Карбону |
Префікс |
+ |
Суфікс |
Формула |
Назва алкану |
|
1 |
мет |
+ |
ан |
CH4 |
метан |
|
2 |
ет |
+ |
ан |
C2H6 |
етан |
|
3 |
проп |
+ |
ан |
C3H8 |
пропан |
|
4 |
бут |
+ |
ан |
C4H10 |
бутан |
|
5 |
пент |
+ |
ан |
C5H12 |
пентан |
|
6 |
гекс |
+ |
ан |
C6H14 |
гексан |
|
7 |
гепт |
+ |
ан |
C7H16 |
гептан |
|
8 |
окт |
+ |
ан |
C8H18 |
октан |
|
9 |
нон |
+ |
ан |
C9H20 |
нонан |
|
10 |
дек |
+ |
ан |
C9H22 |
декан |
NB!Формула утворюється дуже просто:
У загальну формулу алканів CnH2n+2 підставляють число атомів Карбону (n). Наприклад:
n=1, C1H2∙1+2↔ C1H4 ↔ CH4
n=2, C2H2∙2+2↔ C2H6 ↔
І даний ряд у органічній хімії називають гомологічними рядом метану. Всі ці сполуки об’єднує те, що вони мають однакові хімічні властивості. Фізичні ж властивості мають різні. Не здається Вам, що це якась прогресія? Так, прогресія. На що відрізняється кожний попередній представник?
C2H6 – CH4 = –СH2–
–СH2– називають гомологічною різницею.
V. Осмислення знань
1.За допомогою спеціального хімічного годинника. Назвіть гомологічний ряд метану

Рис. 5. Хімічний органічний годинник[5]
2.Знайдіть у таблиці представників 10 гомологічного ряду метану у таній таблиці (роздатковий матеріал або проектування за домолотою проектора)
Таблиця
|
м |
к |
н |
о |
п |
р |
с |
т |
л |
н |
|
н |
м |
е |
т |
а |
н |
д |
в |
а |
д |
|
т |
й |
б |
у |
н |
п |
р |
о |
п |
|
|
я |
а |
н |
т |
а |
н |
н |
н |
а |
н |
|
п |
н |
а |
р |
і |
и |
н |
а |
ц |
й |
|
й |
е |
т |
з |
г |
н |
к |
т |
ш |
д |
|
о |
к |
т |
к |
е |
б |
о |
б |
|
щ |
|
к |
а |
н |
п |
к |
н |
о |
н |
р |
п |
|
е |
г |
е |
р |
с |
г |
н |
а |
о |
б |
|
д |
у |
п |
н |
а |
е |
н |
а |
п |
з |
|
г |
б |
т |
а |
н |
б |
м |
е |
т |
ф |
Матриця з правильними відповідями
|
|
|
|
|
|
|
|
|
|
|
|
|
м |
е |
т |
а |
н |
|
|
|
|
|
|
|
б |
у |
|
п |
р |
о |
п |
|
|
|
|
н |
т |
а |
н |
|
н |
а |
н |
|
|
|
а |
|
|
|
|
а |
|
|
|
|
е |
т |
|
г |
|
к |
т |
|
|
|
|
|
|
|
е |
|
о |
|
|
|
|
к |
а |
н |
|
к |
н |
о |
н |
р |
п |
|
е |
г |
е |
|
с |
|
н |
а |
о |
|
|
д |
|
п |
н |
а |
|
н |
а |
п |
|
|
|
|
т |
а |
н |
|
|
|
|
|
3.Утворіть правильні слова
натем, утбан, натко, теан, ропна, етнгпае, олмгоог
4. «Біла ворона».Знайдіть у ряді зайве слово та поясніть чому
а) метан, етан, пропан, бутан, лактан
б) етен, етан, етин
в) октан, манган, метан
г) пропан, бутан, октан
д) меркаптан, метан, октан,
е) метан, етан, пропан… це
5. Знайдіть зайву формулу та яка не відносить до гомологічного ряду метану
- CH4, C2H6, С3H7, C4H10
- C6H14, C8H18, C10H22, C11H23
VI.Узагальнення та систематизація знань
Отже, метан належить до насичених вуглеводнів (які ще називають алкани (загальна формула яких СnH2n+2) або парафіни), мають гібридизацію sp3. За фізичними метан: безбарвний газ, нерозчинний у воді, розчинний в органічних розчинниках, легший за повітря. Метан належить до парникових газів та утворює гомологічний ряд начичених вуглеводнів.
VII. Домашнє завдання.
- Прочитати[1] ст. 138-146
- Вивчити гомологічний ряд метану
- Письмово виконати[1] ст. 142 № 267, ст. 146 № 277,278
CПИСОК ВИКОРИСТАНИХ ДЖЕРЕЛ
1.Григорович О. В. Хімія 7 клас: для загальноосвітніх навчальних закладів / О. В. Григорович. − Х. :Видавництво “Ранок”, 2015. − С. 138-146.
2. Особливості будови атома Карбону [Електронний ресурс] / Режим доступу: http://www.chemistry.in.ua/wp-content/uploads/structure-carbon-atoms-300x300.png
3. Метан [Електронний ресурс] / Режим доступу: https://xreferat.com/image/108/1307224836_1.png
4. Метан[Електронний ресурс] / Режим доступу: http://ru.solverbook.com/my_images/pic3764.png
5.:Життя і хімія [Електронний ресурс] / Режим доступу: https://scontent.fiev15-1.fna.fbcdn.net/v/t1.0-9/32235725_1682041018548088_4778916716195348480_n.jpg?_nc_cat=0&oh=1e1d89d7a5310a370769df9a60614193&oe=5BB695B3


про публікацію авторської розробки
Додати розробку
