Урок "Практична робота № 2. Розв’язування експериментальних задач"
Тема уроку. Практична робота № 2. Розв’язування експериментальних задач
Мета уроку:
Освітня: удосконалити й закріпити вміння учнів експериментально встановлювати якісний склад речовин; вдосконалювати навички складання реакцій йонного обміну між розчинами електролітів, вміння записувати реакції в молекулярній, повній та скороченій йонній формах, перевірити вміння застосовувати отриманні знання для розв’язування практичних завдань по одержанню й розпізнаванню речовин; вдосконалювати техніку проведення хімічного експерименту;
Розвиваюча: розвивати вміння спостерігати і порівнювати, досліджувати умови протікання реакцій йонного обміну до кінця, порівнювати результати дослідів і робити висновки, встановлювати причинно-наслідкові зв’язки; розвивати довільну увагу; коригувати самоконтроль під час складання рівнянь електролітичної дисоціації речовин, рівнянь реакцій йонногообміну; розвивати в учнів позитивних мотивів навчально- пізнавальної діяльності, інтересів, творчої активності;
Виховна: розвивати в учнів мислення, вміння робити логічні висновки, спираючись на знання хімії, біології, фізики, безпеки життєдіяльності, акуратності, уважності, самооцінки і самоконтролю, уміння працювати в колективі, виховувати самостійність і працьовитість, вміння працювати в групі.
Тип уроку: практична робота
Методи: репродуктивний, частково-пошуковий, дослідницький, пояснювально-ілюстративний, експериментальна задача. словесні, практичні (лабораторний дослід), інтерактивні, використання ІКТ.
Міжпредметні зв'язки: біологія, інформатика, математика, фізика
Девіз уроку: « Хімії навчитися неможливо, якщо не бачити самої практики і
не братися за хімічні операції»
М.В.Ломоносов
Хід уроку
І. Організаційний момент.
ІІ Мотивація навчальної діяльності (слайд № 1)
Великий російський учений-натураліст, геохімік, поет, перший російський академічно освічений вчений, видатний природодослідник Михайло Ломоносов у свій час висловив думку про те, що « Хімії навчитися неможливо, якщо не бачити самої практики і не братися за хімічні операції», вона актуальна і сьогодні. Чому? (висловлювання дітей). Дійсно, ми знаємо, що хімія – наука експериментальна і потрібно не тільки вчитися, а й використовувати свої знання на практиці і сьогодні виконуючи практичну роботу ми ще раз підтверджуємо це.
ІІІ. Оголошення теми уроку, формування мети (слайд № 2-3)
Тема уроку. Практична робота № 2. Розв’язування експериментальних задач. Яка мета нашого уроку? (формування мети разом з учнями:
- удосконалити й закріпити вміння учнів експериментально встановлювати якісний склад речовин;
- вдосконалювати навички складання реакцій йонного обміну між розчинами електролітів,
- вміння записувати реакції в молекулярній, повній та скороченій йонній формах,
- навички прогнозувати можливості перебігу реакцій йонного обміну між двома електролітами;
- вдосконалювати техніку проведення хімічного експерименту)
Очікувані результати:
- розв’язування експериментальних задач на здійснення перетворень між електролітами у водних розчинах за скороченими йонно-молекулярними рівняннями, на визначення йонів у водному розчині за допомогою якісних реакцій
ІV. Актуалізація опорних знань (слайд № 4)
-
Бесіда за питаннями: «Мозковий штурм»
- які реакції називаються реакціями йонного обміну?
- назвіть ознаки проходження реакцій йонного обміну до кінця.
- які реакції називають якісними?
2. «Дешифрувальник» Після введення у комп’ютер результатів лабораторних досліджень загубилися деякі формули речовин. Допоможіть визначити варіанти, якщо частина інформації збереглася.
А) 2KOH + (H2 SO4 ) = K2 SO4 + (2H2O)
Б) (BaCl2) + 2AgNO3 = Ва(NO3)2 + (2AgCl) ↓
В) Na2CO3 + (2HCl) = 2NaCl + (CO2) ↑+ H2O
Г) ВаCl2 + (Na2SO4) = Вa SO4↓ +2NaCl
3. Виконання тестових завдань с. 12 практичного зошита.
V. Виконання практичної роботи (слайд 6)
1. Нагадаємо правила з безпеки життєдіяльності.
Інструкція з безпеки життєдіяльності
*Забороняється пробувати речовини на смак;
* брати речовини руками;
* залишати відкритими склянки з речовинами;
* виливати залишки реактивів в склянки, з яких вони були взяті;
* залишати неприбраними розлиті реактиви;
* обмінювати місцями пробки та піпетки з різних банок.
*працювати тільки над столом;
* обережно поводитись с кислотами, лугами;
* змити реактив водою, а потім обробити поверхню нейтралізуючою речовиною, якщо реактив потрапив на шкіру або одяг;
* збирати залишки реактивів в спеціально призначений посуд;
* після роботи обов′язково вимити руки, прибрати робоче місце
2. Виконання практичної роботи № 2 с. 12 (слайд 7)
VІ. Підведення підсумків. Рефлексія прийом «Одним словом» (слайд 8)
VІІ. Домашнє завдання: опрацювати § 17
Додаткові завдання :
- Доведіть, що яєчну шкаралупу доцільно використовувати на кислих ґрунтах присадибної ділянки для зменшення кислотності. Відповідь поясніть. Підтвердьте рівняннями реакцій.
- Розв’яжіть кросворд:
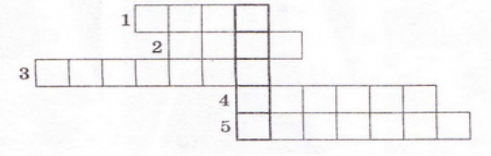
По горизонталі:
- Найпоширеніший дуже слабкий електроліт.(вода)
- Клас неорганічних сполук, здебільшого сильні електроліти. (солі)
- Кількісна характеристика дисоціації електролітів. (ступінь)
4. Кислотний залишок слабкої галогеноводневої кислоти. (фтори)
5. Слабка кислота із жарознижувальним ефектом. (аспірин)
Ключове слово по вертикалі - назва літери - позначення ступеня дисоціації


про публікацію авторської розробки
Додати розробку
