Узагальнення знань з теми "Електролітична дисоціація"
Сотула Оксана Леонідівна, вчитель хімії
КЗ «Бугаївський ліцейІзюмської районної ради Харківської області»
Тема. «Електроліти. Електролітична дисоціація. Реакції йонного обміну між розчинами електролітів»
Мета уроку: узагальнити і систематизувати знання учнів з теми: «Електролітична дисоціація. Реакції йонного обміну між розчинами електролітів».
Очікувані результати навчально-пізнавальної діяльності:
На кінець уроку повинні:
- узагальнити і систематизувати знання з вивченої теми;
- закріпити вміння визначати катіони та аніони в розчинах електролітів, складати молекулярні, йонні (повні та скорочені) рівняння;
- вміти обґрунтувати перебіг реакцій між електролітами у водних розчинах;
- висловлювати судження про значення електролітів та процесу електролітичної дисоціації у природі та житті людини;
- використовувати хімічні знання для пояснення користі і шкоди здобутків хімії і хімічної технології для людини і довкілля;
Ключові компетентності: спілкування державою мовою, основні компетентності у природничих науках і технологіях, інформаційно-цифрова компетентність, ініціативність і підприємливість, екологічна грамотність і здорове життя,
Тип уроку: узагальнення знань, умінь, навичок.
Наочність: таблиці «Розчинність кислот, основ і солей у воді», «Дія індикаторів на розчини кислот, основ».
Роздатковий матеріал: «Анаграма», «Асоціативне гранування», «Слідство ведуть хіміки», «Онлайн-тестування», «Фішбоун» «Листок оцінювання».
Методи та прийоми: словесні: еврістична бесіда, розповідь, наочні: комп’ютерна демонстрація; практичні: розв'язування вправ, робота з онлайн-сервісами (тестування), інтерактивні, елементи STEAM освіти.
Наскрізні змістові лінії:
Здоров’я і безпека (поняття «електроліти й неелектроліти»).
Екологічна безпека і сталий розвиток (застосування якісних реакцій).
Підприємливість і фінансова грамотність (поняття «Розчинність речовин», електроліти й неелектроліти).
Міжпредметні зв’язки: фізика, екологія,природознавство.
Хід уроку.
І. Організаційний момент
Добрий день, сьогодні я з вами буду подорожувати безмежними просторами надзвичайної науки – хімії. Пропоную розпочати наш урок з щирої посмішки, подаруйте її одне одному, а я бажаю кожному із вас, щоб на цьому уроці ви були...
Слайд 1
"У" - УВАЖНИМИ;
"С" - СПОКІЙНИМИ;
"П" - ПРАЦЕЛЮБНИМИ;
"І" - ІТЕЛЕКТУАЛЬНИМИ;
"Х" - ХІМІКАМИ
Тож бажаю вам УСПІХУ в процесі пізнання!
Дуже важливо, щоб ми з вами встановили зворотній зв'язок, давайте зробимо так: я плесну в долоні, ви спробуєте повторити але всі разом, синхронно.
Отже пропоную розгадати анаграму….
Слайд 2
і и я ц с ц а о д і (дисоціація)
ІІ. Оголошення теми і постановка завдань
Тема уроку «узагальнення і систематизація знань з теми: «Електролітична дисоціація. Реакції йонного обміну між розчинами електролітів»
Слайд 3 (число класна робота)
- Тож що будемо робити на сьогоднішньому уроці?
На сьогоднішньому уроці ми маємо узагальнити, систематизувати та поглибити знання про ЕД, закріпити вміння складати, молекулярні, повні та скорочені йонні рівняння, а також спробуємо застосувати знання в нестандартних ситуаціях, бо як сказав великий Гете:
Слайд 4
«Просто знати – це ще не все, знання потрібно вміти використовувати».
ІІ. Мотивація навчальної діяльності.
Проблемне питання
Сьогодні активно розвивається наука і техніка. Значно зросли обсяги хімічних виробництв. Людство зіткнулося зі збільшенням кількості і небезпечності відходів, кислотними дощами, забрудненням водойм.
Слайд 5
Як можна подолати проблеми потрапляння деяких небезпечних йонів у навколишнє середовище?
А для того щоб дати відповідь на це питання, пригадаймо де ж беруться ці йони?
(утворюються під час електролітичної дисоціації)
ІІІ. Застосування вмінь, відпрацювання навичок.
1. «Асоціативне гронування».
Свою винахідливість ви можете проявити, виконуючи вправу «Асоціативне гронування». На зеленому листочку винограду – зазначене поняття «електролітична дисоціація». На виноградинках необхідно записати слова або словосполучення з поняттями цієї теми «Електролітична дисоціація. Реакції йонного обміну між розчинами електролітів».
Слова : йони, слабкі електроліти, сильні електроліти, катіони, аніони, перебіг реакцій до кінця, осад, ступінь електролітичної дисоціації, йонні реакції.
А що означають всі ці поняття? Спробуймо пригадати зігравши у гру «Вірю не вірю»
Слайд 6
2. Вправа «Вірю не вірю»
- Процес розпаду речовини під дією струму називається електролітичною дисоціацією; (вірю)
- Сполуки, водні розчини, або розплави яких не проводять електричний струм називають неелектролітами; (вірю)
- Сполуки, водні розчини, або розплави яких проводять електричний струм називають електролітами; (вірю)
- До електролітів відносяться всі класи неорганічних речовин; ( не вірю )
- Позитивно заряджені йони називають катіонами; (вірю)
- Негативно заряджені йони називають аніонами; (вірю)
- Електроліти, які дисоціюють у водних розчинах на йони Гідрогену і кислотний залишок називаються солями; ( не вірю )
- Електроліти, які дисоціюють у водних розчинах на катіони металу та аніони кислотного залишку називають основами; ( не вірю )
- Електроліти, які дисоціюють у водних розчинах на катіон металу та гідроксид іон називаються основами; (вірю)
- Індикатори – це речовини, які пришвидшують хімічну реакцію. ( не вірю)
Отже
Слайд 7
Слайд 8
3. Випишіть формули електролітів
Ми з вами згадали що таке електроліти і неелектроліти. За 1 хвилини кожен повинен виписати формули електролітів.
NaOH, СО2, НNO3, ВаСІ2, К2SO4 Н2, С12Н22О11, Аl2(SO4)3
Що ж насправді відбувається при взаємодії між електролітами в розчині?
4. Написати рівняння реакції у молекулярній та йонній (повній та скороченій) формах
CuSO4 + 2KOH→ Cu(OH)2 ↓+ K2SO4
Cu + SO4 + 2K + 2OH→ Cu (OH)2 ↓+ 2K + SO4
Cu + OH→ Cu (OH)2 ↓
5. Вправа «Кулак ребро долоня» (1 хв.) вправа з застосуванням методики природовідповідності.
Чи хотіли б ви побувати в ролі слідчого і розкриту таємничу справу. Тож пропоную вправу «Слідство ведуть хіміки»
6. «Слідство ведуть хіміки». Розв’язування ситуаційних задач. Робота в групах - рух по колу
1.Кожна група, ви головна,отримуєте справу – ситуацію.
2. Над отриманою ситуацією головна група працює приблизно 3 хвилини, маркером відповідного кольору зазначаєте розв’язок .
2. Далі свою ситуацію передаєте на експертну перевірку іншим групам за годинниковою стрілкою. Експертні група протягом 1 хвилини аналізують розв’язок, корегують якщо потрібно і за сигналом передають далі.
3. Як тільки ваші ситуації повернулися до вас за одну хвилину перегляньте її і підготуйтеся до відповіді.
Роздатковий матеріал - додаток 1 або додаток 2 (на вибір)
Слайд 9
Ситуація 1.
Ви увійшли до кабінету хімії і побачили, що на столі – краплі якоїсь рідини. Відомо, що попередній клас працював з розчинами кислот і лугів. Як визначити, яка речовина розлита на столі, якщо у вашому розпорядженні лише універсальний індикаторний папір? Запишіть рівняння дисоціації цих речовин і вказати дію індикатору на розчини кислот і лугів.)
Слайд 10
Ситуація 2.
Ви маєте розкрити «мокру справу», що відбулась у розчині. Злочинці з іменами Барій Хлорид і Натрій Сульфат, які працювали парами, заперечують свою причетність до «мокрої справи», стверджуючи, що у них є алібі. Свої докази підтвердіть йонними рівняннями.
(Учням повинні написати рівняння в молекулярному та йонному вигляді.)
Слайд 11
Ситуація 3.
Ви - головний еколог на хімічному підприємстві. Вас хвилює проблема, як запобігти забрудненню навколишнього середовища. Для очищення води від катіонів важких і токсичних металів: Pb2+, Cr3+необхідно перевести в осад. Від швидкості прийняття вами рішення залежить доля міста. Скориставшись таблицею
Отже На початку уроку ми поставили запитання.
Слайд 12
«Від теорії до практики».
Ситуація 4.
Сьогодні активно розвивалася наука і техніка. Значно зросли обсяги хімічних виробництв. Людство зіткнулося зі збільшенням кількості і небезпечності відходів, кислотними дощами. Як можна подолати ці екологічні проблеми?
Слайд 13
Механізми дії цих проблем:
- Розчинення відходів у воді та утворення розчинів електролітів
- Взаємодія розчинів один з одним та з об’єктами навколишнього середовища (кислотні дощі, ерозія ґрунту, забруднення рослин, зниження імунітету, вживання забрудненої їжі та води, знищення природного середовища існування організмів)
- Вдихання відходів та утворення в організмі отруйних речовин
Можливі шляхи вирішення проблем:
- встановлення якісних очисних споруд,
- заборона використання небезпечних продуктів хімічного синтезу,
- комплексне використання сировини,
- вторинна переробка ресурсів,
- знешкодження небезпечних відходів,
- грамотне використання засобів побутової хімії, мінеральних добрив, засобів захисту рослин,
- дотримання здорового способу життя,
- розробка альтернативних видів палива, використання сонячної енергії.
Слайд 14
І на завершення я пропоную вам пройти індивідуальне онлайн-тестування, щоб кожному з вас зрозуміти наскільки якісно була опрацьована дана тема.
7. Онлайн-тестування Освітній портал «На урок»
https://naurok.com.ua/test/elektrolitichna-disociaciya-reakci-yonnogo-obminu-18724.html
IV. Підведення підсумків.
Слайд 15
Метод «фішбоун» (додаток 3)
- Проблема;
- Причини;
- Факти;
- Виснов.ок
![]()
![]()
![]()
![]()
Рефлексія
На стінах класу ви можете побачити вислови відомих людей ( прочитати їх ), дати можливість учням обрати той вислів, який найкраще відображає їхню діяльність на уроці.
Сократ « Я знаю, що я нічого не знаю»
Конфуцій «Я не народився зі знаннями»
Т.Г. Шевченко «Учитеся брати мої, думайте читайте»
Овідій (поет римської імперії) «Я зробив усе, що міг; хай хтось зможе, зробить краще».
Слайд 16
V. Домашнє завдання
Слайд 15
- повторити § 9 у підручнику онлайн-домашнє завдання (освітній портал «На урок»)
Оцінювання
|
Бланк оцінювання активності на уроці
ПІ ____________________ дата ______________
|
|
Бланк оцінювання активності на уроці
ПІ ____________________ дата ______________
|
|
Бланк оцінювання активності на уроці
ПІ ____________________ дата ______________
|
|
Бланк оцінювання активності на уроці
ПІ ____________________ дата ______________
|
|
Бланк оцінювання активності на уроці
ПІ ____________________ дата ______________
|
|
Бланк оцінювання активності на уроці
ПІ ____________________ дата ______________
|
|
Бланк оцінювання активності на уроці
ПІ ____________________ дата ______________
|
Онлайн тестування
Приступаємо до виконання тестових завдань. Зверніть увагу, що у питаннях тестів може бути кілька правильних відповідей. Не забувайте користуватися таблицею розчинності лугів, солей, кислот. На виконання тестових завдань відводиться 7 хвилин.
Тестові завдання
- Чи засвітиться лампочка приладу, якщо його електроди занурити у склянку із дистильованою водою?
а) так б) ні
2. Які з речовин належать до сильних електролітів?
а) сульфатна кислота б) карбонатна кислота
в) калій гідроксид г) магній (ІІ) гідроксид
3.Які з вказаних речовин належать до слабких електролітів?
а) бромідна кислота б) силікатна кислота
в) натрій гідроксид г) купрум (ІІ) гідроксид
4. Розчини яких солей під час дисоціації будуть утворювати бромід – йони?
а) KBr; б) CaBr2 ; в) PbBr2 ; г) NaBr.
5. За яких умов реакції йонного обміну йтимуть до кінця. Коли в результаті реакції утворилися:
а) розчинні речовини; б) осад;
в) газ; г) вода.
6. Між розчинами яких речовин можлива реакція?
а) K2 SO4і H2 SO4 ; б)Na2 SO4 і HCl; в)Al2 (SO4 )3і Ba (NO3 )2;г) K2SiO3і HNO3.
8. У результаті взаємодії яких речовин утвориться осад?
а)AgNO3 і Na3PO4 ; б)CuSO4 і NaOH; в)H2SO4 і Ba(NO3) ; г) KOH і HCl.
 « Я знаю, що я нічого не знаю»
« Я знаю, що я нічого не знаю»
Сократ

«Я не народився зі знаннями»
Конфуцій
«Учитеся брати мої, думайте, читайте»

Т.Г. Шевченко
 « Зробив усе, що міг; хай хтось зможе, зробить краще».
« Зробив усе, що міг; хай хтось зможе, зробить краще».
Публій Овідій Назон
«Слідство ведуть хіміки
Додаток 1
Ситуація 1.
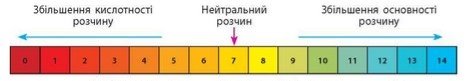
Ви увійшли до кабінету хімії і побачили, що на столі – краплі якоїсь рідини. Відомо, що попередній клас працював з розчинами кислот і лугів. Як визначити, яка речовина розлита на столі, якщо у вашому розпорядженні лише універсальний індикаторний папір?
(Ви повинні написати рівняння дисоціації цих речовин і вказати колір індикатору при дії розчинів кислот і лугів, користуючись шкалою)
Розв’язок:
Ситуація 2.
Ви маєте розкрити «мокру справу», що відбулась у розчині. Злочинці з іменами Барій Хлорид і Натрій Сульфат, які працювали парами, заперечують свою причетність до «мокрої справи», стверджуючи, що у них є алібі. Свої докази підтвердіть йонними рівняннями.
(Ви повинні написати рівняння в молекулярному та йонному (повному, скороченому) вигляді.
Розв’язок:
Ситуація 4.
Сьогодні активно розвивалася наука і техніка. Значно зросли обсяги хімічних виробництв. Людство зіткнулося зі збільшенням кількості і небезпечності відходів, кислотними дощами, забрудненням водойм. Як можна подолати ці екологічні проблеми ?
Запропонуйте способи:
Ситуація 3.
Ви - головний еколог на хімічному підприємстві. Вас хвилює проблема, як запобігти забрудненню навколишнього середовища. Для очищення води від катіонів важких і токсичних металів: Pb2+, Cr3+ необхідно перевести в осад. Від швидкості прийняття вами рішення залежить доля міста. Скориставшись таблицею розчинності, з'ясуйте, у вигляді яких солей можна осадити ці йони. Підтвердіть свої пропозиції молекулярними рівняннями реакцій.
Розв’язок:
Додаток 2
|
|
|
|
|
|
|
|
|
|
|
|
Додаток 3
|
|
|
|
|
|

4




про публікацію авторської розробки
Додати розробку