Урок "Ступінь окиснення. Визначення ступеня окиснення елемента за хімічною формулою сполуки. Складання формули сполуки за відомими ступенями окиснення елементів."
Хімія 9 клас
Урок №25
Тема: Ступінь окиснення. Визначення ступеня окиснення елемента за хімічною формулою сполуки. Складання формули сполуки за відомими ступенями окиснення елементів.
Мета:
- ввести поняття ступеня окиснення; поглибити поняття валентності; виробити навички розрахунку ступеня окиснення в складних речовинах; виявити подібність і відмінність валентності та ступеня окиснення; сформувати вміння складання хімічних формул за відомим значенням ступенів окиснення елементів;
- розвивати логічне мислення та усне мовлення, вміння поєднувати теорію з практикою;
- виховувати любов до предмету.
Обладнання: Періодична система хімічних елементів Д. І. Менделєєва, таблиця електронегативностей хімічних елементів, роздатковий матеріал.
Тип уроку: засвоєння нових знань.
ХІД УРОКУ
I. ОРГАНІЗАЦІЙНИЙ ЕТАП
II. АКТУАЛІЗАЦІЯ ОПОРНИХ ЗНАНЬ І ПЕРЕВІРКА ДОМАШНЬОГО ЗАВДАННЯ
1. Інтерактивний метод «Мозковий штурм»
Відповісти на запитання:
1) Що таке реакція обміну?
2) Написати приклад реакції обміну?
3) Що таке реакція сполучення?
4) Написати приклад реакції сполучення?
5) Що таке реакція розкладу ?
6) Написати приклад реакції розкладу?
7) Що таке реакція заміщення?
8) Написати приклад реакції заміщення?
2. Перевірка домашнього завдання ( Вправа 98)
IIІ. МОТИВАЦІЯ НАВЧАЛЬНОЇ ДІЯЛЬНОСТІ
У йонних сполуках немає спільних пар електронів, тому для цих речовин поняття про валентність не можна використовувати. Для всіх сполук, незалежно від виду хімічних зв’язків, застосовується більш універсальне поняття — ступінь окиснення.
IV. ВИВЧЕННЯ НОВОГО МАТЕРІАЛУ
1. ДАЄМО ПОНЯТТЯ «СТУПІНЬ ОКИСНЕННЯ».
Ступінь окиснення елемента — це умовний заряд атома в речовині, обчислений із припущенням, що вона складається з йонів. Ступінь окиснення характеризує число умовно прийнятих або умовно відданих електронів. Ступінь окиснення може бути позитивним (якщо атом віддав електрони), негативним (якщо атом прийняв електрони) або дорівнювати нулю. Він позначається арабською цифрою зі знаком «плюс» або «мінус» над символом елемента.
2. ПРАВИЛА ВИЗНАЧЕННЯ СТУПЕНЯ ОКИСНЕННЯ.
- Ступінь окиснення атомів в простій речовині дорівнює нулю.
- Атомам деяких хімічних елементів звичайно приписують сталі ступені окиснення. Наприклад, ступінь окиснення Флуору в сполуках завжди дорівнює –1; елементи І, ІІ, ІІІ групи головної підгрупи мають с.о що дорівнює № групи із знаком +.
- Ступінь окиснення Гідрогену в більшості сполук +1, і лише в сполуках з металами він дорівнює –1.
-
Ступінь окиснення Оксигену в більшості сполук –2, і лише в деяких сполуках йому приписують ступінь окиснення –1(
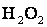 ,
, 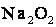 ) або +2 (
) або +2 (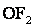 ).
).
- Ступінь окиснення атома металлу побічної підгрупи в сполуках позитивний і чисельно дорівнює його валентності.
- Сума ступенів окиснення всіх атомів у сполуці дорівнює нулю.
- Атоми багатьох хімічних елементів виявляють змінні ступені окиснення.
- Сума ступенів окиснення атомів у складних іонах дорівнює заряду іона.
Користуючись наведеними правилами, визначимо ступені окиснення хімічних елементів у сполуках:
![]()
H2, LiCl, AgNO3, KH, HNO3, O2, Mg, Al2S3, Al, BaH2, Zn(NO3),
Завдання 1. Учні по ланцюжку біля дошки розраховують ступінь окиснення атомів у записаних на дошці формулах речовин:
Cu2O, CO2, CO, HCl, AlI3, SO2, BaCl2, FeSO4, Na2CO3, H2SO4, Al2(SO4)3, Ca3(PO4)2.
3. СКЛАДАННЯ ФОРМУЛИ СПОЛУКИ ЗА ВІДОМИМИ СТУПЕНЯМИ ОКИСНЕННЯ ЕЛЕМЕНТІВ.
В сучасній хімічній науці поняття ступінь окиснення дедалі ширше використовується як універсальна й однозначна величина, хоча для речовин молекулярної й атомної будови вона має умовний характер. Пам’ятаючи правило електронейтральності, а саме що сума ступенів окиснення всіх атомів у кожній речовині дорівнює нулю, видається, його можна використовувати при складанні формул різних сполук.
Розглянемо приклад складання формули сполуки Кальцію з Фосфором.
Розв’язання:
Кальцій – металічний елемент, оскільки він являється елементом головної підгрупи ІІ групи періодичної системи хімічних елементів то має ступінь окиснення +2. Фосфор – неметалічний елемент, він належить до головної підгрупи V групи. У сполуці з металічним елементом Фосфор виявляє негативний ступінь окиснення, який становить 5 – 8 = -3. Записуємо формулу сполуки з невідомими індексами і вказуємо ступені окиснення елементів: СаxРy
Далі діємо так, як при складанні формули бінарної сполуки за валентностями елементів. Знаходимо найменше число, яке ділиться без залишку на значення ступенів окиснення елементів; це число 6. Поділивши його на 2, отримуємо кількість атомів Кальцію у формулі сполуки (6 : 2 = 3), а поділивши на 3, отримуємо кількість атомів Фосфору (6: 3 = 2). Формула сполуки – Са3Р2.
У бінарних сполуках хімічний елемент, що стоїть у цьому ряду лівіше, виявляє негативний ступінь окиснення, а той, що стоїть правіше, — позитивний. Так, у сполуці MgO хімічний елемент Магній мас позитивний ступінь окиснення +2, а Оксиген — негативний ступінь окиснення -2.
Позитивні значення ступенів окиснення мають ті атоми, які віддали свої електрони іншим атомам (зв'язувальна електронна хмара зміщена від них). Наприклад, атоми металів.
Негативні значення ступенів окиснення мають ті атоми, які приєднали електрони від інших атомів (зв'язувальна електронна хмара зміщена до них).
Повторюємо на декількох прикладах порядок складання формул.
Наприклад: скласти формули кальцій нітриду, алюміній сульфіду, натрій фосфіду.
Кальцій нітрид Кальцій - у другій групі - ступінь окиснення +2
Нітроген більш електронегативний, знаходиться у V групі, його ступінь окиснення розраховується 8 - № групи = -3
+2 -3 Cпільне кратне = 6
Сa3 N2
Отже, індекси у формулі будуть відповідно 3 і 2.
Алюміній сульфід Алюміній – у третій групі = +3
Сульфур – 8 - № групи 6 = - 2
+3 -2
Al2S3
Виконання тренувальних вправ
1. Складіть формули:
а) трьох сполук Оксигену з Манганом, у яких Манган проявляє ступені окиснення +2, +4, +7.
б) трьох сполук Нітрогену з Оксигеном, де Нітроген проявляє ступені окиснення +2,+4, +5.
V. УЗАГАЛЬНЕННЯ ТА СИСТЕМАТИЗАЦІЯ ЗНАНЬ
Прийом «Хрестики-нулики»
I команда: Обрати лінію, яка сполучає формули сполук, що мають ступінь окиснення+1.
|
SO2 |
BaO |
H2O |
|
Na2O |
CO2 |
K2O |
|
Fe2O3 |
Al2O3 |
Cu2O |
ІІ команда: Шляхом до виграшу є оксиди з ступенем окиснення елемента +4.
|
SO2 |
BaO |
CuO |
|
N2O |
SiO2 |
H2O |
|
PbO2 |
V2O5 |
CO2 |
IІІ команда: Обрати лінію, яка сполучає формули сполук, що мають ступінь окиснення+3.
|
SO2 |
BaO |
H2O |
|
Na2O |
CO2 |
K2O |
|
Fe2O3 |
Al2O3 |
Cr2O3 |
ІV команда: Шляхом до виграшу є оксиди з ступенем окиснення елемента +2.
|
SO2 |
BaO |
CuO |
|
N2O |
CaO |
H2O |
|
PbO2 |
MgO |
CO2 |
Прийом «Логічні квадрати»
Знайдіть у логічних квадратах місце таким речовинам: CaO, CO2, H2O, N2O3. Поясніть відповідь.
|
Al2O3 |
Fe2O3 |
|
Cl2O3 |
|
|
BaO |
MgO |
|
CO |
|
|
SO2 |
MnO2 |
|
NO2 |
|
|
N2O |
K2O |
|
Cl2O |
|
Контроль знань
( робота на карточках)
Варіант №1
1. Визначте ступінь окислення елементів в речовинах. Вкажіть формулу сполуки, у якій Хром виявляє ступінь окислення +7:
а) CrCl2 б) H2CrO4 в) CrO3 г) К2Сr2O7 д) Cr2O3
Варіант №2
1. Визначте ступінь окислення елементів в речовинах. Вкажіть формулу сполуки, у якій Сульфур виявляє ступінь окислення +4:
а) H2S б) Li2SO4 в) Al2S3 г) Na2SO3 д) SO3
Варіант №3
1. Визначте ступінь окислення елементів в речовинах. Вкажіть формулу сполуки, у якій Хлор виявляє ступінь окислення +5:
а) HСl б) NaClO3 в) MgCl2 г) KClO д) Cl2O7
Варіант №4
1. Визначте ступінь окислення елементів в речовинах. Вкажіть формулу сполуки, у якій Фосфор виявляє ступінь окислення -3:
а) H3PO4 б) Ca3(PO4)2 в) Ba3P2 г) HPO3 д) P2O5
VІ. ПІДВЕДЕННЯ ПІДСУМКІВ УРОКУ.
В ході уроку ми закріпили поняття валентність та ступінь окиснення, вдосконалили вміння користуватися ними на практиці. Знання даної теми є важливими для подальшого оволодіння шкільним курсом хімії.
VIІ. ДОМАШНЄ ЗАВДАННЯ
1. Опрацювати §14 і вивчити записи в зошиті.
2.Вправа 111, ст.83.


про публікацію авторської розробки
Додати розробку
