Урок "Вода -- найдивовижніша речовина на планеті"
Земля – планета різноманітних видів життя, але всі вони залежать від одного – води. Вода проникає скрізь: подобається вам це чи ні. Всі живі організми на планеті ділять між собою цю коштовність. Але запаси води небезмежні. Де ж вона знаходиться і куди тече? Якими властивостями характеризується і чому вони притаманні тільки цій речовині?
УРОК-ПРЕЗЕНТАЦІЯ
«НАЙДОРОЖЧИЙ СКАРБ»
Мета навчальна:
дати уявлення про воду як найважливіший природний оксид; визначити роль води в природі та житті людини; узагальнити знання про фізичні властивості води та її кругообіг у природі на основі знань з курсу фізики та географії.
Мета розвиваюча:
з'ясувати вплив забруднення природних водойм на здоров'я людини.
Мета виховна:
виховати в учнів наукові погляди на розвиток природи, збереження її ресурсів як необхідної умови життя.
Тип уроку: презентація.
Міжпредметні зв’язки: біологія, фізика географія, література.
Основні питання:
- Вода в природі.
- Космічний прибулець чи земний абориген?
- Дивовижні властивості води.
- Галузі застосування води.
- Вода в організмі людини.
- Пити чи не пити? Ось у чому запитання!
- Стан водних басейнів України.
ХІД УРОКУ
І. Повідомлення теми, мети й завдань уроку
Сьогодні ми з вами поговоримо про речовину, вартість якої неможливо виміряти ні грошима, ні найціннішими діамантами.
II. Актуалізація опорних знань
Гра “Детектив”.
(Учні ставлять питання, на які вчитель дає відповідь “так” або “ні”.)
Наприклад:
- Це проста речовина? (Ні)
- Вона перебуває у рідкому стані? (Так)
- Чи змінює ця речовина колір лакмусового папірця? (Ні)
- Отже, вона має нейтральне середовище? (Так)
- Це вода? (Так)

Ось ви й відкрили таємничу скриньку, в якій знаходиться наш найдорожчий скарб. А це означає, що сьогодні ми будемо вивчати відому кожному з раннього дитинства речовину — воду.
III. Виклад нового матеріалу
На екрані – відеофільм «Вода», розповідь звучить текстом до фільму.
Земля – планета різноманітних видів життя, але всі вони залежать від одного – води. Вода проникає скрізь: подобається вам це чи ні. Всі живі організми на планеті ділять між собою цю коштовність. Але запаси води небезмежні. Де ж вона знаходиться і куди тече? Скоро дізнаємось.
Наша подорож починається. І ми відправляємось слідом за краплиною води.
Все живе на Землі, вкючаючи людину, залежить від води. Ніхто не може вижити без неї. Ви на 2/3 складаєтесь із води. І прямо зараз вписуєте ще одну сторінку в дивовижну подорож краплини води. Вода, яку ви вип’єте сьогодні колись наповнювала найглибші океани. В кожній склянці є краплини, якими втамовували спрагу тварини, стародавні люди. Випиваючи її ми стаєм ще одним ланцюжком в дивовижному кругообізі води в природі.
Ми відправляємось за краплиною води і довідаємось про незчисленну кількість див, пов’язаних з водою.
Вода – частина всього живого на Землі. Це єдина речовина, яка в природі існує у трьох агрегатних станах: твердому, рідкому та газоподібному. У вигляді криги – взимку, у вигляді рідини – в тропічних морях, у вигляді пари – в джунглях, створюючи неповторну різноманітність видів флори і фауни.
Від найпосушливіших пустель до найвищих засніжених гірських вершин вода безперервно рухається навколо нашої планети. Кожну мить 12 млрд.тон води знаходиться в атмосфері, обгортаючи земну кулю.
Але що ж таке особливе у воді? Вона, в решті решт, не має ні смаку, ні кольору, ні запаху. Щоб відповісти на це запитання – вдивимось уважно в краплину води.
Це молекула води – Н2О (складається з 2 атомів Н, 1 атому О). Молекули зв’язуються між собою водневими зв’язками, що обумовлені електричними силами. Саме ці зв’язки перетворюють воду на дивовижну речовину.
Вода для нас – найзвичайніша річ. Але були часи, коли її не було зовсім. Як вона потрапила на Землю? Щоб відповісти на питання, вирушимо минуле. В те далеке минуле, коли наша планета була зовсім молодою.
4 міліарда років тому...
Серед учених світу триває суперечка відносно того, як виникла вода на нашій планеті. Одностайної думки не дійшли й досі. Найпоширенішою є теорія про космічне походження води. Італійський хімік Пізані вперше отримав докази такої теорії, коли досліджував метеорит, що впав 1864 року поблизу Оргейля в Південній Франції. Учений виявив у складі “космічного прибульця” майже 14 % води. Подальші дослідження підтвердили: всі метеорити містять воду.
 Видатний учений О. О. Шмідт розробив теорію, яка доводить, що планети утворюються внаслідок конденсації газопилових космічних хмар. Газопилові хмари, обертаючись навколо свого центру, поступово ущільнювались, а оскільки серед пилу були й частки, обліплені льодом, вода потрапляла в тіло планети від кори до ядра. Надалі ядро ущільнилось, у ньому почалися процеси, що супроводжувалися виділенням тепла. Космічний лід почав танути і вода з надр поринула на поверхню. Так утворилися океани, моря, річки й озера. Тільки уявіть, завдяки воді ми всі трішечки інопланетяне!
Видатний учений О. О. Шмідт розробив теорію, яка доводить, що планети утворюються внаслідок конденсації газопилових космічних хмар. Газопилові хмари, обертаючись навколо свого центру, поступово ущільнювались, а оскільки серед пилу були й частки, обліплені льодом, вода потрапляла в тіло планети від кори до ядра. Надалі ядро ущільнилось, у ньому почалися процеси, що супроводжувалися виділенням тепла. Космічний лід почав танути і вода з надр поринула на поверхню. Так утворилися океани, моря, річки й озера. Тільки уявіть, завдяки воді ми всі трішечки інопланетяне!
Інше джерело води заховано глибоко-глибоко, в надрах планети. Тут кисень і водень сполучаються між собою, утворюючи водяну пару. Ця пара й кипляча вода вивержуються на поверхню землі у вигляді гейзерів та вулканічних мас.
 За 3 млрд. років атмосфера Землі добре просочилась парами води. Ця пара огортає планету як ковдра, захищаючи її від згубних променів Сонця. Вона затримує і сонячне тепло, створюючи сприятливий для життя клімат. Без води середньодобова температура на планеті складала б --18oС. Земля була б мерзлою пустелею.
За 3 млрд. років атмосфера Землі добре просочилась парами води. Ця пара огортає планету як ковдра, захищаючи її від згубних променів Сонця. Вона затримує і сонячне тепло, створюючи сприятливий для життя клімат. Без води середньодобова температура на планеті складала б --18oС. Земля була б мерзлою пустелею.
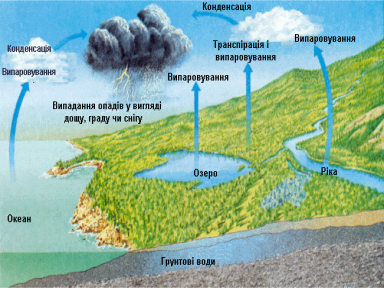
З часом атмосфера Землі прогрівалась і почались дощі. Вода наповнювала океани і моря, а Сонце стало двигуном, який запустив кругообіг води у природі. Ми всі являємось ланцюжками цього великого кола. Дощова вода, що вперше випала тоді, обернулася 8 млн.раз.
Вода перебуває у безперервному ресурсі, вода весь час обертається в процесі кругообігу. З поверхні морів і океанів вона безперервно випаровується. Унаслідок такого випаровування утворюються потужні потоки хмар, енергія яких у вічному кругообігу сил природи перетворюється на дощ, струмочки, річки. Моря й  океани, зігріті сонцем, щороку віддають атмосфері у вигляді водяної пари понад 500 000 млн. м3 води. Це майже трьохсота частина загального об'єму води на землі. Над континентами конденсується приблизно десята частина води, що випаровується.
океани, зігріті сонцем, щороку віддають атмосфері у вигляді водяної пари понад 500 000 млн. м3 води. Це майже трьохсота частина загального об'єму води на землі. Над континентами конденсується приблизно десята частина води, що випаровується.
Але кожну мить якась частина парів води втрачається у верхніх шарах атмосфери. Чи означає це, що запас води колись може вичерпатись?
Для відповіді рушимо до центру Землі. На глибині 30 км – температура перевищує 1000oС. Тут починається мантія, шар, що знаходиться між корою та ядром Землі. В цьому місті знаходиться розпечена вода, її запаси перевищують об’єм Світового океану в 10 раз. Цей гігантський резервуар являється джерелом поповнення води на планеті через виверження гейзерів та вулканів.
Слайд №2.
Отож, вода — це чиста, за звичайних умов безбарвна рідина без смаку і запаху. Температура кипіння 100°С за тиску 101,3 кПа. Температура плавлення — 0 °С. Максимальна густина 1 г/см3 за 4 °С. Вода — одна з найпотрібніших речовин у природі. Загальний об'єм її на Землі 15.1017 м3. На кожного мешканця нашої планети припадає більше 500 млн. м3 води. Такої кількості води вистачить на рік місту з населенням 3 млн. Майже 71 % поверхні нашої планети залито водою. Головне на земній кулі не суходіл, а безкрайній океан — це моря, і ріки, й озера і зовсім тихі сільські ставки.
Відеосюжет про будову молекули води.
Молекула води – це дрібненька молекула, яка має дуже специфічні властивості. Вона характеризується рядом аномалій. Якби не було б хоха б однієї з них – не було б життя на нашій планеті. До цієї пори невідомо, чому тільки вода може перебувати в природі в трьох агрегатних станах. Чому у води найвищий поверхневий натяг з усіх рідин? Чому вона найкращий розчинник на Землі? І яким чином вода здатна підніматись стовбурами велетенських дерев, долаючи тиск у десятки атмосфер?
Те, що вода — найцінніший природний оксид, — не новина. Першим сказав про це мінералог Гаюї на початку XIX ст. Сто років по тому В. І. Вернадський у свої чудовій монографії «Історія мінералів земної кори» присвятив воді багато сторінок — більше, ніж будь-якому іншому мінералу. І тепер у кожному довіднику з мінералогії можна прочитати: «Мінерал цей у земних умовах дуже поширений як у рідкому, так і у твердому та газоподібному станах. Вода — найкорисніша копалина Землі».
 Корисна — навряд чи хтось це заперечуватиме. Копалина — пригадайте, як з допомогою колодязів 1 свердловин добувають підземну воду. Воду шукають частіше, ніж будь-який мінерал. І не лише в спекотних пустелях і сухих степах. Навряд чи знайдеться такий район, де б не проводилися пошуки води.
Корисна — навряд чи хтось це заперечуватиме. Копалина — пригадайте, як з допомогою колодязів 1 свердловин добувають підземну воду. Воду шукають частіше, ніж будь-який мінерал. І не лише в спекотних пустелях і сухих степах. Навряд чи знайдеться такий район, де б не проводилися пошуки води.
Скромний мінерал з простенькою формулою Н20 — найнеобхідніший, найважливіший, найкоштовніший на Землі. Вода — одна з найдивовижніших речовин. її пречудовим властивостям наша планета зобов'язана тим, що на ній з'явилося та розвинулося життя. Жодна інша рідина не має такої сили корисних властивостей. А втім, судіть самі.
Слайд №3.
 Властивість перша: майже всі речовини на Землі під час плавлення збільшуються в об'ємі. Тому вони, як правило, тонуть у власному розплаві. Вода і в цьому разі є аномалією, винятком. Лід має більший об'єм, ніж вода, з якої він утвориться, тому він плаває на воді. Уявіть собі, що вода не мала б цієї надзвичайно рідкісної властивості. Лід, ледве він з'явився б на поверхні водоймищ, одразу ж поринав би на дно. Тоді найглибші океани промерзали б наскрізь. Так само промерзали б озера, ставки, річки. Життя на нашій планеті не змогло б навіть з'явитися.
Властивість перша: майже всі речовини на Землі під час плавлення збільшуються в об'ємі. Тому вони, як правило, тонуть у власному розплаві. Вода і в цьому разі є аномалією, винятком. Лід має більший об'єм, ніж вода, з якої він утвориться, тому він плаває на воді. Уявіть собі, що вода не мала б цієї надзвичайно рідкісної властивості. Лід, ледве він з'явився б на поверхні водоймищ, одразу ж поринав би на дно. Тоді найглибші океани промерзали б наскрізь. Так само промерзали б озера, ставки, річки. Життя на нашій планеті не змогло б навіть з'явитися.
Чому лід плаває, чому моря не промерзають до дна? Замерзаючи молекула води набуває чіткої шестикутної форми. Дрібні кристалики не можуть щільно прилягати один до одного. Між ними утворюються повітряні проміжки, тому лід має меншу густину, ніж рідка вода, є більш легким. Вода має найбільшу густину при 4°С, саме така температура фіксується під кригою водоймища. Моря не промерзають до дна, в них знаходиться велика кількість тварин.
Слайд №

 Властивість друга: вода — найсильніший розчинник. Досить глянути на таблицю хімічного складу морської води, щоб переконатися в цьому. Деякі вчені вважають, що в ній містяться усі без винятку елементи, які є на Землі. А якби вода не мала цієї аномальної для рідини властивості? Адже це вода подає корінням рослин розчинені в ній поживні речовини. Це вона є основою рослинних соків, що розносять ці речовини по коріннях і гілках рослин. Вода — основна частина тваринних організмів та організму людини. Кров людини містить 83 % води, серце й мозок — близько 80 %, кістки — близько 20 %. Цікаво, що в тілі медузи — 99 % води.
Властивість друга: вода — найсильніший розчинник. Досить глянути на таблицю хімічного складу морської води, щоб переконатися в цьому. Деякі вчені вважають, що в ній містяться усі без винятку елементи, які є на Землі. А якби вода не мала цієї аномальної для рідини властивості? Адже це вода подає корінням рослин розчинені в ній поживні речовини. Це вона є основою рослинних соків, що розносять ці речовини по коріннях і гілках рослин. Вода — основна частина тваринних організмів та організму людини. Кров людини містить 83 % води, серце й мозок — близько 80 %, кістки — близько 20 %. Цікаво, що в тілі медузи — 99 % води.
 Властивість третя. Під час охолодження густина води, як і інших речовин, збільшується. Але тільки до певної межі, до +4 °С. Під час охолодження від +4 до 0 °С густина води зменшується. Ця, так би мовити, ненормальна поведінка води має величезне значення. Восени, коли різко знижується температура повітря, охолоджується й вода у водоймищах. Охолодження починається зверху. Охолоджуючись, вода спускається донизу доти, доки температура всього водоймища не знизиться до +4 °С. За такої температури ще цілком можливе життя. З поступовим охолодженням вода вкриває водоймище тонким шаром льоду, що захищає його від подальшого охолодження.
Властивість третя. Під час охолодження густина води, як і інших речовин, збільшується. Але тільки до певної межі, до +4 °С. Під час охолодження від +4 до 0 °С густина води зменшується. Ця, так би мовити, ненормальна поведінка води має величезне значення. Восени, коли різко знижується температура повітря, охолоджується й вода у водоймищах. Охолодження починається зверху. Охолоджуючись, вода спускається донизу доти, доки температура всього водоймища не знизиться до +4 °С. За такої температури ще цілком можливе життя. З поступовим охолодженням вода вкриває водоймище тонким шаром льоду, що захищає його від подальшого охолодження.
 Наступною аномальною властивістю води порівняно з іншими рідинами є те, що зі зниженням температури розчинність газів у ній підвищується. Тому опускання холодної води забезпечує постачання киснем глибинних шарів океанів, морів, озер, річок. Піднімаючись, теплі води, навпаки, виносять розчини солей та інші поживні речовини у верхні шари. Вода має величезну теплоємність. Для порівняння скажемо, що питома теплоємність гасу вдвічі нижча, піску — у п'ять разів нижча, майже в десять разів нижча в заліза, а ртуті — становить ледве 0,03 від теплоємності води. Охолодивши кубічний метр води на 1 °С, можна нагріти тисячу кубічних метрів повітря на З °С. Ця властивість води відіграє велику роль. Завдяки їй вода чудово пом'якшує клімат.
Наступною аномальною властивістю води порівняно з іншими рідинами є те, що зі зниженням температури розчинність газів у ній підвищується. Тому опускання холодної води забезпечує постачання киснем глибинних шарів океанів, морів, озер, річок. Піднімаючись, теплі води, навпаки, виносять розчини солей та інші поживні речовини у верхні шари. Вода має величезну теплоємність. Для порівняння скажемо, що питома теплоємність гасу вдвічі нижча, піску — у п'ять разів нижча, майже в десять разів нижча в заліза, а ртуті — становить ледве 0,03 від теплоємності води. Охолодивши кубічний метр води на 1 °С, можна нагріти тисячу кубічних метрів повітря на З °С. Ця властивість води відіграє велику роль. Завдяки їй вода чудово пом'якшує клімат.
Навесні та влітку вона дуже повільно нагрівається, охолоджуючи готове розпектися повітря. Восени вода поступово остигає, зігріваючи повітря. Завдяки такій значній теплоємності вода переносить величезну кількість тепла з тропічних морів у полярні. Без цієї властивості клімат на Землі був би значно менш сприятливим для життя, незрівнянно суворішими були б зими й спекотнішими літні періоди року. Вода є основним регулятором теплового режиму нашої планети.
 Вода має ще одну аномальну властивість — надзвичайно високу приховану теплоту плавлення. Щоб розплавити 1 кг льоду, треба витратити 79 кілокалорій тепла! У сталі цей коефіцієнт нижчий майже вдвічі, а у свинцю — майже в п'ятнадцять разів. Така властивість води рятує нас від катастрофічних водяних повеней, дає можливість ґрунтам увібрати зайву воду. Цю властивість води також використовують у виробничій діяльності. На багатьох металургійних виробництвах Донбасу як охолоджувач використовують не холодну воду, а окріп. Охолодження відбувається за рахунок теплоти пароутворення. Окріп як охолоджувач використовують там, де потрібно охолодити об'єкти, нагріті більш ніж на 100 °С. Ще один приклад. Коли пізньої весни раптові нічні заморозки загрожують квітучим плодовим деревам, досвідчені садівники заходять вихід, що здається зовсім несподіваним: вони проводять дощування саду. Пелена найдрібніших водяних бризок огортає замерзаючі дерева. Крапельки води покривають пелюстки квітів. Перетворюючись на лід, вода одягає квіти в льодяну шубу, віддаючи їм при цьому своє тепло 335 Дж від 1 кг замерзаючої води. Але й на цьому не закінчується перелік аномальних властивостей води.
Вода має ще одну аномальну властивість — надзвичайно високу приховану теплоту плавлення. Щоб розплавити 1 кг льоду, треба витратити 79 кілокалорій тепла! У сталі цей коефіцієнт нижчий майже вдвічі, а у свинцю — майже в п'ятнадцять разів. Така властивість води рятує нас від катастрофічних водяних повеней, дає можливість ґрунтам увібрати зайву воду. Цю властивість води також використовують у виробничій діяльності. На багатьох металургійних виробництвах Донбасу як охолоджувач використовують не холодну воду, а окріп. Охолодження відбувається за рахунок теплоти пароутворення. Окріп як охолоджувач використовують там, де потрібно охолодити об'єкти, нагріті більш ніж на 100 °С. Ще один приклад. Коли пізньої весни раптові нічні заморозки загрожують квітучим плодовим деревам, досвідчені садівники заходять вихід, що здається зовсім несподіваним: вони проводять дощування саду. Пелена найдрібніших водяних бризок огортає замерзаючі дерева. Крапельки води покривають пелюстки квітів. Перетворюючись на лід, вода одягає квіти в льодяну шубу, віддаючи їм при цьому своє тепло 335 Дж від 1 кг замерзаючої води. Але й на цьому не закінчується перелік аномальних властивостей води.
Якби вода не мала більшості з цих аномальних властивостей, життя на Землі або зовсім не було б, або було б воно далеко не таким могутнім і пишним. Так ось якими, дорогі друзі, чудесно-корисними можуть бути аномалії. Саме аномальні властивості води сприяють життю на нашій голубій планеті Земля. І недаремно в народі кажуть: "Водиця — усього живого цариця", "Де вода, там і життя". Тому й не дивно, що цей незамінний, найкоштовніший мінерал викликає подив, захоплення, бажання оспівувати й возвеличувати його у віршах, піснях, прислів'ях, приказках та порівняннях.
 "...Вода, в тебе немає ні кольору, ні смаку, ні запаху, тебе неможливо описати, тобою насолоджуються, не знаючи, що ти таке. Неправильно сказати, що ти необхідна для життя: ти — саме життя. Ти наповнюєш нас радістю, яку неможливо пояснити нашими почуттями. З тобою починають зростати в нас сили, з якими ми вже попрощалися. З твоєї милості в нас знову починають вирувати висохлі джерела нашого серця», — так писав про воду Антуан де Сент-Екзюпері.
"...Вода, в тебе немає ні кольору, ні смаку, ні запаху, тебе неможливо описати, тобою насолоджуються, не знаючи, що ти таке. Неправильно сказати, що ти необхідна для життя: ти — саме життя. Ти наповнюєш нас радістю, яку неможливо пояснити нашими почуттями. З тобою починають зростати в нас сили, з якими ми вже попрощалися. З твоєї милості в нас знову починають вирувати висохлі джерела нашого серця», — так писав про воду Антуан де Сент-Екзюпері.
Вода є основним середовищем, у якому відбуваються процеси обміну речовин та перетворення енергії. Вода має унікальні хімічні та фізичні властивості. Деякі з них ми вже розглянули. Молекула води Н20 складається з двох атомів Гідрогену, які пов'язані міцним ковалентним зв'язком з атомом Оксигену. Молекула води електронейтральна, бо на її різних полюсах розташовані позитивні та негативні електричні заряди. Це визначає і таку властивість молекули води, як полярність. Вода визначає внутрішньоклітинний тиск, тургор та об'єм клітин.
Вона здатна формувати водну оболонку навколо певних сполук, що запобігає їхній взаємодії між собою. Таку воду називають зв'язаною, структурованою. Її частка становить 4-5 % від загальної кількості води в організмі. Іншу частину води 95-96 %, не зв'язану з іншими сполуками, називають вільною. Саме вільна вода є універсальним розчинником, кращим, ніж більшість інших рідин, через це відіграє надзвичайно важливу роль у живих організмах, оскільки більшість біохімічних реакцій відбувається у водних розчинах.
Вода бере безпосередню участь у реакціях гідролізу — розщеплення органічних сполук з приєднанням до місця розриву іонів молекули води Н+ та ОН-. 3 водою пов'язана також регуляція теплового режиму організмів, їй притаманна велика теплоємність, тобто здатність поглинати тепло за незначних змін власної температури. Завдяки цьому вода запобігає різким змінам температури в клітинах і в організмі в цілому за значних її коливань у навколишньому середовищі. Під час випаровування води організми витрачають багато тепла. Так вони захищають себе від перегрівання. Завдяки високій теплопровідності вода забезпечує рівномірний розподіл теплоти між тканинами організму, циркулюючи по порожнинах органів і тіла.
Важливе біологічне значення для функціонування організмів має і те, що вода під впливом розчинених у ній речовин може змінювати свої властивості, зокрема температуру замерзання і кипіння. Так, із настанням зими у клітинах морозостійких рослин і холоднокровних тварин підвищується концентрація розчинних вуглеводів та інших сполук. Це перешкоджає переходу води в організмах у кристалічний стан і таким чином запобігає їхній загибелі. На перебіг біохімічних реакцій у водних розчинах істотно впливає концентрація іонів Гідрогену.
Будова молекули води (перегляд відео сюжету, слайд № )
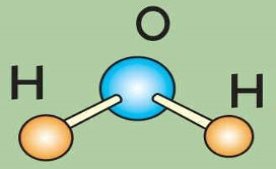 Молекула води являє собою діполь. З одного боку молекули превалює «--» заряд, з іншого – «+». Це відомий факт різноіменно зарядженими краями молекули притягуються. Ще одна молекула, ще... Так формується структура води.
Молекула води являє собою діполь. З одного боку молекули превалює «--» заряд, з іншого – «+». Це відомий факт різноіменно зарядженими краями молекули притягуються. Ще одна молекула, ще... Так формується структура води.
Слайд №
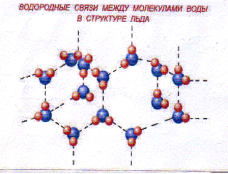 Структура води відіграє більшу роль, ніж хімічний склад води. Структура – це те, як організовані її молекули. Вона рухлива і швидко руйнується. Проте, придивившись можна помітити стабільні утворення – кластери. Вважається, що саме кластери – комірки пам’яті, в які вода як на магнітну стрічку записує все, що «чує» і «бачить», «відчуває».
Структура води відіграє більшу роль, ніж хімічний склад води. Структура – це те, як організовані її молекули. Вона рухлива і швидко руйнується. Проте, придивившись можна помітити стабільні утворення – кластери. Вважається, що саме кластери – комірки пам’яті, в які вода як на магнітну стрічку записує все, що «чує» і «бачить», «відчуває».
Слайд №
Вчені висунули сенсаційну гіпотезу, що всі закони створення світу записані саме у воді. «Золота пропорція», вона ж «божественна суть» була виявлена в молекулі талої води. В звичайній молекулі води кут між зв’язками дорівнює 104 °, в молекулі талої води – незмінно додівнює 108°. А співвідношення довжин водневих зв’язків – 0,618. Це число Фібаначчі.
Післі замерзання—відтаювання у воді стирається вся інформація, крім базової програми життя. Розташування листочків на гілці, пелюсток у квітці, ниточок у павутинні, чудернацька будова мушлі, молекула ДНК, Всесвіт. Саме вода несе програму розвитку всього живого на нашій планеті.
Слайди №
Зміна структури води під дією різних чинників (хімічні речовини, різноманітні звуки, музика, воднева бомба).
Слайди №
Хімічні властивості води
Воду можна одержати шляхом розкладання гідроген пероксиду.
2Н202 → (Мn02) → 2Н20 + 02↑
Мn02 — каталізатор, який прискорює хімічну реакцію, але сам при цьому не бере участі у реакції.
Взаємодія з металами
2Na + 2Н20 → 2NaОН + Н2↑
NаОН — це складна речовина, що належить до класу основ
Zn+ Н20→ZnО + Н2↑
Не всі метали однаково реагують з водою. Ми зможемо описати це cхемою:
Н20 + Ме → (Na, К, Lі, Са, Ва, Мg) → Ме(ОН)n +Н2↑
Н20 + Ме → (Zп, Fе) → МеnОm+ Н2↑
Н20 + Ме → (Си, Ag., Аu) → не реагують
Взаємодія води з оксидами металів
СаО + Н20→Са(ОН)2 — гашене вапно
Взаємодія води з оксидами неметалів
С02+Н20 →Н2С03
S03+Н20 →Н2S04
SiO2 + Н2O ≠
Оксиди неметалів з водою утворюють кислоти.
Способи одержання
У промисловості не одержують, а беруть із природних джерел, очищаючи фізичними та хімічними методами.
- 2Н2 + 02 → 2Н20 — вибух «гримучої суміші»
- СиО + Н2 → Си + Н20
- СН4 + 202 → С02 + 2Н20
- СаО + 2НС1→ Н20 + СаС12
-

NaОН + НС1 → NaCl + Н20 - 2NaОН+C02 → Nа2С03+Н20
А зараз ми повернемося до хімічних властивостей води, про які ми ще сказали.
- ЗН20 + Р205 → 2Н3Р04
- Н20 + С12→ НС1 + НСЮ
- Н20 + С→Н2↑ + СО↑
- 2Н20 + 2F2 → 4НF↑ + 02 ↑
- 2Н20 + СаН2 → Са(0Н)2 + 2Н2↑
- 2Н20 →2Н2↑ + 02↑
Слайди №
Галузі застосування
- Як хімічна сировина: для одержання водню, кисню, кислот, лугів, різних органічних сполук.
- Як розчинник у різних галузях промисловості, у будівництві, на транспорті.
- У парових двигунах, системах охолодження й опалення.
- У побуті, а також для зрошення полів, садів і городів.
- Як каталізатор.
- Є найважливішою біологічною рідиною, необхідною для процесів життєдіяльності живих організмів травлення, кровообігу, розмноження.
Жодна рідина у світі не має такої кількості корисних якостей, як вода. Вода чудовий розчинник. У ній розчиняють майже всі речовини. Морська вода містить близько 60 елементів періодичної системи Менделєєва. Деякі вчені вважають, що у воді є всі хімічні елементи без винятку.
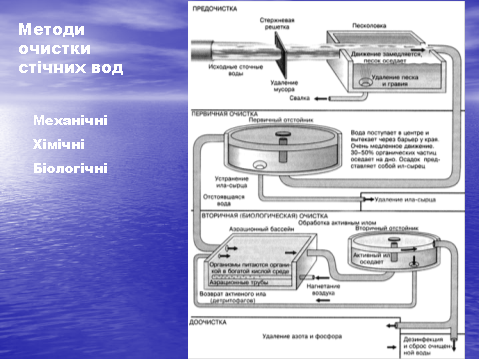
Існують такі види води: дистильована, прісна, жива, грозова, аномальна та інші види води. Для побутових потреб людина використовує воду з річок, озер або підземних джерел. Природна вода ніколи не буває чистою. Крім розчинних домішок вона містить тверді частинки піску, глини, рештки рослин і тварин, різноманітні мікроорганізми. Серед останніх можуть бути і хвороботворні, які, потрапляючи до організму людини, чи тварин, викликають різні захворювання. Тому природну воду перед уживанням очищують. Для очищення води від твердих диспергованих речовин її фільтрують через пористі речовини вугілля, випалену глину, фільтри-преси, суміш піску з гравієм. Фільтри затримують також більшу частину бактерій. Крім того, для знезаражування води її хлорують. Для повної стерилізації води треба не більше 0,7г хлору на 1 тонну води. З цією ж метою використовують озон. Фільтруванням можна видалити з води тільки нерозчинні домішки. Хімічно чисту воду одержують шляхом перегонки дистиляції.
У наш час очищують не тільки питну, але й стічні води, особливо води теплоелектростанцій, хімічних підприємств. Адже проблема охорони навколишнього середовища стає все більш актуальною, а одним із головних завдань людства є збереження чистоти водних ресурсів.
Вода — найсильніший поглинач сонячного тепла на поверхні Землі, й основна роль у цьому належить Світовому океану. Від поверхні океану відбивається 8 % сонячної радіації. Завдяки високій теплоємності води океани виступають акумулятором сонячної енергії на планеті, а поверхневі течії океанів переносять тепло по планеті, впливаючи на клімат.
Сонце — великий енергетик. Воно нагріває воду всюди, де вона є: Метеорологи підрахували, що Сонце випаровує на Землі за 1 хвилину мільярд тонн води. Енергія Сонця, яка піднята з водяною парою, виділяється назад. Кожну хвилину водяна пара віддає атмосфері Землі велику кількість енергії — 2,2 1018 Дж.
Стільки енергії за короткий час можуть виробити 40 млн. електростанцій. Ця енергія переходить у теплову, нагріваючи повітря. Це вона переносить воду у хмарах і зрошує дощами поверхню Землі. Вода дуже широко застосовується людиною.
Важко уявити собі хоч одну галузь промисловості, де не використовується вода. її енергія нас зігріває, плавить метал, перевозить мільярди людей. З допомогою спеціальних приладів, які дають змогу отримати надтонкий струмінь води, під величезним тиском «ріжуть метал», «рубають» вугілля у шахтах. Працює вода у ковальських цехах: металевий лист, що знаходиться на прес-формі, поміщають у спеціальний резервуар, який заповнюють водою і герметично закривають. Унаслідок гідроудару лист деформується і набуває форми тієї заготовки, на якій він лежав. Таким чином, з мінімальними витратами можна отримати, наприклад, крило автомобіля чи навіть кузов.
З давніх-давен вода збуджувала уяву людини. Безліч легенд, народних казок, прислів'їв, повір'їв пов'язані з водою. Наприклад, «мертва» і «жива» вода, релігійні обряди водохрещення, цілющі властивості «святої» води, тощо.
Люди бачили, що у воді живуть різні істоти, наземні рослини ростуть завдяки воді, та й людина не може без неї жити.
У 1805 р. Ж. Гей-Люссак і А. Гумбольдт встановили класичну формулу води — Н20. Отже, це природний оксид, назва якого гідроген оксид.
Перевіримо ваші знання про воду, які ви вже маєте.
- Що являє собою вода за нормальних умов?
- В яких агрегатних станах перебуває вода на Землі? (У рідкому, твердому та газоподібному)
- Що відбувається з водою за температури 100 °С? (Вода кипить, перетворюючись на пару)
- Що спостерігаємо за температури 0 °С? (Вода, перетворюючись на лід, переходить у твердий стан)
- Чому лід плаває на поверхні води? (Його густина менша за густину води в рідкому стані)
- Чому дорівнює густина води? (р = 1 г/см3)
- Чи може вода поглинати тепло? (Так, велику кількість, при цьому сама істотно не нагрівається)
- Чи проводить вода електричний струм? (Лід і дистильована вода не проводять, а вода, в який розчинені солі, — так)
- Чи може вода проводити звуки? (Так, завдяки її звукопровідності «спілкуються» живі істоти, які населяють воду)
10) Чи є вода в організмі людини? (Так, дуже багато)
Слайд №
В безмежному космічному просторі ми шукаємо відповідь на розв’язання стародавньої тайни – тайни створення світу. А відповідь знаходиться тут – на маленькій блакитній планеті. Це знання завжди було поруч з людиною. Дар, який ми називаємо життям, був довірений одній, єдиній в світі речовині, яка здатна зберегти і передати його людям – воді.
Чи знаєте ви, що...
.. .радіоспостереження з орбіти супутників дають можливість вивчати розподіл температури Світового океану, запас вологи в хмарах, кількість водяної пари в атмосфері, зафіксувати зони опадів, штормів і сильного морського хвилювання, що має велике значення для метеорології?
...опромінюючи чисту воду ультразвуком, можна одержати гідроген пероксид?
...у Світовому океані на кожного жителя планети припадає близько З млн. м3 води?
...якби висота земної кори була всюди однакова, наша планета вкрилася б шаром води заввишки 2 400 метрів?
...звук у воді поширюється у п'ять разів швидше, ніж у повітрі?
...в Антарктиді сконцентровано 87 % льодових запасів планети, а середня товщина льоду становить 2,5 км?
...теоретично в абсолютно чистій воді такий поверхневий натяг, що по ній можна ходити, кататися на ковзанках. Але практично абсолютно чисту воду ще ніхто у світі не одержав?
...довжина Дніпра становить 2 200 км, а площа його басейну — 504 тис. км2?
...під 400-метровим шаром антарктичного льоду розташоване море, глибина якого близько 200 м, на його воду понад 120 тис. років не потрапляло сонячне світло, але дивно те, що в ній виявлено життя — ракоподібні тварини та одноклітинні рослини — діатомеї?
...підвищення температури води в гарячих джерелах— ознака землетрусу, який наближається?
...людина може прожити без їжі тиждень, без води — п'ять днів, без повітря — п'ять хвилин.
...цінні породи дерев сушать у воді? Для цього крізь воду, в якій знаходиться дерево, пропускають електрострум, який у деревині проходить швидше, ніж у воді, і тому деревина виділяє надлишок вологи у воду.
...об'єм усієї води на нашій планеті становить 1 800 млн. км3?
...використання води як пального не забруднює навколишнє середовище? Одержаний із води водень — джерело палива. Окиснюючись, він знову дає воду. З води океанів і морів можна одержати 1,3 • 1018 т водню. Такої кількості водню як пального вистачило б на мільйони років.
...роль пилки може виконувати вода? Сильний струмінь води під тиском ріже навіть метал.
...перепис снігу і льоду показав, що загальна маса льоду на поверхні землі становить майже 2/3 води планети?
...за температури —ЗО...—60 °С сніг випадає у вигляді льодяних кристалів (голок, пластинок, призм), а там, де вологий клімат, — у вигляді багатогранних і ажурних шестигранних зірочок?
...пустелі є на території 50-ти країн? Площа посушливих земель становить 47 млн. км2, або 35 % поверхні материків, що в три з половиною аза більше, ніж площа всіх сільськогосподарських угідь на планеті.
...загальна поверхня земної кулі становить 510 млн. км2, із них суша — 149 млн. км2?
...близько 86 % водяної пари надходить в атмосферу в результаті випаровування води з поверхні морів та океанів, 14 % — з поверхні суші?
...найбільшу кількість радіоактивних речовин містять тумани і мряка?
...воїни легендарної Малої землі користувалися джерелом прісної води, розміщеним на відстані 100 м від ворога? Шлях до джерела обстрілювався перехресним вогнем. Фляга води нерідко коштувала життя кількох воїнів.
...в Яворівському районі на Львівщині вперше в країні видобувають сірку з допомогою води, нагрітої до 160 °С?
Пити чи не пити? Ось у чому запитання!
1-й учень. Основна маса води нашої планети (95 %) — це солона вода морів і океанів — не придатна для вживання людиною. 5 % становить прісна вода, з яких 4 % — вода, яка міститься в льодовиках і не може використовуватись людиною.
Отже, для задоволення потреби людини у воді залишається тільки 1 %.А потреби ці значні. (Демонструється інформаційний плакат.)
Чи знаєте ви, що...
...за все життя людина випиває 75 тонн води?
...85 % усіх захворювань передаються водою?
...найбільш цінною є тала вода?
...людина може прожити без їжі тиждень, без води — п'ять днів, без повітря 5 хвилин?
...одержаний з води водень — паливо, яке не забруднює навколишнє середовище?
...роль пилки може виконувати вода? Сильний струмінь води під тиском ріже навіть метал,
...водопровідну воду можна кип'ятити тільки після того, як вона відстоялась не менше доби.
Стан водних басейнів України
Недарма видатний музикант і хімік І. П. Бородін стверджував: «Природа — такий же унікум, як картина Рафаеля. її легко зруйнувати, а відновити — неможливо».
Господарча діяльність людини, розвиток промисловості, катастрофа на Чорнобильській АЕС, нехтування принципів раціонального природокористування — ось основні складові кризової ситуації, що склалася в нашій державі. Дніпро, Дністер, Буг, Чорне та Азовське море, безліч малих рік складають водний басейн України.
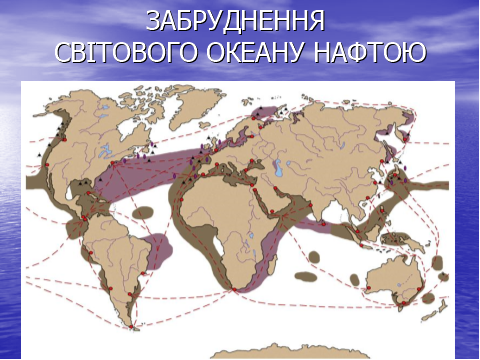
Забруднення води
|
Види забруднення |
Приклади |
|
1. Фізичні |
Пісок, глина |
|
2. Біологічні |
Бактерії, віруси |
|
3. Хімічні |
Добрива, отрутохімікати, бензин, машинне масло, нафта, каналізаційні стоки, викиди підприємств |
|
4. Теплові |
Тепла вода із заводів, пралень |
|
5. Механічні |
Сміття |
Ми живемо в басейні ріки Прут. Це одна з найбільших річок Європи, яка раніше була чистою, характеризувалась великою біологічною продуктивністю, годувала і напувала мільйони людей. Нині екосистема Прута повністю деградована.
Так, щорічно з Прута для потреби промисловості відбирають близько 10 млрд. кубометрів води.
Щорічно з різними стоками в Прут потрапляє близько 350 тис.т. сполук Нітрогену, 37 тис. т фосфорних, 14 тис. т калійних, близько 1 тис. т заліза, 42 т нікелю, 1 т цинку, 1 т міді, 0,2 т хрому. Зараз води Прута — це суміш небезпечних для життя речовин.
Уявіть собі що ви директор заводу мер міста санітарний лікар учитель учень водій. Які методи роботи ви будете впроваджувати з метою покращення екологічної ситуації в місті? Назвіть три основні положення.
Давньогрецький філософ Фалес говорив: «Початок і сутність усього — вода».
Отже, розповісти все-все про цю дивовижну речовину під час однієї зустрічі просто неможливо, та ми й не ставили перед собою такої мети. Але сподіваємося, що після всього почутого ви зрозуміли: вода — це найцінніший мінерал Землі, який потребує від нас дбайливого, економного ставлення. А щоб правильно використовувати речовини, треба вивчати їх властивості, досліджувати їх поводження в присутності інших речовин.
Дуже дивно, що все, що стосується води, ми сприймаємо як незаперечний факт. Можемо ми, чи повинні контролювати кругообіг води в природі? Чи взагалі не варто втручатися в цей процес? Наші спроби змінити щось в цьому процесі, якій вивірений тисячоліттями, може скінчитися катастрофою. День став набагато довшим, ніж був у минулому столітті, витрати води все збільшуються, і виникають сумніви: невже водний резервуар буде колись вичерпаний. Як же попередити катастрофу?
Неможливо зазирнути в майбутнє. Але одне відомо точно: кругообіг води змінити неможливо: ні прискорити, ні уповільнити. Не було б кругообігу життя...
Додатки

Слайд № 1

Слайд № 2

Слайд № 3

Слайд № 4

Слайд № 5

Слайд № 6

Слайд № 7

Слайд № 8

Слайд № 9

Слайд № 10

Слайд № 11

Слайлд № 12

Слайд № 13


Слайд № 14

Слайд № 15

Слайд № 16

Слайд № 17

Слай № 18

Слайд № 19

Слайд № 20

Слайд № 21

Слайд № 22

Слайд № 23

Слайд № 24

Слайд № 25
Слайд № 26

Слайд № 27

Слайд № 28
Слайд № 29

Слайд № 30

Слайд № 31

Слайд № 32
1


про публікацію авторської розробки
Додати розробку
