Узагальнення знань з теми: «Властивості основних класів неорганічних сполук»
Дана розробка допоможе:
- у цікавій формі узагальнити і закріпити знання про хімічні властивості основних класів неорганічних сполук і їх взаємоперетворення;
- розвивати уміння складати хімічні формули за валентністю, рівняння хімічних реакцій;
- вдосконалювати вміння експериментально підтверджувати хімічні властивості речовин.
- сприяти розвитку креативного мислення, мовних навиків.
- розвивати творчий потенціал учнів при підготовці до уроку.
- виховувати бажання активно вчитися, з цікавістю, без примушення.
Дата ______ Клас _____ Вчитель: Дерев’янко Л.В.
УРОК № ______
Узагальнення знань з теми:
«Властивості основних класів неорганічних сполук »
Мета :
- у цікавій формі узагальнити і закріпити знання про хімічні властивості основних класів неорганічних сполук і їх взаємоперетворення;
- розвивати уміння складати хімічні формули за валентністю,
рівняння хімічних реакцій;
- вдосконалювати вміння експериментально підтверджувати хімічні
властивості речовин.
- сприяти розвитку креативного мислення, мовних навиків.
- розвивати творчий потенціал учнів при підготовці до уроку.
- виховувати бажання активно вчитися, з цікавістю, без примушення.
Тип уроку: узагальнення і систематизація знань
Форма проведення : урок-подорож
Форми роботи: робота у групах-екіпажах, індивідуальна, експериментальна робота, творчі ігри «Знайти родичів», «Розсипані формули», «Відгадай загадку», складання рівнянь реакцій , складання та розв’язування задач, кросворду « Назви сіль », здійснення ланцюжків послідовних перетворень.
Обладнання:
- Періодична система хімічних елементів Д. І. Менделєєва,
- таблиця розчинності,
- ряд активності металів,
- картки із завданнями,
- пробірки, штатив для пробірок, спиртівка, трубка з газовідвідною пробкою, дерев’яний тримач,
Реактиви: вапняк, розчини речовин : натрій гідроксиду, сульфатної кислоти , хлоридної кислоти, купрум (ІІ) хлориду.
Базові поняття і терміни: оксид, основа, кислота, амфотерний гідроксид, сіль, генетичний зв’язок.
Підготовка до уроку. На першому уроці з теми «Основні класи неорганічних сполук» вчитель оголошує про майбутній урок-подорож. Клас об’єднується у чотири екіпажі. Кожен екіпаж вибирає собі консультанта (учня, що має міцні знання з предмету). Надалі консультанти готують свої екіпажі до гри-подорожі. З метою підготовки до цього уроку в класі вивішуються питання, на які слід звернути увагу.
На даному етапі учні повинні:
- класифікувати неорганічні речовини по складу і властивостям;
- складати генетичні ряди металів і неметалів;
- ілюструвати рівняння хімічних реакцій, генетичний зв'язок між членами ряду;
- характеризувати хімічні властивості речовин даного класу;
- вміти доводити основний та кислотний характер властивостей
неорганічних сполук;
- визначати практично за допомогою хімічних реакцій розчини кислот, лугів,
хлоридів, сульфатів, карбонатів.
ХІД УРОКУ
- Організація класу.
Кожен екіпаж сідає за окремі столи на чолі з консультантом.
На магнітній дошці прикріплені номери груп-екіпажів.
Після кожного завдання на дошці відмічаються результати за допомогою різнокольорових знаків :
- червоний - екіпаж слідує далі в експресі, тому що завдання виконано на високому рівні ,
- жовтий - пасажирський вагон, завдання виконано на достатньому рівні,
- сірий - загальний вагон, завдання виконано на середньому рівні,
- чорний – дрезина, завдання виконано на початковому рівні.
Учитель. Екіпажі готові до подорожі? Тоді в путь! Сьогодні ми з вами, діти, проводимо узагальнюючий урок з теми : «Основні класи неорганічних речовин». А для цього я запрошую вас зробити подорож в дивовижну і загадкову хімічну країну. Багато у неї таємниць і загадок. Країну цю населяють безліч маленьких істот-речовин. Кожен народ має свій хімічний склад, особливості, звичаї, традиції. У цій дивовижній країні живуть речовини прості і складні, спокійні, врівноважені, неспокійні, просто буйні; отруйні і нешкідливі; корисні і дуже шкідливі; кислі і солоні, солодкі і гіркі, смачні і без смаку; конфліктні і компромісні, що мають різні погляди на ставлення один до одного, але живуть вони за загальними хімічними законами в мирі, злагоді і взаємній повазі. Я запрошую вас в країну Хімію.
Жителі цієї країни надіслали нам запрошення, під яким вони залишили свої автографи. Відгадавши кожен з них, ми зможемо вирушити в дорогу.
Завдання 1. «Знайти родичів»
А1 (ОН) 3, СO2, Mn2O7, HNO3, H2SiO3, Na2[Zn (ОH)4], Mg (OH) 2, CaCO3, RbOH, CuO, HBr, FeO, CsOH, Ca (OH) Cl, H2SO4, K2NaPO4, A1 (OH) 2C1 , NaHCO3, KC1O3, V2O5, H3PO4, H2Se, NaOH, Al2O3, CuSO4, Fe(OH)3, HCl, K2O, Ba(OH)2, Cu(OH) 2, ZnO, H3As O4.
До дошки виходять по одному учаснику від кожного екіпажу.
Учень з першого екіпажу виписує основні, кислотні і амфотерні оксиди;
другого - розчинні і нерозчинні основи;
третього - кислі,основні, середні,комплексні та подвійні солі;
четвертого - кислоти одноосновні, двоосновні, трьохосновні.
Учитель. Отже, ви впоралися з першим завданням, і ми можемо вирушати в дорогу. Займіть , будь ласка, свої місця згідно «куплених квитків».
Ось ми і в гостях у місцевих жителів. Але їх так багато. Давайте прочитаємо, що ж це за станція. (Оксиди.)
Значить, ми на станції «ОКСИД». А ось і її начальник. Подивіться, що він нам приніс. Це нове завдання. Якщо ми з ним впораємося, нам дадуть «зелене світло». Чи відомо вам, діти, які є оксиди на світі?
Завдання 2 . «Відгадай загадку»
- У цих оксидів пристрасті різні:
То кислоти їм подобаються кислі,
То до води їх душа схиляється ,
Та не з усіма вона дружить збирається.
Скажіть, як такі оксиди називаються?
(Основні оксиди.)
- А в цих пристрасті свої
До основ спішать вони,
Розчинні, дуже бажані,
Але у води не всі в пошані.
Ти це згадай
І назву цьому оксиду дай.
(Кислотний оксид.)
- Буває оксид двоїстий,
На совість він не чистий,
То до сильної кислоти поспішає,
То луг до себе пригортає,
І тим і іншим поклоняється.
Як такий оксид називається?
(Амфотерний оксид.)
За кожну правильну відповідь команда отримує додатковий бал, який враховується після кожного завдання при визначенні «класу» вагона.
Учитель. Ми їдемо далі. Щоб нам не було нудно, давайте пограємо гру
«Розсипані формули».
Гра «Розсипані формули»
Складіть формули всіх можливих оксидів, комбінуючи нижчеприведені складові частини по горизонталі (зліва направо) і вертикалі (зверху вниз) за умови, що складові частини повинні стояти поряд. Сума всіх оксидів дорівнює відносній атомній масі атома Карбону.
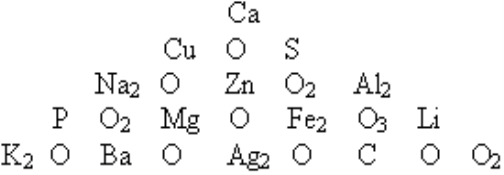
Учитель. Ми з вами і не помітили, як пролетів час і ми під'їхали до нової станції. О! Та це станція експериментів, а називається вона «Основи».
А ось і начальник станції із завданням.
Конфуцій одного разу сказав: “ Добре володіти природним даруванням, але вправи, друзі, дають нам більше, ніж природне дарування ”. Перевіримо ваші практичні навики і уміння.
Я зачитую вам вірш про властивості основ.
Після кожних чотирьох строчок віршу ви будете виконувати експеримент і записувати рівняння реакції в зошит. Учень, який складе рівняння першим записує його на дошці , а екіпаж - отримує додатковий бал.
Прошу консультантів приступити до роботи, ваша мета - перевірити техніку експерименту і допомогти своїй команді у виконанні досліду.
Завдання 3. « Практичне»
Згадаймо про їдку основу.
Наллємо до неї кислоту,
Вагань нема ,бо маємо ми знову
Лиш сіль та воду на яву.
Учні проводять реакцію нейтралізації натрій гідроксиду сульфатною кислотою .
Тепер візьмемо оксид кислотний
І гідроксид, розчинний у воді,
То під водою, аж на дні пробірки -
Чергова сіль лежить тобі.
Учні виконують експеримент. Одержують вуглекислий газ і пропускають його через розчин гідроксиду кальцію.
А якщо до солі луг додати,
То інша сіль й основа на яву.
Але цьому не варто сліпо довіряти,
Бо пам’ятку ми знаємо одну!
Питання. Про яку пам’ятку йдеться мова ?
Відповідь . Солі взаємодіють з лугами, якщо одна із новоутворених речовин (сіль або основа ) є нерозчинною.
Учні проводять реакцію взаємодії натрій гідроксиду з купрум (ІІ) хлоридом .
В раніш добутий нерозчинний гідроксид,
Ви кислоту долийте поступово ,
А в результаті – осад зник,
Бо сіль з водою утворилась як відомо.
Учні виконують реакцію взаємодії купрум (ІІ) гідроксиду з хлоридною кислотою.
Ну і останнє, про що я хочу нагадати ,
І це вам також необхідно знати,
Що нерозчинну основу
При нагріванні можна розкладати.
Учні розкладають купрум (ІІ) гідроксид.
Учитель. Увага! Наступна станція – «КИСЛОТИ»
Після кожного віршу(крім першого) необхідно записати на дошці рівняння реакції. Перш ніж ми дивитимемося реакції , один учень від кожного екіпажу спробує скласти умову задачі до реакції, що запропонував їх екіпаж (Індивідуальне завдання).
Право першої відповіді має екіпаж, з більшою кількістю балів.
Кислота та синій лакмус –
Лакмус зразу став червоним.
Визначають так кислоти
У день гожий і негожий.
Всі кислоти, крім нітратної,
1 метал, що є до водню,
Реагують так завзято,
Що утворять сіль і водень.
В кислоту додай оксид ти,
Того, справжнього металу,
І без сумніву одержиш
Сіль і воду ти по праву.
Кислота і всі основи
Взяли вже собі за моду,
Де б не стрілися вони -
Враз утворять сіль і воду.
У кислот і солей є договір законний ,
Радо бачаться вони лиш при одній умові.
Пам’ятку мерщій згадай
І рівняння ці складай.
А тепер подивимося на складені рівняння реакцій (перевірка написання реакцій).
І так, нам пропонують вирішити наступні задачі (учні зачитують умови і розв’язують їх біля дошки ,інші – в зошитах ( чотири варіанти). Потім перевіряють один у одного, оцінюють, звіряючись з розв’язком на дошці).
Після підведення підсумків цього завдання учитель оголошує:
- Діти, ми прибуваємо до останньої станції цієї країни - «Солі».
- Погляньте , що написано на будівлі станції:
О, Сіль! Як багато в цьому слові
Для серця хіміка злилось,
Багато в ньому озвалось.
А тут нас з вами зустрічає гід - натрію хлорид. (Входить хлорид натрію - учень, одягнений у білий халат з написом NaCl.)
Хлорид натрію. Добрий день! Я проведу невелику екскурсію для вас по нашій станції. Раз ви до нас доїхали, значить, ви добре знайомі з нами. І я розповім вам трохи про себе.
У всіх країнах вживають сіль. І це не дивно. Без солі не можуть жити люди і тварини. Дорослій людині для підтримки життєдіяльності необхідно отримувати 8 - 10г солі щодоби. Недолік солі (як, втім, і її надлишок) згубно позначається на здоров'ї. Сіль міститься в слині, шлунковому соку; наявність солі в крові забезпечує необхідний осмотичний тиск.
Вважають, наприклад, що масова загибель наполеонівських солдатів, особливо поранених, під час відступу була обумовлена нестачею кухонної солі. У стародавніх народів нерідко були війни через соляні джерела, а деякі народи Африки платили колись за сіль золотим піском. Римські легіонери часів Цезаря частину платні отримували сіллю. Сіль заміняла гроші в багатьох країнах. У багатьох народів сіль - символ гостинності, вірності, привітності. Хлібом-сіллю зустрічають дорогих гостей.
Жителі нашої станції приготували для вас всього одне нескладне завдання.
Завдання 4. Кросворд « Назви сіль »
У виробництві та побуті часто користуються технічними назвами солей. Заповніть клітини кросворду назвами солей, формули яких наведені:
1. Cu2 (OH) 2CО3
2. CuSO4 • 5Н2О
3. Na2B4О7 • 10Н2О
4. AgNO3
5. К2СО3
6. NaCl
7.KMnO4
8. Na2СО3
4 6
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
5 |
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
8 |
|||||||||||||||||||||||||
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
7 |
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
||||||||||||||||||||||||||||
Відповіді до кросворду «Назви сіль»
4 6
|
1 |
м |
а |
л |
а |
х |
і |
т |
|
|
к |
|
|
|
|
||||||||||||||||||||
|
я |
|
|
|
|
|
5 |
б |
у |
р |
а |
|
|
||||||||||||||||||||||
|
п |
|
х |
|
|
8 |
|||||||||||||||||||||||||||||
|
|
2 |
м |
і |
д |
н |
и |
й |
к |
у |
п |
о |
р |
о |
с |
|
|
с |
|
||||||||||||||||
|
|
с |
|
|
|
о |
|
н |
|
о |
|||||||||||||||||||||||||
|
|
|
|
|
т |
н |
д |
||||||||||||||||||||||||||||
|
м |
а |
р |
г |
а |
н |
ц |
і |
в |
к |
а |
||||||||||||||||||||||||
|
|
ш |
|
||||||||||||||||||||||||||||||||
Відповіді:
1. Малахіт. 5. Поташ.
2. Мідний купорос. 6. Кухонна.
3. Бура. 7. Марганцівка.
4. Ляпіс. 8. Сода.
Учитель. Ну, ось і закінчилася наша подорож, і ми вирушаємо додому.
Діти, нам уже час повертатися, але я загубила нашу маршрутну карту. Тепер не знаю, якою дорогою поїдемо додому. Але ви можете мені допомогти - необхідно здійснити ланцюжок послідовних перетворень. Якщо це буде зроблено вірно, ми дізнаємося коротший шлях і вирушимо назад.
CuCO3 ? Cu
CuSO4 ? ? Cu
(Учні виконують завдання. Вчитель перевіряє правильність виконання)
Учитель. Я вітаю всіх з успішним подоланням перешкод на шляху та думаю, що ви загартувалися в дорозі і будете впевненіше відчувати себе у різних життєвих ситуаціях, де необхідно використати знання про неорганічні речовини. Не забудьте зробити замітки у ваших щоденниках. (див. домашнє завдання)
VI. Домашнє завдання
Опрацювати §28 - 39 підручника( О.В. Григорович . Хімія 8 клас. Харків, «Ранок», 2016)
- Творче завдання. Скласти і виконати генетичний ланцюжок перетворень за участі відомих вам класів неорганічних сполук та скласти і розв’язати задачу за рівнянням хімічної реакції про улюбленого представника будь – якого класу.
- VІІ. Рефлексія.
- Чи сподобалось вам подорожувати ?
- Що найбільше сподобалось, запам’яталось?
- Що могло б бути краще ?
- Що із сьогоднішнього уроку ви б використали у житті?
VIІІ. Оцінювання роботи учнів .

про публікацію авторської розробки
Додати розробку
